Тверді розчини як розчини молекул. Поняття міналу.
|
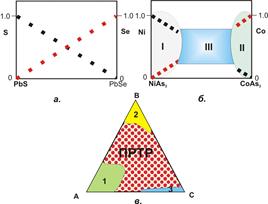
| Рис. 6.3. Схеми варіацій хімічного складу твердих розчинів. ПРТР – продукти розпаду твердих розчинів. |
Тверді розчини можна уявити як взаємне розчинення молекул, що відповідають різним мінеральним видам. Так, твердий розчин форстериту Mg2[SіO4] та фаяліту Fe2[SіO4],що називається олівіном (Mg,Fe)2[SіO4], можна показати як твердий розчин молекули фаяліту (Fa) у форстериті (Fo). Склад мінералу із формулою (Mg0.85Fe0.15)2[SіO4] є результатом взаємного розчинення цих молекул і може бути записаний як Fo0.85Fa0.15. У такому твердому розчині існує, в першому наближенні, дві катіонні кристалохімічні позиції. Тетраедрична позиція Si є спільною для обох молекул, а друга може заселятися Fe або Mg в однаковій мірі. У наведеному прикладі, 85% точок, що відповідають другій кристалохімічній позиції, заселено Fe, а 25% - Mg. Якщо прийняти склад розчину за одиницю, то це рівнозначно розчину, у якому 0.15 часток молекули Fa (Fe2[SіO4]) розчинилось у 0.85 часках молекули Fo (Mg2[SіO4]). Ці уявні компоненти (молекули)) (Fo і Fa у даному випадку), що формують твердий розчин, називаються міналами. У розгляненому випадку, олівін є твердим розчином фаялітового та форстеритового міналів.
Сполуки, що відповідають міналам, повинні мати подібну кристалічну структуру. Вони можуть реально існувати як мінерали, або ж бути уявними, тобто фази такого складу і такої структури в чистому вигляді нестабільні у природних умовах.
Склад твердих розчинів може бути зображений графічно (рис. 6.3), якщо по осі ординат покачати частку одного із міналів, а по осі абсцис – вміст іншого міналу в мінералі. У цьому випадку можливі два варіанти:
1. Точки складу утворюють неперервну лінійну послідовність, як у випадку твердого розчину галеніту PbS і клаусталіту PbSe.
- Точки складу утворюють локальні лінійні послідовності, розірвані областю відсутності відповідних складів. На рисунку 6.3б в області можливих складів твердого розчину рамельсбергіту NiAs2 і сафлориту CoAs2 виділяються поля І і ІІ, в межах яких склад твердого розчину змінюється неперервно, і поле ІІІ, в межах якого точки складу твердого розчину відсутні.
Якщо два мінерали можуть утворювати тверді розчини між собою і, як результат їх взаємного розчинення, спостерігається неперервна зміна хімічного складу твердого розчину від одного мінералу до іншого, тоді ми маємо справу із неперервним рядом твердих розчинів(приклад твердого розчину галеніт-клаусталіт Pb(S,Se)).У термінах ізоморфізму йому відповідають поняттяповногоабодосконалого ізоморфізму. Такий стиль взаємного розчинення спостерігається між крайніми членами ряду гранатів - гросуляром Ca3Al2[SіO4]3 та андрадитом Ca3Fe3+2[SіO4]3 та серед карбонатів між сидеритом Fe[CO]3 і магнезитом Mg[CO3].
Якщо ж в ході взаємного розчинення двох міналів стабільні кристалічні структури виникають тільки в декількох вузьких інтервалах, тоді ми маємо справу із перервними рядами твердих розчинів. У термінах ізоморфізму йому відповідають поняттячастковогоабонедосконалого ізоморфізму.
У випадку формування твердого розчину в певному інтервалі хімічного складу існує гомогенна кристалічна фаза – мінерал із стабільною кристалічною структурою; збільшення вмісту одного із компонентів призведе до нестабільності структури твердого розчину і перетворення гомогенної мінеральної фази у зросток двох мінералів. Це явище гетерогенізації називається розпадом твердого розчину.
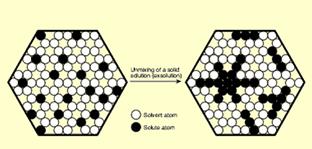
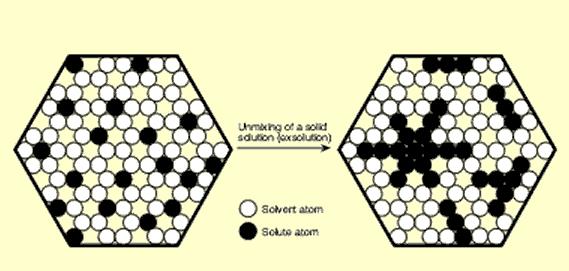
Продуктами розпаду твердих розчинів є включення мінералу–розчиненого компоненту, закономірним чином розміщені в матриці мінералу–розчинника. Орієнтація і морфологія дочірніх мінеральних включень часто підпорядковується кристалічній структурі мінералу-господаря (рис. 6.4 і 6.5). Структури, що утворюються таким чином, називаються структурами розпаду твердих розчинів.
| 
|
| Рис. 6.4. Схема, що показує розпад твердого розчину корунд Al2O3 – гематит Fe2O3. При розпаді твердого розчину атоми Fe переміщуються і формують кристали гематиту в матриці корунду. Орієнтація цих кристалів співпадає із симетрією мінерала-господаря і паралельна призмі {1010} корунду. | Рис. 6.5. Зерно діопсиду CaMgSi2O6 із орієнтованими включеннями енстатиту Mg2Si2O6; при високих температурах взаємна розчинність обох мінералів є повною. При зниженні температури твердий розчин розпадається із формуванням двох мінеральних фаз, розподіл Ca і Mg в яких відповідає мінімуму вільної енергії в системі. The view from the University of Melbourne: http://jaeger.earthsci.unimelb.edu.au/Images/Mineralogical/Textures/main.html. |
Дата добавления: 2015-05-21; просмотров: 1921;
