ПРОИЗВОДСТВО МЕТАНОЛА
Метанол является ценным крупнотоннажным продуктом, находящим широкое применение в различных отраслях промышленности.
Объем потребления метанола в мире непрерывно возрастает. В настоящее время его мировое производство превышает 20 млн. т/год.
Традиционным потребителем метанола является производство формальдегида (в первую очередь, его водного раствора - формалина), который получают окислительной конверсией метанола. На долю формальдегида приходится половина производимого метанола.
Потребителями метанола являются производства различных мономеров (например, метилметакрилата и диметилтерефталата), метилтретбутилового эфира (МТБЭ), метилгалогенидов, метиламинов, ионообменных смол, уксусной кислоты. Метанол также широко используется как растворитель и экстрагент.
Одной из новых областей применения метанола является использование его в качестве моторного топлива взамен ставшего дефицитным и весьма дорогим бензина.

Метанол либо добавляют к бензину в количестве до 5%, либо используют целиком вместо бензина. Однако метанол обладает более низкой теплотворной способностью и является весьма токсичным, что, вероятно, будет сдерживать его применение.
Метанол – ядовитая бесцветная жидкость со сладковатым запахом.
Метанол в числе других кислородсодержащих соединений впервые был получен из оксида углерода и водорода в 1913 г. Для этой цели использовали железные катализаторы, которые однако быстро покрывались углеродом и дезактивировались. Применение цинк-хромовых катализаторов позволило устранить этот недостаток. Было установлено, что оксид цинка не чувствителен к сере, соединения которой обычно содержатся в синтез-газе и отравляют металлические катализаторы.
Реакция образования метанола идет с выделением тепла и уменьшением объема, поэтому ей благоприятствуют низкие температуры и высокие давления. При синтезе метанола протекают следующие реакции:
СO+2H2 → CH3OH –ΔН25= 110,8 кДж/моль (1)
СO+H2O → CO2+H2 –ΔН25= 41 кДж/моль (2)
CO2+3H2 → CH3OH+H2O –ΔН25= 60,4 кДж/моль (3)
С повышением температуры степень превращения СО заметно снижается.
Условия проведения реакции определяются катализатором. Если катализатор обладает такой высокой активностью, что уже при низкой температуре достигается высокая степень превращения СО, то синтез метанола можно осуществлять уже при давлении 5 МПа. В противном случае, то есть при применении менее активного катализатора, работающего при более высокой температуре, необходимо давление ~30 МПа. Катализаторы, обычно применяемые в промышленности, проявляют активность только при высоких температурах (360-380оС), т.е. в условиях термодинамически неблагоприятных. В промышленности наибольшее распространение получили цинк-хромовые катализаторы, а в последние годы – медьсодержащие катализаторы, достаточно активные при температуре 220-270оС.
При управлении селективностью синтеза метанола необходимо учитывать, что протекание этой реакции гораздо менее термически благоприятно, чем протекание таких побочных реакций, как образование углеводородов, высших спиртов, диметилового эфира. Эти реакции можно подавить варьированием состава катализатора.
В зависимости от применяемых катализаторов (а, следовательно, условий синтеза) различают два варианта превращения синтез-газа в метанол: синтезы при высоком и низком давлении.
При высоком давлении применяют катализаторы на основе оксида цинка, характеризующиеся низкой чувствительностью к сере, промотированные оксидами хрома (межкристаллический промотор – располагающийся вне кристаллической решетки ZnO) или оксидами железа, кальция, магния (внутрикристаллические промоторы – располагающиеся внутри кристаллической решетки ZnO).
Реакторы высокого давления представляют собой цельнокованные аппараты колонного типа, для эффективного теплоотвода используют реакторы полочного типа с промежуточным вводом холодного газа и выносным или встроенным теплообменником. Обычное число полок 5-6, для пуска агрегата применяют встроенный электронагреватель или специальную трубчатую печь.
Наиболее эффективными каталитическими системами, работающими при низком давлении, являются медьсодержащие оксидные катализаторы. Однако медьсодержащие катализаторы отличаются высокой чувствительностью к примесям сернистых соединений, почти всегда содержащимся в синтез-газе. Если при синтезе на цинк-хромовых катализаторах допустимо содержание сероводорода в синтез-газе выше 100 ррm, то для медных катализаторов этот показатель не может превышать 1 ppm.
При низком давлении используют полочные реакторы, аналогичные тем, что применяются при высоком давлении, или реакторы трубчатого типа, в которых катализатор загружен в трубки, а тепло реакции отводится кипящей водой, циркулирующей в межтрубном пространстве реактора и связанной с паросборником, так как при съеме тепла генерируется водяной пар. При использовании трубчатого реактора не требуется пусковой нагреватель, реактор в пусковой период разогревается водяным паром из сети, что является преимуществом реактора этого типа. В то же время достоинством полочного реактора является простота конструкции и легкость загрузки и выгрузки катализатора.
Природный газ отделяют от тяжелых углеводородов и компримируют в турбокомпрессоре 1 до 2,5 МПа, после чего направляют на очистку и далее в блок конверсии метана 3. Туда же поступает водяной пар. К метану добавляют небольшое количество СО2. Конверсия метана осуществляется при температуре 850—860 °С. После печей конверсии синтез-газ поступает в котел-утилизатор 4, где генерируется пар высокого давления (12 МПа), который затем перегревается и поступает на турбины — привод компрессоров 1 и 11. Если конверсии подвергают тяжелое жидкое сырье, то блок очистки располагается после конверсии, а необходимость в компрессоре 1 отпадает. В последнем случае конверсию проводят при давлении 5,8 МПа, а синтез-газ после очистки не нуждается в дополнительной компрессии и поступает в циркуляционный компрессор 11.
Синтез-газ, полученный из природного газа, направляют на доохлаждение с целью конденсации воды. Далее синтез-газ дожимается в турбокомпрессоре 12 до 5—5,5 МПа, смешивается с циркуляционным газом и через теплообменник 6, обогреваемый горячим реакционным газом, поступает в два параллельно работающих реактора синтеза метанола 7.
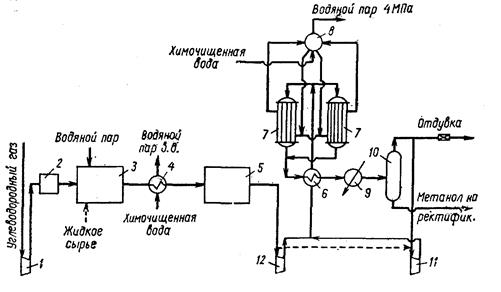
Технологическая схема синтеза метанола под низким давлением:
1,11,12— компрессоры; 2 — блок очистки; 3-блок конверсии метана; 4 - котел-утилизатор; 5 — блок очистки и доохлаждення синтез-газа; 6- теплообменник; 7 — реакторы синтеза метанола; 8—паросборник; 9 - холодильник; 10— газосепаратор в. д.
Реакторы трубчатого типа охлаждаются циркулирующей в межтрубном пространстве водой. Пар направляется в паросборник 8 , куда подается и химически очищенная вода. Конденсат из паросборника вновь поступает в реакторы 7, а водяной пар высокого давления направляется на перегрев и используется в турбинах. Продукты реакции направляются через теплообменник 6 , где отдают свое тепло синтез-газу, в конденсатор-холодильник 9 и в газосепаратор 10 для отделения метанола от циркуляционного газа. Последний поступает на прием циркуляционного компрессора 11 и вновь направляется в систему синтеза. Часть газа отдувают для удаления поступающих в систему инертных примесей (главным образом метана и азота). Метанол-сырец из газосепаратора 10 направляется на ректификацию.
Дата добавления: 2015-04-15; просмотров: 4849;
