Измерение электропроводности слабого электролита
Измеряют электропроводности растворов уксусной кислоты (или другой, предложенной преподавателем) следующих концентраций: 0,001 н, 0,01 н, 0,1 н, 1 н.
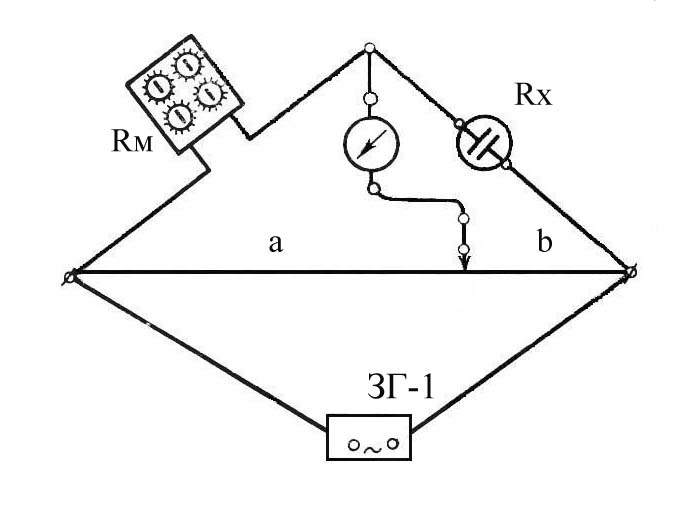
Начинают измерения в растворе меньшей концентрации. Электроды и сосуд перед началом измерений необходимо ополоснуть сначала дистиллированной водой, а затем определяемым раствором. Объем кислоты в сосуде должен быть таким же, каким был объем раствора хлорида калия.
Зная сопротивление раствора и постоянную сосуда - С0, находят удельную электропроводность данного раствора по формуле:
æ х = 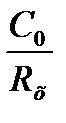 , [Ом-1 . см-1 ].
, [Ом-1 . см-1 ].
По формуле 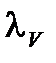 = æ ×
= æ × 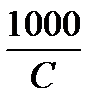 находят эквивалентную электропроводность. Затем по таблицам определяют
находят эквивалентную электропроводность. Затем по таблицам определяют 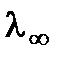 , как сумму подвижностей катиона и аниона.
, как сумму подвижностей катиона и аниона.
По формуле 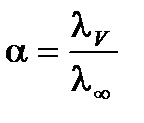 определяют степень электролитической диссоциации.
определяют степень электролитической диссоциации.
Рассчитать значение 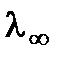 , как сумму подвижностей катиона и аниона, взяв значения из таблицы в лаборатории.
, как сумму подвижностей катиона и аниона, взяв значения из таблицы в лаборатории.
По формулам 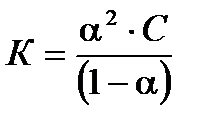 или
или 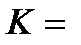
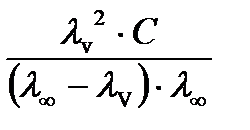
проверяют закон разведения Оствальда.
Таблица 2
Экспериментальные и расчетные данные
| № | Конц. раствора | Rм | Плечи реохорда | Rх | æ | 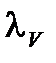
| a | К | |
| а | б | ||||||||
| 0,001 н | 1) 2) 3) | ||||||||
| Rх ср | |||||||||
| 0,01 | 1) 2) 3) | ||||||||
| Rх ср | |||||||||
| 0.1 | 1) 2) 3) | ||||||||
| Rх ср | |||||||||
| 1) 2) 3) | |||||||||
| Rх ср |
1. Теория электролитической диссоциации С. Аррениуса. Закон разведения Оствальда, его физический смысл.
2. Электропроводность слабых электролитов, удельная и эквивалентная, зависимость их от концентрации и температуры.
3. Экспериментальные методы определения электропроводности электролитов (схема установки, электроды, ток). Постоянная сосуда, физический смысл и метод определения.
4. Определение электропроводности при бесконечном разведении для слабых электролитов. Формула Кольрауша.
5. От чего зависят удельная и эквивалентная электропроводности сильных электролитов? Подвижности ионов и закон Кольрауша.
Зависимость подвижностей и электропроводности от концентрации в рамках теории Дебая-Гюккеля-Онзагера. Физический смысл электрофоретического и релаксационного эффектов. Эффекты Вина и Дебая-Фалькенгагена.
6. Способы определения электропроводности при бесконечном разведении для слабых и сильных электролитов.
Вопросы
1. Теория электролитической диссоциации. Закон разведения Оствальда, физический смысл. Электропроводность электролитов - эквивалентная и удельная. Зависимость удельной электропроводности от концентрации для слабых и сильных электролитов. Формула Кольрауша для эквивалентной электропроводности при бесконечном разведении.
2. Скорость движения ионов, абсолютная скорость, подвижность. Аномальная подвижность ионов гидроксония и гидроксила в водных растворах, причины.
Работа № 20
Дата добавления: 2015-02-16; просмотров: 2648;
