Законы термодинамики
Термодинамика – это наука о законах превращения тепловой энергии. Тепловая энергия или тепло – это энергия, которая передается от одного тела к другому при их контакте (теплопередача). Тепло можно превратить в механическую работу и, наоборот, механическую работу можно превратить в тепло. Все эти процессы изучает термодинамика. Термодинамика основывается на общих принципах природы и не рассматривает строение вещества изучаемой системы. Поэтому выводы термодинамики имеют общий характер и не зависят от деталей строения системы.
В термодинамике рассматривается три типа систем.
Изолированные системы, которые не обмениваются с внешней средой ни энергией, ни веществом.
Закрытые системы, которые обмениваются с внешней средой энергией, но не обмениваются веществом.
Открытые системы, которые обмениваются с внешней средой и энергией, и веществом3.
Опыт показывает, что если два тела, имеющие разные температуры, привести в соприкосновение, то через некоторое время температуры этих тел выравниваются и больше не изменяются. Говорят, что система достигла термодинамического равновесия. Равновесное состояние системы характеризуется тем, что все термодинамические параметры (температура, давление, химический потенциал и др.) одинаковы в любой точке системы и самопроизвольно не изменяются со временем.
Всякое изменение термодинамических параметров системы называется термодинамическим процессом. В природе существует два вида термодинамических процессов – обратимые и необратимые. Если система переходит из одного состояния А в другое состояние В таким образом, что существует хотя бы один способ вернуть систему обратно, не производя при этом каких-либо изменений в окружающих телах, то такой процесс называется обратимым. Если этого сделать не удается, то процесс необратим. Обратимые процессы являются равновесными, т. е. состоят из последовательности равновесных состояний.
Современная термодинамика делится на два больших раздела: равновесная термодинамика закрытых и открытых систем и неравновесная термодинамика открытых систем. Равновесная термодинамика основывается на трех основных законах или началах.
Первое начало термодинамикиявляется, по существу, законом сохранения энергии для термодинамических процессов. Мы уже знаем, что молекулярная система обладает кинетической энергией движения молекул и потенциальной энергией взаимодействия молекул друг с другом. Сумма этих энергий составляет внутреннюю энергию системы 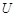 .
.
Система при определенных условиях может совершать работу А. Например, газ под поршнем может расширяться и перемещать поршень, а вместе с ним и груз, прикрепленный к поршню. Механическая работа, произведенная силой 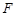 , действующей на какое-либо перемещающееся тело, определяется формулой
, действующей на какое-либо перемещающееся тело, определяется формулой 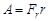 . Здесь
. Здесь 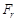 – проекция силы
– проекция силы 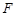 на направление перемещения,
на направление перемещения, 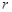 – величина перемещения (путь, пройденный телом). Если эту формулу применить к поршню, который перемещается под действием сил давления, то получим
– величина перемещения (путь, пройденный телом). Если эту формулу применить к поршню, который перемещается под действием сил давления, то получим 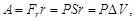 где
где 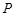 – давление газа,
– давление газа,  – изменение объема газа. Работа имеет размерность энергии (Дж) и определяется энергией, которую затрачивает газ на ее производство.
– изменение объема газа. Работа имеет размерность энергии (Дж) и определяется энергией, которую затрачивает газ на ее производство.
В молекулярную систему можно передать количество теплоты 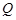 путем теплопередачи. Это тоже энергия, переданная системе извне. Эта энергия может пойти на увеличение внутренней энергии системы или на совершение системой механической работы. Таким образом, получаем
путем теплопередачи. Это тоже энергия, переданная системе извне. Эта энергия может пойти на увеличение внутренней энергии системы или на совершение системой механической работы. Таким образом, получаем
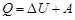 .
.
Здесь 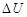 – изменение внутренней энергии системы. Эта формула выражает первое начало термодинамики. Ее можно рассматривать и в обратном порядке. Совершая работу над системой (например, опуская поршень в цилиндре с газом), можно получить тепло или увеличить внутреннюю энергию системы (нагреть газ). Таким образом, первое начало термодинамики говорит о том, что система может совершить работы ровно столько, сколько энергии в нем содержится и сколько тепла ему передано.
– изменение внутренней энергии системы. Эта формула выражает первое начало термодинамики. Ее можно рассматривать и в обратном порядке. Совершая работу над системой (например, опуская поршень в цилиндре с газом), можно получить тепло или увеличить внутреннюю энергию системы (нагреть газ). Таким образом, первое начало термодинамики говорит о том, что система может совершить работы ровно столько, сколько энергии в нем содержится и сколько тепла ему передано.
Первое начало термодинамики запрещает создание так называемого вечного двигателя первого рода. Вечный двигатель первого рода – это такая фантастическая машина, которая может совершать работу без внешнего источника энергии. Проекты такого двигателя часто предлагались начиная с XIII в. и иногда предлагаются и сегодня. Простейшие проекты основаны на циклическом движении какого-либо массивного тела (например, тело опускается с высоты и затем поднимается обратно за счет собственной инерции), при этом оно совершает работу (поднимает грузы). Предлагались также проекты с использованием жидкостей и газов. Естественно, что все эти двигатели не работали. Пока не был известен закон сохранения энергии, были не понятны и причины такого неуспеха. Казалось, что достаточно придумать удачную конструкцию двигателя и можно обеспечить себя бесплатной рабочей силой. Тем не менее еще в 1775 г. Парижская академия наук отказалась рассматривать проекты вечного двигателя. Лишь в середине XIX в. с открытием закона сохранения энергии стали понятны причины принципиальной невозможности создания вечного двигателя первого рода. В связи с этим первое начало термодинамики можно сформулировать так: вечный двигатель первого рода невозможен.
Второе начало термодинамики.Ограничения, накладываемые первым началом на термодинамические процессы, не являются единственными. Можно представить процессы, которые не запрещены первым началом термодинамики, но никогда не происходят в природе. Например, вообразим себе следующий процесс: ставим чайник с водой на лед, через некоторое время вода в чайнике закипает, а лед еще сильнее остывает. Ясно, что это невозможно, но тем не менее первое начало термодинамики выполняется. Энергия, которую содержит лед, перетекает в чайник и нагревает его, а сам лед при этом теряет энергию и остывает. Мы можем сформулировать правило, которое запрещает такие процессы: тепло перетекает от более нагретого тела к менее нагретому. Это – одна из формулировок второго начала термодинамики.
Еще один пример. Представим себе двигатель, который черпает энергию из окружающей среды и полностью превращает ее в работу. При этом энергия окружающей среды немного понижается. Такой двигатель называется вечным двигателем второго рода. Например, такой двигатель находится на корабле. Он берет энергию из океана и превращает ее в работу гребных винтов. Такой корабль мог бы плавать вечно без заправки топливом. Единственным изменением в окружающей среде, возможно, было бы некоторое, очень малое остывание океана. Оказывается, такой двигатель построить нельзя. Если бы это было возможным, то, получив энергию от холодного тела, можно было бы превратить ее в работу (например, в движение какого-либо другого тела). Это тело можно поместить на поверхность третьего более нагретого по сравнению с первым тело. В результате трения второго и третьего тел они будут нагреваться. Единственным результатом действия такого двигателя будет передача тепла от менее нагретого тела к более нагретому, т. е. можно сделать чайник, который закипает за счет энергии льда. Таким образом, еще одной формулировкой второго начала термодинамики может служить утверждение о невозможности создания вечного двигателя второго рода.
Чтобы выразить второе начало математически, вводится новая термодинамическая переменная, которая является функцией состояния системы, т. е. функцией термодинамических переменных 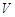 и
и 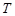 . Она обозначается
. Она обозначается 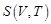 и называется энтропией. Изменение энтропии системы определяется соотношением
и называется энтропией. Изменение энтропии системы определяется соотношением 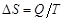 (
( 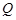 – количество теплоты, переданной системе при температуре системы
– количество теплоты, переданной системе при температуре системы 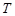 ). Рассчитаем изменение энтропии при теплообмене между двумя телами:
). Рассчитаем изменение энтропии при теплообмене между двумя телами: 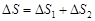 ,
, 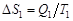 ,
, 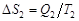 . Здесь
. Здесь 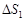 и
и 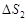 – изменение энтропий первого и второго тел;
– изменение энтропий первого и второго тел; 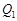 и
и 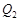 – теплоты, получаемые первым и вторым телами в процессе теплообмена;
– теплоты, получаемые первым и вторым телами в процессе теплообмена; 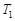 и
и 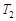 – температуры первого и второго тел. В соответствии с первым началом термодинамики
– температуры первого и второго тел. В соответствии с первым началом термодинамики 
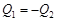 , так как полная энергия системы сохраняется. Отсюда,
, так как полная энергия системы сохраняется. Отсюда, 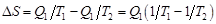 . Пусть
. Пусть 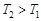 . Тогда тепло передается от второго тела к первому и
. Тогда тепло передается от второго тела к первому и 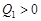 . Поскольку в этом случае
. Поскольку в этом случае 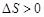 , энтропия системы в целом возрастает. Если бы тепло могло переходить от менее нагретого тела к более нагретому, то энтропия убывала бы. В равновесии энтропия достигает своего максимума, возможного в системе при данных условиях, и не изменяется со временем. Таким образом, второе начало термодинамики можно сформулировать следующим образом: энтропия изолированной системы может только возрастать, достигая максимума в равновесном термодинамическом состоянии.
, энтропия системы в целом возрастает. Если бы тепло могло переходить от менее нагретого тела к более нагретому, то энтропия убывала бы. В равновесии энтропия достигает своего максимума, возможного в системе при данных условиях, и не изменяется со временем. Таким образом, второе начало термодинамики можно сформулировать следующим образом: энтропия изолированной системы может только возрастать, достигая максимума в равновесном термодинамическом состоянии.
Дата добавления: 2015-01-15; просмотров: 3789;
