I Закон термодинамики для потока газа .
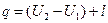
Несколько изменим схему, покажем, что поступающее и выталкиваемое рабочее тело находится под давленирем
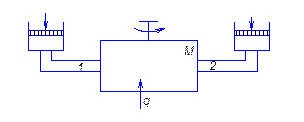
Внутренняя энергия газа во впускном трубопроводе 1 – U1.
Внутренняя энергия газа в выпускном трубопроводе 2 – U2 полностью p;T;V.
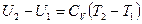 - для идеального газа.
- для идеального газа.
Работа деформации раскладывается на составляющие:
а) Внешне полезная;
б) располагаемая;
в) техническая работа.
Внешне полезной lп называется та часть от общей работы которая идет например на вращение вала или другую рабочую операцию.
Располагаемая - часть работы, которая расходуется на увеличение кинетической энергии рабочего тела, lр, т.к. ее можно превратить в работу (например использовав турбину и т.д.).
Если в поршневых и турбинных двигателях главный результат lп , то в реактивных двигателях главный результат – lр. Эта располагаемая работа реализуется в процессе полета ракет или летательных аппаратов.
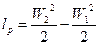
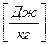
Сумма внешне полезной и располагаемой работ называется технической работой.
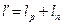
Работа вытеснения.
Проходя через машину газ совершает работу. При поступлении совершается работа вталкивания, т.к. давление в 1 постоянно, то величину работы можно посчитать:
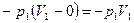 - она отрицательна, т.к. она совершается над рабочим телом.
- она отрицательна, т.к. она совершается над рабочим телом.
При выходе из машины совершается работа выталкивания:
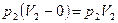
Их алгебраическая сумма – работа вытеснения.
Вся работа деформации l состоит из:
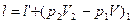
Изображение технической работы в диаграмме P-V.
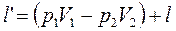
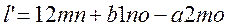
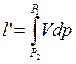
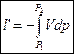
Рассмотрим соотношение между l и l’:
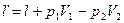
Для внешней работы в политропном процессе:
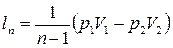
Подставим S :
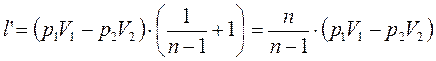
Сравним l и l’:
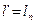
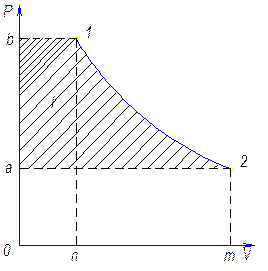
Уравнение I-го закона термодинамики для
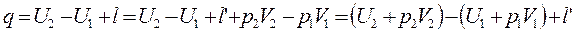
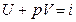 - энтальпия или полная энергия 1 кг. газа.
- энтальпия или полная энергия 1 кг. газа.
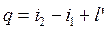
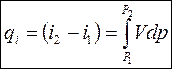
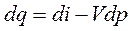
В любом термодинамическом процессе подводимое к потоку газа тепло, расходуется на совершение технической работы и увеличение энтальпии.
Энтальпия (i) – внутреннее тепло, один из параметров вещества.
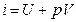 где U – кинетическая энергия молекул газа,
где U – кинетическая энергия молекул газа,
PV – потенциальная энергия давления, т.к. 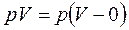
Пользуются разностью энтальпий. Из уравнения для потока напишем:
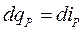
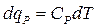
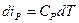 - при
- при 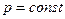
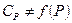 - для идеального газа
- для идеального газа
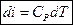
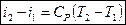
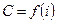
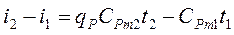
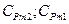 - средние теплоемкости газа, от О, t1 и t2
- средние теплоемкости газа, от О, t1 и t2
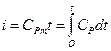
За О принимается энтальпия при 0°С.
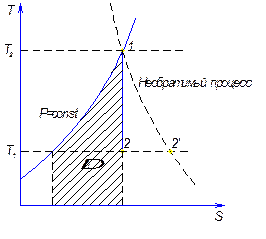
Изменение энтальпии можно показать … в энтропийной диаграмме Т-S.
Пример: Определить изменение энтальпии воздуха при его изобарном охлаждении от 300° до 10°С.
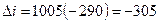
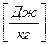
II-й закон термодинамики.
I-й закон не касается условий, при которых возможен переход тепла в работу. Опыт показывает, что если ТА > ТВ , то тепло идет только от А к В, причем при ТА = ТВ теплообмен прекращается. Исходя из I-го закона термодинамики не понятно, почему в тепловых двигателях все подведенное тепло не превращается в работу (h < 1), тогда, как известно, что работа превращается в тепло на 100%.
Все эти взаимные превращения и рассматриваются II-м законом термодинамики, он ограничивает действие I-го закона.
1) Установление условий превращения тепла в работу.
2) Установление степеней совершенства этого превращения.
Формулировка II-го закона термодинамики.
Формулировка Карно (для тепловых двигателей):
Всюду, где имеется разность Т°, возможно возникновение работы.
Т.е. тепло не может всё превращаться в работу, часть тепла переходит к источнику с низкой Т°.
Формулировка Оствольда:
Осуществление вечного двигателя II-го рода (h=100%) невозможно.
Формулировка …:
Тепло не может переходить само собой от тела более холодного к более нагретому.
Т.е. для этого перехода необходимо затратить работу(например в холодильных машинах).
Формулировка Ломоносова:
Холодное тело В, погруженное в тело А не может воспринять большую степень, чем имеет А.
Дата добавления: 2015-02-28; просмотров: 3031;
