Исследование газовых процессов.
Изохорный, изобарный, изотермический, адиабатный, политропный.
В каждом процессе один из параметров состояния постоянный (const).
1. Изохорный процесс:
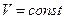 ;
; 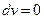 Уравнение состояния идеального газа для 1 и 2 го состояний:
Уравнение состояния идеального газа для 1 и 2 го состояний:
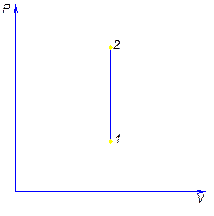
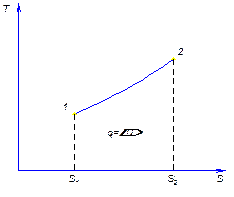
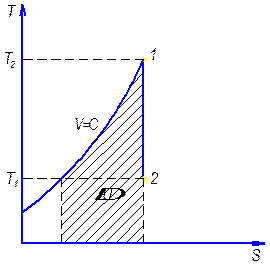
Рис. Изохора
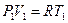
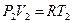 поделим
поделим
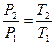
Работа при неизменяемом объёме равна нулю 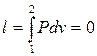
При этом все тепло идет на изменение внутренней энергии 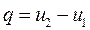
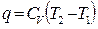 .
.
Из уравнения (1) при постоянном объеме изменение энтропии может
быть вычислено 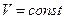 :
: 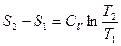
2. Изобарный процесс: 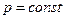
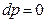 Для двух состояний идеального газа:
Для двух состояний идеального газа:
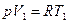
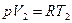
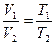
Работа при изобарном процессе:
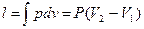
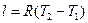
При приращении температуры на 1 градус 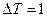 работа равна газовой постоянной:
работа равна газовой постоянной:
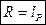
По физическому смыслу газовая постоянная R есть работа расширения газа в обратимом процессе при постоянном давлении 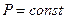 и при нагревании газа на 1°
и при нагревании газа на 1°
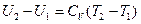
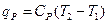
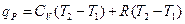
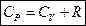 - уравнение Майера
- уравнение Майера
Из уравнения (1) и соотношения (2):

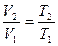
 Следует, что энтропия в изобарном процессе может быть вычислена:
Следует, что энтропия в изобарном процессе может быть вычислена:
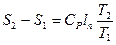
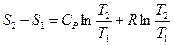

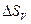 <
< 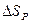 т.к.
т.к. 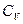 <
< 
При этом в координатах t-s изохора проходит круче изобары (см. рис.) .
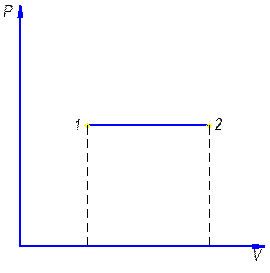
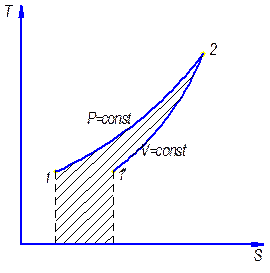
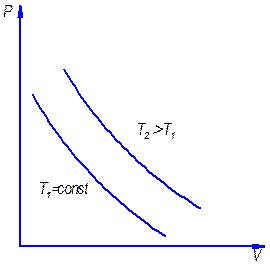
3. Изотермический процесс:
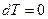
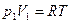
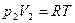
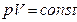
Равнобочная гипербола (снова строчные символы)
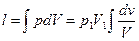
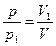
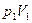 - для 1 процесса
- для 1 процесса 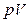 - текущее значение
- текущее значение
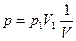
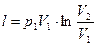
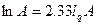
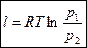
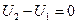
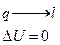
Изменение энтропии
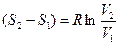
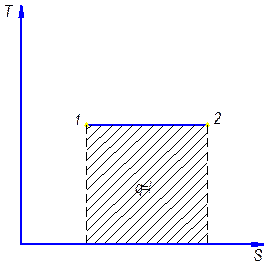
4. Адиабатный процесс: - без теплообмена c внешней средой
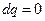
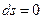
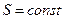
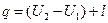
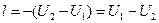
Работа расширения за счет изменения внутренней энергии
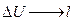
Используя (1) выведем уравнение адиабаты в 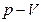
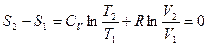
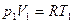
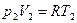
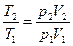
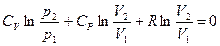
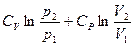
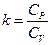
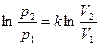
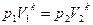
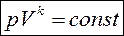
k – показатель адиабаты
Неравнобочная гипербола
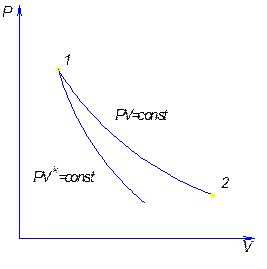
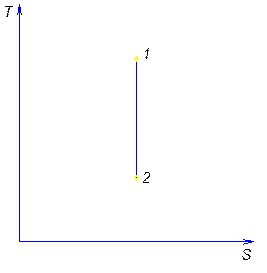
Соотношения между параметрами состояния и работой газа в адиабатном процессе.
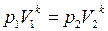
p иV
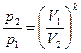 (1)
(1)
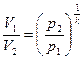 (2)
(2)
T иV
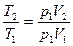 (3)
(3)
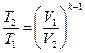 (4) – из (1) и (3)
(4) – из (1) и (3)
T и p
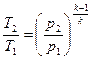 (5) – из (2) и (3)
(5) – из (2) и (3)
Изменение внутренней энергии газа:
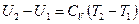 (6)
(6)
Работа газа:
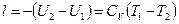 (7)
(7)
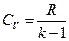 подставляем в (7)
подставляем в (7)
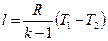
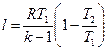 - подставим (4)
- подставим (4)
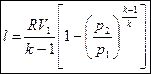
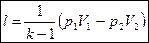
Пример: Воздух адиабатно расширяется от 780° до 200° С. Определить DU; l. Показать график процесса DU в диаграмме T-S.
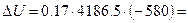 или
или 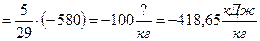
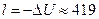
Дата добавления: 2015-02-28; просмотров: 1515;
