Химическая реакция как лимитирующая стадия процесса.
 | |||
 | |||






 С
С
СГН=
СГЗ=




 СГЯ
СГЯ

0 R r 0 r R
Рисунок 20. Профиль концентраций газа при условии отсутствия диффузии газа через слой продуктов реакции и через пограничный слой.
Поскольку течение реакции не зависит от наличия слоя золы, количественное реагирование вещества пропорционально активной поверхности невзаимодействующего ядра. Отсюда, скорость реакции, отнесенная к единице поверхности ядра частицы:
 (91)
(91)
Заменив, как и в предыдущих случаях скорость расходования реагента dNГ/dtна скорость продвижения границы ядра dr/dt, получаем
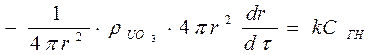 (92)
(92)
Откуда
 (93)
(93)
С учетом зависимости (76) уравнение (93) принимает вид
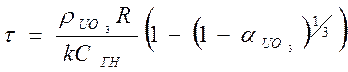 (94)
(94)
При a=1 получим время полного превращения tП твердой частицы, имеющей радиус R, при протекании гетерогенного процесса в кинетической области:
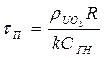 (95)
(95)
Итак, для кинетической области гетерогенного взаимодействия
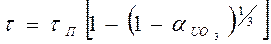 (96)
(96)
Так как k – константа скорости химической реакции зависит в основном от температуры, то наиболее целесообразным способом управления гетерогенным процессом, лимитируемым химической реакцией, является именно изменение температуры.
Дата добавления: 2014-12-26; просмотров: 1532;
