Реакции замещения. По способности вступления в реакции электрофильного замещения пиррол напоминает фенол и анилин
По способности вступления в реакции электрофильного замещения пиррол напоминает фенол и анилин. Атомы углерода в пирроле α-электроноизбыточны. Если в бензоле на каждый атом кольца приходится один электрон, то в случае пиррола - больше, причем, электронная плотность распределена неравномерно. В пирроле наибольшая электронная плотность приходится на 2 – и 5-положения кольца.
Однако такая электроноизбыточность не объясняет предпочтительности α-положения пиррола в реакциях электрофильного замещения. В этих реакциях более существенную роль играет, по-видимому, то обстоятельство, что при α-атаке образуется более стабильный σ-комплекс,
чем при β-атаке. Действительно, в карбокатионе, образующемся при атаке в α-положение, в делокализации заряда участвуют три канонические структуры, а в альтернативном случае – только две структуры
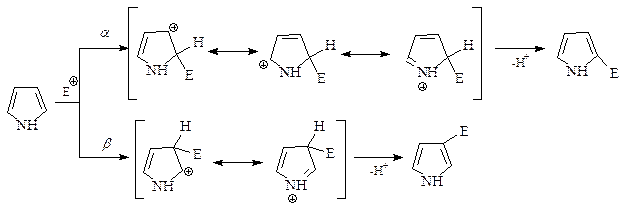
Рассмотрим конкретные реакции электрофильного замещения с участием пиррола.
Галогенирование. Пиррол галогенируется так же легко, как и фенол. Если не предпринимать мер предосторожности, галогенирование идет во все положения фуранового кольца. Моногалогенпирролы удается получить лишь в особо мягких условиях
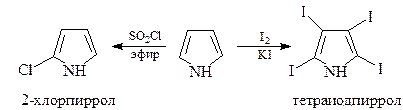
Тетраиодпиррол используется как антисептик (иодол).
Нитрование. При нитровании пиррола ацетилнитратом при относительно низкой температуре (5оС) в продуктах реакции нитрогруппа занимает α-положение (выход около 7%)
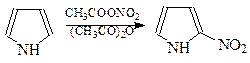
Известно, что реакционная способность каждого из α-и β-углеродов пиррола в рассматриваемой реакции выше, чем у бензола более чем в 1000 раз.
Сульфирование. Вследствие ацидофобности пиррола сульфировать его серной кислотой не представляется возможным. Чтобы обойти это затруднение, применяют уже знакомый пиридинсульфотриоксид. Как и в случае других реакций электрофильного замещения, сульфирование пиррола идет с участием α-положений кольца

Алкилирование. Как и в случае фурана, прямое алкилирование пиррола протекает неоднозначно и сопровождается полимеризацией. Поэтому с целью введения алкильного радикала в пиррольное ядро, прибегают к косвенному приему. Сперва получают металлическое производное этого гетероцикла, затем реакцией с галогеналкилами проводят N- и С-алкилирование. При температурах реакции ниже 0оС происходит N-алкилирование, а продукты С-алкилирования обычно получают восстановлением продуктов их ацилирования
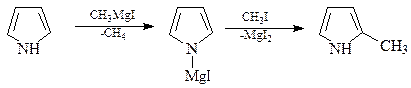
Ацилирование. Остаток карбоновой кислоты во 2-положение пиррольного кольца можно ввести при помощи реакции гетероцикла с ангидридами кислот. Так, пиррол реагирует с уксусным ангидридом при 150оС даже без катализатора

При формилировании пиррола используется реакция Вильсмайера-Хаака. В этой реакции в качестве ацилирующего средства применяют диметилформамид в присутствии фосфорилхлорида

Наконец, следует отметить, что реакционная способность пиррола позволяет реагировать ему даже с солями диазония

Дата добавления: 2014-12-24; просмотров: 3180;
