Визуализационные методы диагностики
Ультразвуковое исследование (УЗИ) и компьютерная томография (КТ) позволяют выявить в поджелудочной железе объёмное образование диаметром до 2 см, а также расширение жёлчных протоков и протока поджелудочной железы, метастазы в печень и внепеченочное распространение первичной опухоли. Хотя УЗИ более доступно и его стоимость меньше, проведение исследования может бы гь затруднено из-за усиленного газообразования в кишечнике. Часто КТ более предпочтительна (см. рис. 29-5), а современные модификации её — спиральная КТ и динамическая КТ с высоким разрешением — позволяют установить диагноз более чем в 95% случаев |14|. В настоящее время не выявлено каких-либо преимуществ магнитно-резонансной томографии.
Прицельная пункционная биопсия объёмного образования поджелудочной железы под контролем УЗИ или КТ безопасна и позволяет установить диагноз у 57—96% больных |30, 44). Риск метастазирования опухоли по пункционному каналу невелик |33|.
Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) обычно позволяет визуализировать проток поджелудочной железы и жёлчные протоки, выполнить биопсию ампулы (рис. 33-2), получить жёлчь или сок поджелудочной железы, выполнить щёточную биопсию места стриктуры для цитологического исследования (рис. 33-3) |20].
Выявление стриктуры жёлчных или панкреатических протоков даёт веские основания подозревать её злокачественную природу (см. рис. 29-11, а), но иногда результаты ЭРХПГ могут быть ошибочными, и тогда для установления диагноза необходимо морфологическое исследование. Особенно важно выявить нетипичные опухоли, например лимфому, поскольку они поддаются традиционным методам лечения.
У больных, у которых отмечается рвота, исследование с барием позволяет оценить степень инвазии и обструкции двенадцатиперстной кишки.
Определение стадии опухоли
Определение стадии опухоли важно для оценки её резектабельности. Несомненные признаки метастазирования можно выявить при клиническом обследовании, рентгенографии грудной клетки, КТ или УЗИ. Неоперабельность опухоли можно установить при динамической КТ с контрастированием, но с уверенностью судить о резектабельности по результатам этого исследования невозможно [14, 15]. Динамическая КТ может выявить прорастание в сосуды, но менее пригодна для оценки инвазии подлежащих тканей и местных или отдалённых метастазов. Ангиография столь же эффективна для определения резектабельности опухоли, как и динамическая КТ; при этом окклюзия крупных сосудов, особенно плотное облегание их опухолью, служит противопоказанием к операции [13]. Хотя в некоторых специализированных центрах необходимость в ангиографии в связи с широким применением КТ уменьшилась, во многих случаях её применение перед операцией целесообразно для уточнения анатомии сосудов, так как различные аномалии их встречаются примерно у трети оперируемых больных.
Лапароскопия позволяет выявить мелкие метастазы в печень, а также обсеменение брюшины и сальника и выполнить биопсию. Если метастазы не выявлены при лапароскопии, КТ и ангиографии, благоприятный исход операции возможен у 78% больных [46].
Портография с КТ также позволяет выявлять метастазы в печень, но малоэффективна для оценки местных изменений, вызванных самой опухолью поджелудочной железы.
Эндоскопическое УЗИ предложено недавно. Оно позволяет с помощью эндоскопа с ультразвуковым датчиком на конце визуализировать через стенку желудка и двенадцатиперстной кишки поджелудочную железу и окружающие её ткани. В опытных руках точность оценки стадии опухоли (Т) достигает 85%, выявления инвазии сосудов — 87%, поражения регионарных лимфатических узлов (N) — 74%
[35]. Опыт применения этого метода пока невелик. Результаты исследования в значительной степени зависят от квалификации врача, а само оно требует больших затрат времени, поэтому метод не вошел в повседневную клиническую практику.
Прогноз
Прогноз при раке поджелудочной железы неблагоприятный. После наложения билиодигестивного анастомоза средняя выживаемость составляет около 6 мес. Прогноз при ацинарноклеточном раке хуже, чем при протоковом, поскольку регионарные лимфатические узлы поражаются раньше. Опухоль резектабельна лишь у 5—20% больных.
Летальность после радикальной операции составляет 15—20% [17], но в последнее время в специализированных центрах, где производится гораздо больше операций и хирурги обладают большим опытом, её удалось снизить до 5% [44]. В недавнем сообщении из одного специализированного центра после 145 панкреатодуоденальных резекций летальных исходов не было. Однако это исключительный случай [8].
Параллельно снижению послеоперационной летальности пятилетняя выживаемость повысилась до 20% [6]. Возможно, это отражает более раннюю диагностику благодаря применению современных визуализационных методов исследования либо является следствием отбора для операции больных с менее распространённым поражением. Однако по-прежнему не решена проблема борьбы с рецидивами опухоли. Тотальная панкреатэктомия не позволяет достичь большей продолжительности жизни по сравнению с меньшей по объёму панкреатодуоденальной резекцией по Уипплу и вызывает недостаточность экзокринной функции железы и тяжёлый диабет [4].
В целом перспективы при раке поджелудочной железы неблагоприятные: в одном исследовании из 912 больных через 3 года были живы 23 и только 2 больных можно было считать излеченными [10].
Прогноз при раке ампулы более благоприятен, пятилетняя выживаемость после радикальной операции при опухоли, не распространяющейся за пределы сфинктера Одди, составила 85%, а при более выраженной инвазии — 11—25%. Методом выбора является панкреатодуоденальная резекция. В некоторых случаях можно выполнить локальное иссечение опухоли [3].
Лечение
Панкреатодуоденальная резекция
Решение о выполнении панкреатодуоденальной резекции принимают исходя из результатов клинического обследования больного и визуализационных методов исследования, позволяющих установить стадию рака. Операцию усложняет ограниченный доступ к поджелудочной железе, которая расположена на задней стенке брюшной полости вблизи oi жизненно важных органов. Лишь небольшая часть больных оказываются операбельными.
Классическим вариантом панкреатодуоденальной резекции является операция Уиппла, которую производят одномоментно, удаляя решонарные лимфатические узлы, всю двенадцатиперстную кишку и дистальную треть желудка. В 1978 г. эту операцию модифицировали |42|, чтобы сохранить функцию привратника и антрального отдела желудка (пилоросохраняющая панкреатодуоденальная резекция). Благодаря этому уменьшаются клинические проявления постгастрорезекционного синдрома и частота образования язв, а также улучшается пишеварение |23|. Выживаемосгь не отличается oт таковой после классической операции. Для восстановления пассажа жёлчи общий жёлчный проток анастомозируют с тощей кишкой. Проток оставшейся части поджелудочной железы также анастомозируют с тощей кишкой. Проходимость кишечника восстанавливают путём дуоденоеюностомии.
Обязательно следует проводить исследование замороженных срезов краёв резецированных органов.
Прогноз определяется размерами опухоли, гистологически выявляемой инвазией кровеносных сосудов и состоянием лимфатических узлов. Наиболее важна гистологическая картина при исследовании лимфатических узлов. Если в них нет метастазов, пятилетняя выживаемость составляет 40—50%, а в случае их выявления — 8% [7]. Прогноз зависит также от гистологических признаков инвазии сосудов (в случае их выявления продолжительность жизни в среднем составляет 11 мес, при их отсутствии — 39 мес).
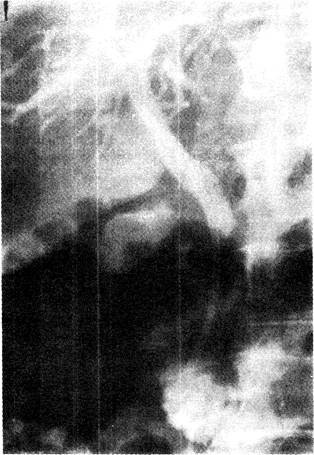
Рис. 33-4. Эндопротез из полиэтилена 10 F . установленный эндоскопически в суженном дистальном отделе общего желчною протока, обеспечил свободное прохождение контрастного вещества в двенадцатиперстную кишку и декомпрессию жёлчных путей.
Методом выбора при раке ампулы также является панкреатодуоденальная резекция. В ряде случаев у таких больных производят локальное иссечение опухоли (ампулэктомию) [3|. У неоперабельных больных иногда удаётся добиться ремиссии или уменьшения размеров рака ампулы эндоскопической фотохимиотерапией 11 j. Этот метод заключается в эндоскопическом облучении опухоли, сенсибилизированной внутривенным введением гематопорфирина, красным светом (длина волны 630 нм).
Паллиативные вмешательства
К паллиативным вмешательствам относятся наложение обходных анастомозов и эндоскопическое или чрескожное чреспечёночное эндопротезирование (стентирование).
При появлении на фоне желтухи рвоты вследствие обструкции двенадцатиперстной кишки выполняют холедохоеюностомию и гастроэнтеростомию. При изолированной обструкции жёлчного протока некоторые авторы рекомендуют во время наложения билиодигестивного анастомоза профилактически наложить также гастроэнтероанастомоз. Однако большинство хирургов решают этот вопрос исходя из размеров опухоли и проходимости двенадцатиперстной кишки во время интраоперационной ревизии.
Выбор между хирургическим и нехирургическим методом лечения зависит от состояния больного и опыта хирурга.
Эндоскопическое стентирование (рис. 33-4) оказывается успешным в 95% случаев (в 60% с первой попытки); при этом летальность в течение 30 дней после вмешательства оказывается ниже, чем при наложении билиодигестивного анастомоза [38]. Если эндоскопическая процедура оказывается безуспешной, можно выполнить чрескожное или комбинированное чрескожное и эндоскопическое стентирование [34] (см. главу 29).
Результаты чрескожного стентирования (рис. 29-20), летальность, частота осложнений аналогичны результатам паллиативных операций; при этом средняя продолжительность жизни больных после этих вмешательств составляет соответственно 19 и 15 нед. К осложнениям стентирования относятся кровотечение и жёлчеистечение [5]. Эндоскопическое эндопротезирование реже сопровождается осложнениями и смертью больных, чем чрескожное [40].
У 20—30% больных в течение 3 мес после установки пластмассовые стенты приходится заменять вследствие обструкции их сгустками жёлчи [39]. Расправляющиеся стенты из металлической сетки вводят как эндоскопически, так и чрескожно (см. рис. 29-16). Эти стенты остаются проходимыми дольше, чем пластмассовые (в среднем 273 и 126 дней соответственно) [11]. Но, учитывая высокую стоимость таких стентов, их устанавливают в основном у тех больных с нерезектабельным периампулярным раком, у которых во время замены пластмассового стента в связи с закупоркой констатируют медленный рост опухоли и предполагают относительно большую продолжительность жизни [29].
Стентирование жёлчных протоков без вскрытия брюшной полости особенно показано пожилым больным из групп высокого риска, у которых выявлены крупная нерезектабельная опухоль поджелудочной железы или обширные метастазы. У более молодых больных с нерезектабельной опухолью, у которых предполагается большая продолжительность жизни, можно прибегнуть к наложению билиодигестивного анастомоза.
Согласно современным подходам к лечению рака головки поджелудочной железы, больной не должен умереть с неустранённой желтухой или страдая от невыносимого зуда.
Вспомогательные методы лечения
Результаты предоперационной химио- и рентгенотерапии неутешительны. В некоторых случаях улучшения удаётся добиться, применяя после радикальной резекции комбинированную рентгено-и химиотерапию [16]. При нерезектабельных опухолях никакие схемы лучевой или химиотерапии не дали положительных результатов.
Блокада чревного сплетения (чрескожная под рентгенологическим контролем или интраоперационная) позволяет на несколько месяцев уменьшить боли, однако более чем в половине случаев они появляются вновь [24].
Доброкачественная ворсинчатая аденома фатеровой ампулы [36]
Эта опухоль вызывает жёлчную колику и обструктивную желтуху. ЭРХПГ позволяет выявить опухоль ампулы и выполнить биопсию.
При исследовании полученной ткани выявляют дисплазию, карциноэмбриональный антиген и онкомаркёр СА19/9 [48]. Эти изменения следует трактовать как предрак. При ворсинчатой аденоме ампулы производят панкреатодуоденальную резекцию [3]. Если радикальная операция невозможна, прибегают к паллиативной мере — установке стента. В настоящее время изучается эффективность эндоскопической фотохимиотерапии [1].
Кистозные опухоли поджелудочной железы [45]
Кистозные опухоли поджелудочной железы могут быть доброкачественными или злокачественными. К ним относят цистаденокарциному, простую (серозную или слизистую) и папиллярную цистаденому. Их можно принять за псевдокисты. В 40% случаев они протекают бессимптомно. Программа обследования должна включать КТ, ангиографию и ЭРХПГ. Диагностике может помочь исследование содержимого кисты (цитологическое и иммуногистохимическое для выявления онкомаркёров) [22]. Опухоль бывает злокачественной в 44% случаев. Методом выбора является панкреатодуоденальная резекция. Результаты исследования свежезамороженных срезов и даже результаты обычного гистологического исследования могут быть ошибочными. Все слизистые кистозные новообразования следует считать потенциально злокачественными.
Эндокринные опухоли поджелудочной железы [37]
К эндокринным опухолям поджелудочной железы относят инсулиному, карциноидную опухоль, гастриному, ВИПому, ППому и соматостатиному. Для клинической картины этих опухолей характерны признаки объёмного образования в эпигастральной области, боль, желтуха, а также системные проявления действия выделяемого ими гормона. Частота малигнизации зависит от типа опухоли. Лечение заключается в иссечении опухоли или резекции поджелудочной железы, а также в назначении лекарственных средств для нейтрализации эффектов выделяемых опухолью гормонов. Пятилетняя выживаемость в целом составляет 40-60%.
Хронический панкреатит
Панкреатит, обычно алкогольной этиологии, может вызывать сужение внутри панкреатической части общего жёлчного протока [2]. При обострениях панкреатит может возникать преходящий холестаз, который обусловлен преимущественно отёком поджелудочной железы. Более длительно сохраняющийся холестаз наблюдается при сдавлении общею желчною протока фиброзно-изменённой тканью поджелудочной железы на фоне прогрессирующего панкреатита. Обструкция общего желчного протока и стойкий холестаз могут наблюдаться также при сдавлении его псевдокистой пли абсцессом головки поджелудочной железы.
Стеноз общего жёлчного протока развивается примерно у 8% больных с хроническим алкогольным панкреатитом: если чаще проводить холангиографию. лот показатель, по-видимому, окажется ещё выше. Заподозрить стеноз общего жёлчного протока можно при более чем двукратном повышении активности ЩФ на протяжении более 1 мес. При ЭГХПГ выявляют сужение дистального отела общею жёлчного протока, ровные контуры его, что иногда напоминает «крысиный хвост» (рис. 33-5). Проток поджелудочной железы может быть извитым, расширенным и иметь неровные контуры. Возможно обызвествление поджелудочной железы.
При биопсии печени выявляют портальный фиброз |27|. признаки билиарной обструкции, иногда билиарный цирроз. Признаки алкогольного поражения печени встречаются редко.
Хронический панкреатит может осложняться тромбозом селезёночной вены.
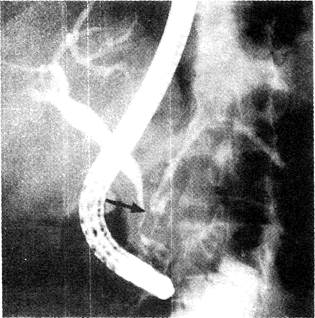
Рис. 33-5. Хронический алкогольный панкреатит. При ЭРХПГ отмечается сужение дистальных отделов общего жёлчного протока по типу «крысиного хвоста» (показано стрелкой).
Лечение
При панкреатите большое значение имеет ранняя диагностика стриктуры жёлчных путей, поскольку отсутствие желтухи не исключает возможности развития билиарного цирроза и острого холангита.
Больной должен полностью отказаться от употребления алкоголя.
Значение хирургического лечения окончательно не установлено. Данные клинического и лабораторного обследования, а также результаты визуализационных методов исследования не всегда позволяют отличить больных со стенозом общего жёлчного протока от больных, страдающих алкогольной болезнью печени или имеющих нормальную гистологическую картину при биопсии печени [211. Биопсия печени позволяет оценить необходимость хирургической декомпрессии жёлчного протока. Обструкцию жёлчного протока, обусловленную хроническим панкреатитом, можно успешно устранить с помощью пластиковых или металлических сетчатых стентов, но для оценки этого метода лечения требуется изучение отдалённых результатов. Острый холангит, билиарный цирроз и стойкая желтуха — абсолютные показания к хирургическому вмешательству. Обычно выполняют холедохоэнтеростомию.
Обструкция общего жёлчного протока увеличенными лимфатическими узлами
Сдавление общего жёлчного протока лимфатическими узлами наблюдается чрезвычайно редко. Увеличенные лимфатические узлы билиопанкреатодуоденальной зоны почти всегда поражены метастазами; источник этих метастазов часто находится в желудочно-кишечном тракте, в лёгких или в молочной железе или им оказывается гепатокарцинома.
Метастазы в лимфатические узлы ворот печени вызывают выраженную желтуху; при этом чаще отмечается инвазия общего жёлчного протока, чем просто сдавление. Метастазы в паренхиму печени также могут поражать жёлчные протоки, вызывая их обструкцию.
Лимфатические узлы по ходу общего жёлчного протока могут увеличиваться не только при злокачественных новообразованиях, но при этом обычно не происходит сдавление протока. Желтуха при саркоидозе и инфекциях, например при туберкулёзе, инфекционном мононуклеозе, обусловлена не обструкцией, а непосредственным поражением печени или гемолизом.
Увеличение лимфатических узлов при ретикулёзах очень редко вызывает обструкцию общего жёлчного протока, а наблюдаемая в этом случае желтуха обусловлена поражением паренхимы печени, усилением гемолиза или имеет неясную холестатическую природу (см. главу 4).
Дата добавления: 2017-02-20; просмотров: 914;
