Области применения КМ 1 страница
Наиболее широко используются полимерные композиционные материалы-композиты. Большая номенклатура матриц в виде термореактивных и термопластичных полимеров обеспечивает их широкий выбор для работы в диапазоне от отрицательных температур до 100-200°С - для органопластиков, до 300-400 °С, для стекло-, угле- и боропластиков. Композиты с полиэфирной и эпоксидной матрицей работают до 120-200°, с феноло-формальдегидной - до 200-300 °С, полиамидной и кремнийорганической - до 250-400°С. Металлические композиционные материалы на основе алюминия, магния и их сплавов, армированные волокнами из бора, углерода, карбида кремния применяют до 400-500°С; композиционные материалы на основе сплавов никеля и кобальта работают при температуре до 1200 °С, на основе тугоплавких металлов и их соединений - до 1700°С, на основе углерода и керамики - до 2000 °С.
Использование композитов в качестве конструкционных, теплозащитных, антифрикционных, радио- и электротехнических и других материалов позволяет снизить массу конструкции, повысить ресурсы и мощности машин и агрегатов, создать принципиально новые узлы, детали и конструкции. Композиционные материалы применяют в химической, текстильной, горнорудной, металлургической промышленности, машиностроении, на транспорте, для изготовления спортивного снаряжения, музыкальных инструментов, в строительстве, в военном деле и т.п..
КМ различных типов и конструкций находят широкое применение в различной сфере человеческой деятельности:
- в судостроении: детали судов, яхт, катеров, внутренняя отделка, судовая мебель, буи, бакены, оснастка для рыбного промысла;
- в машиностроении: коррозионностойкое оборудование, детали машин станков, механизмов;
- оборудование для очистки воды;
- в строительстве: железо-бетонные изделия, фасады зданий, отделка, перегородки, панели для крыш, элементы сборных конструкций: двери, рамы;
- сельское хозяйство: силосные башни, клетки для скота, сараи, планки для подвешивания тушь скота;
- в быту: мебель, корпуса телевизоров, лыжи, оборудование для спортивных площадок и для аттракционов, элементы конструкций плавательных бассейнов, спортивные тумбы, спортивные снаряды и т.д
Разрабатываются КМ со специальными свойствами, например, радиопрозрачные и радиопоглощающие материалы, материалы для тепловой защиты орбитальных космических аппаратов (с малым коэффициентом линейного термического расширения и высоким удельным модулем упругости) и другие. Прочностные свойства КМ на основе алюминия и магния (прочность, модуль упругости, усталостная и длительная прочность) более чем в 2 раза (до 500 °С) выше, чем у обычных сплавов. КМ на основе никеля и кобальта увеличивают уровень рабочих температур от 1000 до 1200°С, а на основе тугоплавких металлов и соединений — до 2000°С. Повышение прочностных и упругих свойств материалов позволяет существенно облегчить конструкции, а увеличение рабочих температур этих материалов даёт возможность повысить мощность двигателей, машин и агрегатов.
Области применения КМ многочисленны; кроме авиационно-космической, ракетной и других специальных отраслей техники, они применяются в автомобильной промышленности — для деталей двигателей и кузовов автомашин; в машиностроении — для корпусов и деталей машин; в горнорудной промышленности — для бурового инструмента, буровых машин и др.; в металлургической промышленности — в качестве огнеупорных материалов для футеровки печей, кожухов и другой арматуры печей, наконечников термопар; в строительстве — для пролётов мостов, опор мостовых ферм, панелей для высотных сборных сооружений и др.; в химической промышленности — для автоклавов, цистерн, аппаратов сернокислотного производства, ёмкостей для хранения и перевозки нефтепродуктов и др.; в текстильной промышленности — для деталей прядильных машин, ткацких станков и др.; в сельскохозяйственном машиностроении — для режущих частей плугов, дисковых косилок, деталей тракторов и других; в бытовой технике — для деталей стиральных машин, рам гоночных велосипедов, деталей радиоаппаратуры и др.
Применение КМ в ряде случаев потребует создания новых методов изготовления деталей и изменения принципов конструирования деталей и узлов конструкций.
Области применения композиционных материалов с каждым годом становятся все шире. Они применяются в авиации для высоконагруженных деталей самолетов (обшивки, лонжеронов, нервюр, панелей и т.д.) и двигателей (лопаток компрессора и турбины и т.д.), в космической технике для узлов силовых конструкций аппаратов, подвергающихся нагреву, для элементов жесткости, панелей, в автомобилестроении для облегчения кузовов, рессор, рам, панелей кузовов, бамперов и т. д., в горной промышленности (буровой инструмент, детали комбайнов и т.д.), в гражданском строительстве (пролеты мостов, элементы сборных конструкций высотных сооружений и т. д.) и в других областях народного хозяйства.
Применение композиционных материалов обеспечивает новый качественный скачок в увеличении мощности двигателей, энергетических и транспортных установок, уменьшении массы машин и приборов.
Органоволокниты применяют в качестве изоляционного и конструкционного материала в электро-и радиопромышленности, авиационной технике, автостроении; из них изготовляют трубы, емкости для реактивов, покрытия корпусов судов и другое.
Стекловолокниты – это композиция, состоящая из синтетической смолы, являющейся связующим, и стекловолокнистого наполнителя. В качестве наполнителя применяют непрерывное или короткое стекловолокно. Прочность стекловолокна резко возрастает с уменьшением его диаметра (вследствие влияния неоднородностей и трещин, возникающих в толстых сечениях). Свойства стекловолокна зависят также от содержания в его составе щелочи; лучшие показатели у бесщелочных стекол алюмоборосиликатного состава.
Неориентированные стекловолокниты содержат в качестве наполнителя короткое волокно. Это позволяет прессовать детали сложной формы, с металлической арматурой. Материал получается с изотопными прочностными характеристиками, намного более высокими, чем у пресс-порошков. Представителями такого материала являются стекловолокниты АГ-4В, а также ДСВ (дозирующиеся стекловолокниты), которые применяют для изготовления силовых электротехнических деталей, деталей машиностроения (золотники, уплотнения насосов и т.д.). При использовании в качестве связующего непредельных полиэфиров получают премиксы ПСК (пастообразные) и препреги АП и ППМ (на основе стеклянного мата). Препреги можно применять для крупногабаритных изделий простых форм (кузова автомашин, лодки, корпуса приборов и т.п.).
Композиционные материалы с неметаллической матрицей, а именно полимерные карбоволокниты используют в судо- и автомобилестроении (кузова гоночных машин, шасси, гребные винты); из них изготовляют подшипники, панели отопления, спортивный инвентарь, детали вычислительной техники. Высокомодульные карбоволокниты применяют для изготовления деталей авиационной техники, аппаратуры для химической промышленности, в рентгеновском оборудовании и другом.
Карбоволокниты с углеродной матрицей заменяют различные типы графитов. Они применяются для тепловой защиты, дисков авиационных тормозов, химически стойкой аппаратуры.
Изделия из бороволокнитов применяют в авиационной и космической технике (профили, панели, роторы и лопатки компрессоров, лопасти винтов и трансмиссионные валы вертолетов и т.д.).
В машиностроении композиционные материалы широко применяются для создания износостойких покрытий на поверхности деталей узлов трения, а также для изготовления различных деталей двигателей внутреннего сгорания.
Полимерные материалы на основе политетрафторэтиленов модифицируются ультрадисперсными алмазографитовыми порошками, получаемыми из взрывных материалов, а также ультрадисперсных порошков мягких металлов.
В авиации и космонавтике с 1960-х годов существует острая необходимость в изготовлении прочных, лёгких и износостойких конструкций. Композиционные материалы применяются для изготовления силовых конструкций летательных аппаратов, искусственных спутников, теплоизолирующих покрытий космических зондов. Композиты широко применяются для изготовления обшивок воздушным и космическим аппаратам, а так же к наиболее нагруженным силовым элементам.
Благодаря своим характеристикам (прочности и лёгкости) КМ применяются в военном деле для производства различных видов брони: бронежилетов, касок, брони для военной техники.
Множество изобретений в этой сфере были придуманы во время войн. Вторая мировая война позволила армированным полимерам перекочевать из лабораторий в реальный мир. Альтернативные материалы, позволяющие снизить вес конечного изделия, были необходимы в военном авиастроении. Очевидным стали преимущества композитов в плане их веса и прочности.
В настоящее время практически все страны мира для повышения эффективности и мобильности военного оборудования применяют для изготовления стратегических оружий и оборонительной техники композиционные материалы. И это очень широкий спектр, например, сменный ствол винтовки Christensen Arms, выполнен из углепластика. Винтовка построена на базе затворной группы Remington-700.
Приклады для винтовок, выполнены из композитных материалов. В целом, область применения КМ в военном деле широко распространена. Например, межконтинентальная баллистическая ракета «Тополь-М»: на 90% состоит из композитов, включая конструкции двигателей и головную часть.
Стволы для винтовок, пластиковые приклады, обоймы и магазины из композиционных материалов, бинокли, ножи и многие другие.
Основное преимущество КМ в том, что материал и конструкция создается одновременно. Исключением являются препреги, которые являются полуфабрикатом для изготовления конструкций. Следует отметить, что КМ создаются под выполнение конкретных задач, соответственно не могут вмещать в себя все возможные преимущества. Это значит, что КМ не явлется идеальным материалом. Прочность КМ определяется уровнем межмолекулярного (адгезионного) взаимодействия между адгезивом и субстратом, матрицей и наполнителем.
2. Теоретические основы межмолекулярных взаимодействий на границе раздела фаз
КМ имеют различные конструкции, состоят из различных материалов, но большинство из них имеют одно общее – они получены путем склеивания двух и более поверхностей. Прочностные свойства КМ зависят от адгезионной прочности, определяемой взаимодействием между молекулами и атомами веществ различной природы.
Под адгезией понимают сцепление между двумя приведенными в контакт материалами, различными по своей природе. Трудно назвать сферу человеческой деятельности, где бы не приходилось сталкиваться с адгезией, начиная с изготовления обуви до производства сложнейших космических аппаратов.
Адгезионные явления имеют место при производстве КМ и изготовлении изделий из них, сварке металлов и пластиков, в картонном и обувном производствах, ракетной и космической технике и т.д.
Адгезия – сцепление (слипание) приведенных в контакт разнородных твердых или жидких тел, обусловленное межмолекулярной связью. Адгезия (от лат. adhaesio — прилипание) в физике — сцепление поверхностей разнородных твёрдых и/или жидких тел. Адгезия обусловлена межмолекулярными взаимодействиями (вандерваальсовым, водородным, химическими связями) в поверхностном слое и характеризуется удельной работой, необходимой для разделения поверхностей. В некоторых случаях адгезия может оказаться сильнее, чем когезия, т. е. межмолекулярного взаимодействия внутри однородного материала, в таких случаях при приложении разрывающего усилия происходит когезионный разрыв, т. е. разрыв в объёме менее прочного из соприкасающихся материалов.
Адгезия имеет место в процессах склеивания, пайки, сварки, нанесения покрытий. Адгезия матрицы и наполнителя композитов (композиционных материалов) является также одним из важнейших факторов, влияющих на их прочность.
Явление адгезии имеет место при сварке, паянии, лужении, склеивании, при изготовлении фотоматериалов, а также при нанесении лакокрасочных полимерных покрытий, предохраняющих металлические детали от коррозии; причинами нарушения адгезии в последнем случае являются напряжения, возникающие вследствие усадки плёнки, а также различие коэффициентов теплового расширения плёнки и металла.
Адгезия также является причиной повышенного износа трущихся деталей.
Адгезия существенно влияет на природу трения соприкасающихся поверхностей: так, при трении поверхностей с низкой адгезией трение минимально. В качестве примера можно привести политетрафторэтилен (тефлон), который в силу низкого значения адгезии в сочетании с большинством материалов обладает низким коэффициентом трения. Для устранения адгезионных явлений при трении тонтактирующих поверхностей вводят слой смазки, препятствующий их контакту. Некоторые вещества со слоистой кристаллической решёткой (графит, дисульфид молибдена), характеризующиеся одновременно низкими значениями адгезии и когезии, применяются в качестве твёрдых смазок. При рассмотрении данного материала различают понятия:
Фаза (англ. phase) - однородная обособленная часть системы, отделенная от других частей разграничивающими поверхностями.
Адгезив (англ. adhesive) - клеящее вещество или связующее (клей), соединяющий между собой другие материалы путем сцепления с их поверхностями. Подразделяется на - органические (природные, синтетические);
- неорганические (силикатные и на основе неорганических вяжущих веществ-металлфосфатные клеи или зубные цементы).
Агеренд (англ. adherend) - склеиваемый материал, субстрат.
Субстрат (англ. substrate) - материал, на поверхность которого наносят клей. склеиваемые материалы, которые подразделяются на
- неорганические (стекло, металлы, керамика и др.);
- органические (каучуки, целлюлоза, кожа, и т.д.).
Аутогезия - связь одноименных (совместимых) материалов от момента приведения их в контакт до момента диффузионного исчезновения геометрической границы раздела.
Когезия (англ. cohesion) – взаимодействие (сцепление) между находящимися в контакте поверхностями двух однородных по составу тел.
Липкость - сопротивление, оказываемое клеем при отделении его от субстрата.
Промотор - добавка к адгезиву (клею), увеличивающая механическую прочность адгезионных соединений.
Соединение клеевое - соединение двух субстратов (тел) между собой слоем клея (рисунок 2.1.).
Абгезив (англ. abhesive) - разделительный материал, предотвращающий адгезию.
|
|
|

Рисунок 2.1. Схема адгезионного соединения
Образование клеевых соединений, лакокрасочных покрытий начинается с растекания полимера по поверхности субстрата, ее смачивания, а затем адсорбции полимеров и формирования клеевого соединения в зависимости от природы растворителей, наполнителей, пластификаторов, и самой поверхности субстрата.
Адгезионное явление – результат проявления молекулярного взаимодействия между материалами адгезива и субстрата на границе раздела фаз, в результате чего могут возникать самые различные силы, от наиболее слабых – физических (водородных, Ван-дер-Ваальсовых) до сил химической природы.
2.1.Виды межмолекулярных взаимодействий на границе раздела фаз
Основой адгезионных взаимодействий являются межмолекулярные связи между адгезивом и субстратом, начиная от самых слабых-дисперсионных (физических) до сиьных-химических (ионных, ковалентных, координационных).
Виды связи дифференцируют условно на первичные и вторичные (таблица 2. 1). Физические взаимодействия составляют кулоновские, Ван-дер-ваальсовые силы, водородного взаимодействия. Промежуточное состояние между физическими и химическими взаимодействиями занимают комплексные соединения, в которых реализуются донорно-акцепторные, водородные взаимодействия.
Таблица 2.1. – Виды связи и уровень их энергии
| № | Вид связи | Энергия связи, кДж/моль |
| Первичные: | ||
| ионные | 600 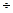 1100 1100
| |
| ковалентные | 60-700 | |
| металлические | 110-350 | |
| химические | ||
| кислотно-основные | 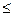 1000 1000
| |
| кислотно-основные льюисовского типа | 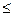 80-100 80-100
| |
| Вторичные: | ||
| водородное | 4-7 ккал/моль, может достигать значений 20-30 ккал/моль. | |
| с участием атомов фтора | 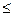 40 40
| |
| в отсутствие атомов фтора | 10 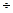 25 25
| |
| Ван-дер-ваальсовые | 1–30 кДж/моль. | |
| .5 | диполь-дипольные взаимодействия | 4-20 |
| индуцированные диполь-дипольные | До 2,0 | |
| Дисперсионные (лондоновские) взаимодействия | 0,08 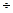 40 40
| |
| Кислота-донор, основание-акцептор атома водорода | ||
| Кислота-акцептор, основание-донор электронной шары |
Ван-дер-ваальсовые силы — одна из разновидностей сил притяжения, действующих между атомами и молекулами. Важность этих сил следует из двух уникальных их свойств. Во-первых, эти силы универсальны. Такой механизм притяжения действует между всеми атомами и молекулами. Он ответствен за такие явления, как сцепление атомов инертных газов в твердом и жидком состояниях и физическая адсорбция молекул на поверхности твердых тел, когда отсутствуют химические связи. Во-вторых, эти силы сохраняют значительную величину при сравнительно больших расстояниях между молекулами и отличаются аддитивностью для большого числа молекул. Ван-дер-ваальсовы силы влияют на различные свойства газов. Кроме того, они приводят к возникновению притяжения между двумя твердыми объектами, разделенными малым зазором, что существенно для сцепления и устойчивости коллоидов. Если молекулы находятся на некотором расстоянии друг от друга, теоретические выражения для этих сил особенно просты и к настоящему времени подтверждены экспериментально как для изолированных молекул, так и для двух твердых объектов, разделенных малым зазором.
Межмолекулярные физические взаимодействие - взаимодействие молекул между собой, не приводящее к разрыву или образованию новых химических связей. В их основе, как и в основе химической связи, лежат электрические взаимодействия. Ван-дер-ваальсовы силы заметно уступают химическому связыванию. Силы Ван-дер-Ваальса включают все виды межмолекулярного притяжения и отталкивания. Они получили название в честь Я.Д. Ван-дер-Ваальса, который первым принял во внимание межмолекулярные взаимодействия для объяснения свойств реальных газов и жидкостей. Эти силы определяют отличие реальных газов от идеальных, существование жидкостей и молекулярных кристаллов. От них зависят многие структурные, спектральные и другие свойства веществ.
Основу ван-дер-ваальсовых сил составляют кулоновские силы взаимодействия между электронами и ядрами одной молекулы, ядрами и электронами другой. На определенном расстоянии между молекулами силы притяжения и отталкивания уравновешивают друг друга, и образуется устойчивая система.
Полярные молекулы, в которых центры тяжести положительного и отрицательного зарядов не совпадают, например HCl, H2O, NH3, ориентируются таким образом, чтобы рядом находились концы с противоположными зарядами. Между ними возникает притяжение.
Различают ориентационные, индукционные и дисперсионные силы. Ориентационные и индукционные силы возникают при взаимодействии полярных молекул. Дисперсионные силы обусловлены возникновением мгновенных дипольных моментов, вызванных флуктуацией электронной плотности.
Ориентационное взаимодействие.Такой вид межмолекулярного взаимодействияосуществляетсямежду полярными молекулами (диполь–диполь), т. е. молекулами с постоянными дипольными моментами (рисунок2.2.).

Рисунок 2.2. Схемы взаимодействия диполей.
Потенциал взаимодействия (U0) жестко ориентированных диполей является анизотропным, т. е. зависит от ориентации постоянного диполя. Он пропорционален квадратам дипольных моментов и обратно пропорционален температуре и расстоянию между диполями в шестой степени:
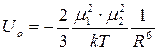 , 2.1.
, 2.1.
где m1 и m2 – моменты диполей; k – постоянная Больцмана; Т - температура, R – расстояние между диполями.
Притяжение диполей может осуществляться только тогда, когда энергия притяжения превышает тепловую энергию молекул. Обычно это имеет место в твердых и жидких веществах. Диполь-дипольное взаимодействие проявляется в полярных жидкостях (например,вода).
Индукционное взаимодействие. Если рядом с полярной молекулой окажется неполярная, то полярная молекула начнет влиять на нее. Поляризация нейтральной частицы под действием внешнего поля (наведение диполя) происходит благодаря наличию у молекул свойства поляризуемости γ. Постоянный диполь может индуцировать дипольное распределение зарядов в неполярной молекуле. Под действием заряженных концов полярной молекулы электронные облака неполярных молекул смещаются в сторону положительного заряда и дальше от отрицательного. Неполярная молекула становится полярной, и молекулы начинают притягиваться друг к другу, только намного слабее, чем две полярные молекулы (рисунок 2.3.).
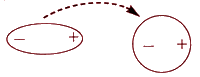
Рисунок 2.3. Схема взаимодействия полярной и неполярной молекул.
Энергия взаимодействия наведенных диполей, называемая индукционной или поляризационной определяется по формуле 2.2:
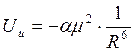 , где 2.2
, где 2.2
a - коэффициент поляризации молекул.
Энергия притяжения между постоянным и наведенным диполем (энергия Дебая) определяется выражением:
EД = −2 μнав2 γ / R6, 2.3
где μнав - момент наведенного диполя.
Притяжение постоянного и наведенного диполей обычно очень слабое, поскольку поляризуемость молекул большинства веществ невелика. Оно действует только на очень малых расстояниях между диполями. Этот вид взаимодействия проявляется главным образом в растворах полярных соединений в неполярных растворителях.
Дисперсионное взаимодействие. Между неполярными молекулами также может возникнуть притяжение. Электроны, которые находятся в постоянном движении, на миг могут оказаться сосредоточенными с одной стороны молекулы, то есть неполярная частица станет полярной. Это вызывает перераспределение зарядов в соседних молекулах, и между ними устанавливаются кратковременные связи (рисунок 2.4.):

Рисунок 2.4. Схема установления связи между неполярными молекулами
Энергия такого взаимодействия (энергия Лондона) описывается уравнением:
Eд = −2 μмгн2 γ2 / R6, 2.4
где μмгн - момент мгновенного диполя. Лондоновские силы притяжения между неполярными частицами (атомами, молекулами) являются весьма короткодействующими. Значения энергии такого притяжения зависят от размеров частиц и числа электронов в наведенных диполях. Эти связи очень слабые - самые слабые из всех межмолекулярных взаимодействий. Однако они являются наиболее универсальными, так как возникают между любыми молекулами.
Под воздействием внешнего поля (света) происходит смещение центров тяжести электрических зарядов молекул. Дисперсионное или лондоновское взаимодействие молекул описывается следующей формулой:
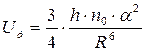 , 2.5
, 2.5
h·n0 – термический или характеристический квант, который определяется на основе дисперсии света.
| Среди перечисленных наиболее сильными, как правило, являются дисперсионные взаимодействия. Для небольших молекул энергия ван-дер-ваальсовых взаимодействий может составлять порядка 1–30 кДж/моль. Ван-дер-ваальсовое взаимодействие имеет место не только между молекулами, но и между нанообъектами, например углеродными нанотрубками. Несмотря на слабость этого взаимодействия, оно обеспечивает устойчивость молекулярных кристаллов, клатратов, супрамолекулярных комплексов, связь молекул с поверхностями (адсорбцию) и играет важную роль в процессах синтеза и построения молекулярных наноструктур. |
Межмолекулярное отталкивание. Если бы молекулы только притягивались друг к другу, это привело бы к их слиянию. Но на очень малых расстояниях их электронные оболочки начинают отталкиваться. Энергия отталкивания описывается выражением 2.6:
E = + k / R6, 2.6
где k - постоянная отталкивания, n принимает различные целые значения (5-15). Силы межмолекулярного отталкивания действуют на очень малых расстояниях.
Общее уравнение межмолекулярного взаимодействия при постоянной температуре (уравнение Леннарда-Джонсона) в большинстве случаев имеет вид
EM = − a / r6 + b/ r12 2.7
и носит название "потенциала 6-12", поскольку энергия притяжения пропорциональна 1 / r6, а энергия отталкивания - 1 / r12.
Силы взаимного притяжения молекул обратно-пропорциональны межмолекулярному расстоянию R6. Эти силы быстро убывают с увеличением расстояния и становятся очень малыми на расстояниях ~5А°. Важная роль во взаимодействиях между молекулами адгезива и субстрата принадлежит водородным связям. Энергия водородной связи, оцениваемая обычно = 4-7 ккал/моль, может достигать значений 20-30 ккал/моль.
Имеется еще один вид межмолекулярного взаимодействия – это поляризационная связь. Частным случаем этого взаимодействия являются связи с переносом заряда, т.е. образованием комплексов между адгезивом и субстратом. В результате переноса зарядов относительно неактивные молекулы могут приобрести реакционную способность. Энергия образования комплексов колеблется от десятых долей до нескольких ккал/моль.
Одним из видов межмолекулярного взаимодействия является донорно-акцепторное взаимодействие, приводящее к образованию комплексов. Различают слабые (с энергией связей ~2 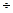 3 ккал/моль) и прочные (с энергией связей до 50 ккал/моль) комплексы, т.е. с энергиями, близкими к ван-дер-ваальсовым и химическим связям.
3 ккал/моль) и прочные (с энергией связей до 50 ккал/моль) комплексы, т.е. с энергиями, близкими к ван-дер-ваальсовым и химическим связям.
Донорами электронов с переносом заряда в органических комплексах являются ароматические углеводороды и некоторые их производные, полимеры с сопряженными связями. В качестве акцепторов выступают галогены, галогенводороды, хлориды металлов, ангидриды ди- и поликарбоновых кислот, хлорангидриды, нитропроизводные, бензол, хиноны и их производные.
Между молекулами адгезива и субстрата возможно образование и химических связей – ковалентных, ионных, координационные с энергией от нескольких десятков до сотен ккал/моль.
Адгезионная прочности оценивается по сопротивлению разрушения адгезионного соединения. Для упрощения расчета предположим, что разрушение адгезионного соединения происходит путем одновременного нарушения молекулярных связей на определенной площади контакта (по методу нормального отрыва).
Теоретические значения механической прочности выражаются формулой 2.8:
Fm = 1,46·(U/r), 2.8
где U – потенциальная энергия частиц; r – расстояние между частицами.
Прочность композиционного материала зависит от природы материалов, входящих в состав КМ, прочности связи между молекулами адгезива и субстрата на границе раздела фаз.
2. Теории адгезии полимеров
Первые работы по изучению механизма адгезии появились в начале 20-х годов прошлого столетия. В связи с развитием науки и техники активно проводились научные исследования, накапливался и обобщался экспериментальный материал по влиянию различных факторов на прочность адгезионных соединений. В связи с этим стали появляться теоретические работы по адгезии.
Дата добавления: 2017-02-20; просмотров: 1134;
