Пальмитиновая кислота
гексадекан 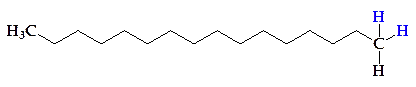
Сравнение этих веществ показало, что для получения искусственных жирных кислот нужно к парафиновым углеводородам «прибавить» кислород, то есть окислить их. На этом и основано производство заменителей пищевых жиров. Жирные кислоты получаются из недефицитных продуктов переработки нефти.
Но если принцип синтеза жирных кислот очень прост, то сам процесс их получения достаточно сложен. Промышленный синтез жирных кислот представляет собою крупное современное производство. Оно состоит из трех этапов: окисления парафина и получения так называемой смеси сырых кислот, их «облагораживания» (очищения от примесей) и, наконец, разделения «облагороженной» смеси на отдельные фракции жирных кислот.
Окисление парафина производится в больших аппаратах — колоннах, заполненных расплавленным парафином, в массе которого находится катализатор. Снизу с помощью распыляющего устройства подают сильную струю воздуха, который проходит сквозь толщу парафина. В результате кислород соединяется с парафиновыми углеводородами и превращает их в жирные кислоты.
В составе парафина находится много различных углеводородов с числом атомов углерода от 18 до 36. Они вступают во взаимодействие с кислородом с разной скоростью; кроме того, при этом наблюдается множество побочных реакций. В результате наряду с жирными кислотами выделяется ряд менее ценных веществ. Поэтому после реакции окисления производят очистку жирных кислот от примесей. Окисленный парафин откачивают и промывают; при этом теплая вода уносит из него отработанный катализатор и некоторые ненужные вещества. Чтобы отделить жирные кислоты от основной массы всех остальных веществ, не вступивших в реакцию, парафин подается в смеситель, где обрабатывается раствором соды. При этом жирные кислоты превращаются в мыльный раствор. Затем на втором этапе производства эту смесь подвергают тепловой обработке: она нагревается в печи под высоким давлением до 320 0С и подается в испаритель. Здесь вода и еще оставшиеся в составе кислот вредные примеси испаряются, уносятся вверх и попадают в холодильник, а «облагороженный» раствор стекает вниз. Он направляется в мешалку, где обрабатывается серной кислотой в присутствии сульфата натрия. Серная кислота, разрушая мыло, выделяет жирные кислоты в свободном состоянии, так сказать, возвращает им нормальный вид. Далее жирные кислоты промываются и сушатся. И, наконец, наступает третий, последний этап производства. Смесь жирных кислот проходит через вакуум-аппараты, при этом из нее выделяются отдельные, необходимые промышленности фракции жирных кислот. Процесс этот совершается многократно. Подобным способом вырабатывается большое количество жирных кислот — до 920 килограммов из одной тонны парафина. Так в общих чертах осуществляется синтез жирных кислот.
Отходы, получаемые при «облагораживании» жирных кислот, не выбрасываются. В составе этих веществ находятся углерод, водород и кислород — те элементы, из которых «строятся» жирные кислоты. В дальнейшем они используются поэтому как сырье: смешиваются с новой порцией парафина и вместе с ним снова подвергаются окислению. Синтетические жирные кислоты почти лишены цвета, запаха и посторонних примесей. Они мало отличаются от кислот, выделенных из растительных и животных жиров.
В наши дни искусственные жирные кислоты все более заменяют природные жиры в разных отраслях промышленности. Они используются в производстве мыла вместо дефицитного кокосового масла, с помощью которого раньше изготовлялись высокосортные туалетные сорта, а также вместо хлопкового масла и саломаса (гидрированный растительный жир), использовавшегося для производства бытового хозяйственного мыла.
Из синтетических жирных кислот приготовляются теперь различные смазочные материалы, которые вырабатывались прежде из растительных жиров. Синтетические кислоты успешно конкурируют с природными при изготовлении высококачественных олиф. Искусственные жиры — ценнейший материал в производстве резины: они заменяют необходимую для этого стеариновую кислоту, которую выделяют из дорогостоящего стеарина.
5.4 БИОХИМИЯ ИММОБИЛИЗОВАННЫХ ФЕРМЕНТОВ
Одним из перспективных направлений, стоящих на стыке биохимии и современной биотехнологии является технология создания иммобилизованных ферментов. Ферменты, а даже целые ферментные системы, широко используются в различных отраслях промышленности, медицине, сельском хозяйстве и т.д.
Ферменты как вещества белковой природы весь восприимчвы к действиям окружающей среды (температура, свет и т.п.), именно по этой причине они весьма неустойчивы при хранении. Кроме того, ферменты не могут быть использованы многократно из-за трудностей в отделении их от субстратов и продуктов реакций. Выход из данной ситуации был предложен в начале ХХ века когда Дж. Нельсон и Е. Гриффин адсорбировали на угле инвертазу и показали, что она сохраняет в таком виде свою каталитическую активность. Принцип создания иммобилизованных ферментов заключается в прикрепление их в активной форме к нерастворимой основе или заключение в полупроницаемую мембранную систему.
Прикрепление (иммобилизация) ферментов к носителю осуществляется адсорбционно, химической связью или путем механического включения фермента в органический или неорганический гель (в капсулу и т. п.). При этом прикрепление молекулы фермента ведется за счет функциональных групп, не входящих в активный центр фермента и не участвующих в образовании фермент-субстратного комплекса.
В качестве носителя иммобилизованного фермента могут выступать вещества органической и неорганической природы; зернистой или волокнистой структуры; пластинчатой, трубчатой, шарообразной (капсулярной) формы и т.д.
Необходимо отметить, что органические носители (низко- и высокомолекулярные) могут быть как синтетического, так и природного происхождения. Синтетические полимерные носители подразделяют на группы в связи с химическим строением основной цепи макромолекул: полиметиленовые, полиамидные, полиэфирные. Природные полимерные органические носители, получившие наибольшее распространение, делят в соответствии с их биохимической классификацией на 3 группы: полисахаридные, белковые и липидные.
Наиболее часто для иммобилизации используются такие полисахариды, как целлюлоза, декстран, агароза и их производные. Целлюлоза гидрофильна, имеет много гидроксильных групп, что позволяет модифицировать её, замещая эти группы (см. п. 5.3). Для увеличения механической прочности целлюлозу гранулируют путем частичного гидролиза, в результате которого разрушаются аморфные участки. На их место для сохранения пористости между кристаллическими участками вводят химические сшивки. Гранулированную целлюлозу легко превратить в различные ионообменные производные, такие как ДЭАЭ-целлюлоза, КМЦ и др.
Широкое распространение получили природные носители на основе декстрана, имеющие общее «сефадексы». При высушивании они легко сжимаются, в водных же растворах способны к сильному набуханию. Пористость образуемых сефадексами гелей может регулироваться степенью полимеризации углевода, а также характером и числом сшивок (чаще всего «сшивка» осуществляется формальдегидом). Подобные водорастворимые препараты часто используются как носители лекарственных средств в медицине и фармакологии.
Белки в качестве носителей обладают рядом достоинств: вместительны, способны к биодеградации, могут применяться в качестве тонкой (толщиной 80 мкм) мембраны. Иммобилизацию ферментов на белковых носителях проводят как в отсутствии, так и в присутствии сшивающих агентов. Белки используются и в фундаментальных биологических исследованиях, и в медицине. К недостаткам белков в качестве носителей относят их высокую иммуногенность (за исключением коллагена и фибрина). Наиболее для иммобилизации используются структурные (кератин, фибрин, коллаген), двигательные (миозин) и транспортные (альбумин) белки.
Синтетические полимерные носители применяются для ковалентной и сорбционной иммобилизации ферментов, для получения гелей, микрокапсул. Они могут иметь макропористую, изопористую структуру, а также гетеропористую структуру. Для получения полимерных гидрофильных носителей широко используется акриламид - производное акриловой кислоты.
Преимущества иммобилизованных ферментов перед нативными предшественниками:
- иммобилизованный фермент может быть легко отделим от реакционной среды, что позволяет приостановить реакцию в любой момент, использовать фермент повторно, или получать чистый от фермента продукт;
- реакцию можно проводить непрерывно, регулируя ее скорость, а также выход продукта;
- возможно изменение ряда свойств иммобилизованного фермента (специфичность, зависимость активности фермента от значений рН среды, ионного состава, деуствия денатурирующих агентов);
- возможна регуляция активности иммобилизованных ферментов путем изменения свойств самого носителя.
Дата добавления: 2017-08-01; просмотров: 859;
