3 страница
Вміст іонів Са і Мg у використовуваній воді має бути нижчим від розрахункової кількості цих іонів у робочому розчині, інакше порушується оптимальне співвідношення іонів К і Са +Мg, проявляється їхній антагонізм, і скорочення поглинання К рослинами.
Часто вода має надлишок гідрокарбонатів, іонів Nа. СІ, Мg, Б, 7п, Ре. Тільки надлишок Мg не є токсичним; але однаково виникає дисбаланс елементів живлення. Надлишок Са, Mn, Fe, НС03"1 також створює дисбаланс, порушується оптимальне співвідношення цих елементів у робочому розчині. Крім того, надлишок Cl, Mn, S може бути токсичним, тобто дисбаланс і токсичність - результат неконтрольованої кількості цих елементів. До токсичних гідрокарбонатів у воді належать NaHC03 і АІ(НС03)3. Ось чому гідрокарбонати необхідно нейтралізувати частково, а іноді і повністю. При рН розчину добрив рівному 5,5, зазвичай залишається у воді 1 мМо/л НС03, при рН рівному 5 у воді залишається 0,3 мМо/л і менше гідрокарбонатів.
Надлишок Na у робочих розчинах понад 60 мг/л небезпечний для тепличних культур, оскільки поступово нагромаджується у кореневій зоні. Установлено, що концентрація Na+ 30-60 мг/л відчутно знижує інтенсивність росту томата, огірків та інших тепличних рослин. Крім того, Na - антагоніст Са, Mg, К, про що йтиметься нижче.
Нейтралізувати негативну дію підвищеної кількості Na можна, збільшуючи в поживних розчинах і дренажі норми Са, Mg, К та витримуючи співвідношення цих елементів.
Ще одна проблема - це вода з підвищеним вмістом сірки, S - > 60 мг/л (SO„- > 150 мг/л), яка в ґрунтовому розчині посилює засвоюваність рослинами Na і одночасно зменшує засвоюваність Са. Надмірні кількості сірки у воді зменшують попередньою обробкою води активним хлором (Na НОСІ)2, хлорним вапном, рідким хлором. Норма активного хлору має складати 0,6 мг на 1 мг сірки. Такою ж кількістю активного хлору дезактивують надлишок Fe2 і Мп. Попереднє осадження надлишкової кількості сірки у воді можна здійснити, додаючи крейду СаСо3 до води і активно перемішуючи її (фонтанування).
Для визначення якості води при приготуванні робочих розчинів, особливо в регіонах, де використовують воду з підвищеними кількостями у воді Са, Mg, S, Na, СІ, враховують такі показники:
1 ) Показник рН води і робочого розчину. Влітку вода у відкритих водойм має вищу лужність, ніж навесні і восени. Це пов'язано з діяльністю синьо-зелених водоростей і розкладанням гідрокарбонатів на С02 і ОН. Тому влітку необхідно частіше проводити аналіз води з відкритих водойм. Попередня кислотна обробка води в басейнах-нагро- маджувачах улітку до рН = 6 - важливий технологічний прийом підготовки води для ма- лооб'ємного вирощування: при такій кислотності запобігається осадження солей Са і Mg на трубах-магістралях. Твердість води й осадження солей на магістралях краплинного зрошення і крапельницях також пов'язані з надлишком Fe, Mn, A,, Zn, S.
Гідрокарбонати у воді представлені солями карбонової кислоти - Н2С03, котрі дисо- ціюються у воді на Н' і НС03~1. Іони НС03^\ вступаючи в реакцію з іонами металів, що містяться у воді, утворюютьтакі солі: Са (НСО,)„ Mg (HCOJ,, NaHC0o, КНСО„. Це -осно- вні солі за їх кількістю у воді. Крім того, у воді можуть міститися: NH^HCOg, Al (НС03)3, Zn(HC03)2, Cu(HC03)2,MnHC03, із нихтільки№НС03і АІ(НС03)3-токсичні для рослин. Нейтралізація гідрокарбонатів кислотами до рівня 0,5-1 мМо/л - для створення визначеної буферності розчину - бажана при показнику кислотності розчину в межах рН = 5,5-5,3.
Кислотна обробка бікарбонатів призводить до виділення в розчин іонів металів. Засвоєння цих іонів рослинами відбувається при таких співвідношеннях у розчинах, коли їх кількість не викликає антагоністичної взаємодії.
Попереднє хімічне водоочищення також необхідне, коли у воді виявлено значні кількості гідрокарбонатів - 3,5-4 мМо/л і більше (214-244 і > мг/л НС03). Для попереднього хімічного водоочищення можна рекомендувати установку збірної ємності обсягом близько 55 м3 (1 шт. на 1 га), оскільки основне водоспоживання відбувається в літні місяці. Для видалення з води іонів СГ, Fe 2+, S непогано використовувати басей- ни-відстійники великої ємності з аераторними установками, де можна використовувати активний С1. Це - балонний хлор чи гіпохлорит кальцію із вмістом активного хлору від ЗО до 70 %. Активний хлор нейтралізує: H2S - 1 мг на 1 мг Cl, Fe2+ - 1 мг на 0,6 мг СІ, Мп - 1 мг на 0,6 мг СІ.
Дуже ефективна активна аерація води з наступною фільтрацією її через піщано- гравійний фільтр. Після цього необхідно провести аналіз води для визначення рН, ЕС, кількості катіонів і аніонів, для правильного приготування робочих розчинів.
У процесі вирощування рослин необхідно регулярно контролювати кількість макро- і мікроелементів у ґрунтовому розчині, вижимці із субстрату для коригування показників живлення.
Також варто враховувати й інші фактори, що впливають на засвоєння елементів живлення та темпи росту і розвитку рослин.
Часто засвоєння пов'язане із несприятливими для культур кліматичними умовами: занадто низькою чи занадто високою температурою, інтенсивністю світла, агротехнічними умовами, зокрема, недостатнім чи надмірним водопостачанням, неналежними добривами чи використанням для зрошення води поганої якості. Нестача живлення (фактична відсутність, незасвоєння, неналежна реакція ґрунтового розчину), надлишок елементів живлення, нерозвинена коренева система, неправильне зрошення, високі концентрації катіонів і аніонів, особливо ІЧа і СІ також негативно впливають на засвоєння елементів живлення рослинами.
Ознаки порушення нормального росту і розвитку рослин зазвичай виявляються на всій рослині, але найчастіше це спостерігається на листках і плодах в овочевих культур, на листках і квітках у квіткових культур. На листі відбувається зміна забарвлення, їх деформація, зменшення розмірів, плямистість і некроз, що призводить до часткового чи повного засихання, пожовтіння, побуріння країв листкових пластинок, деформації квіток і суцвіть; некротичне розтріскування, плями на плодах томатів, огірків та інших тепличних культур.
Ознаки нестачі поживних речовин можуть з'являтися і на різних частинах рослин: на молодих і старих листках, точках росту. Ці ознаки на молодих листках і конусах росту частіше інформують про нестачу В, Са, Си, їїе, Мп, тобто - кальцію і мікроелементів, а на старих листках - N1, Мg, К, S, Мо. При використанні повноцінних за складом поживних розчинів різні плямистості, некрози, хлорози свідчать про неможливість їхнього засвоєння - це - реакція рослин на низьку чи високу температуру субстрату, слабкий розвиток кореневої системи, або ж - про фітотоксичність хімічних засобів чи захисту живлення. Пожовтіння нижніх листків томатів (коли головна жилка листка зелена) - звичайний прояв нестачі магнію, що може бути пов'язана з умовами підвищеної потреби рослин (але не тільки!) у магнії, недостатньою освітленістю, неправильним (зазвичай недостатнім) зрошенням, високою нічною температурою, недостатньою аерацією, надміром калію (антагоніста магнію). При антагонізмі між калієм і магнієм трапляється не тільки магнієвий хлороз, а й листя обпадає без зовнішніх ознак хлорозу, наприклад, на трояндах. А в томатів на наймолодших листках темно-зелене забарвлення - ознака надлишку азоту і нестачі йоду, світло-зелене - нестачі азоту. Побуріння і відмирання верхівкових листків у томатів виникає через нестачу фосфору.
Антоціановий відтінок нижньої частини листа томатів, троянд - ознака нестачі фосфору через занадто низьку температуру субстрату, надлишку азоту чи сірки, слабкої кореневої системи, занадто високого (рН понад 6,2) показника кислотності ґрунтового розчину. Плямистість листків і всихання їхніх країв відбувається при нестачі калію. Скручування молодих листків томатів та інших культур пов'язане із нестачею марганцю й міді, високим показником рН ґрунтового розчину (лужна реакція замість звичайної з рН 5,3-5,8). Зміна конуса росту пов'язана з нестачею кальцію і бору при зависокому показникові рН ґрунтового розчину - понад 6,5.
Тепличні рослини відзначаються дуже різною здатністю поглинання і засвоєння азоту і калію. У томатів гірше надходить фосфор до рослин. Часто ситуацію не виправляє підвищення доз фосфору, швидше вона поліпшується при збалансованій кількості N. Р, К, Са, Мg у ґрунтовому розчині і кислотності на рівні рН 5-6. У томатів поглинання Са і Мg протягом вегетації зазвичай рівномірне, а споживання N систематично зростає до пори найінтенсивнішого плодоношення. Недостатнє живлення призводить до порушень росту: нестача N - до повільного росту коренів, К - до зниження життєздатності рослин, Мg - до несприятливих фізіологічних змін, Са - до слабкої кореневої системи і тонких відростків, Ре - до затримки росту, В - до розтріскування листків, крихкості пагонів, скидання зав'язей. Надмірне живлення також впливає негативно, посилюється антагонізм між засвоєнням рослинами іонів. Це спричиняє нерівномірне споживання іонів і їхнє нагромадження в ґрунтовому розчині.
Необхідний не тільки постійний моніторинг елементів живлення в ґрунтовому розчині й ґрунті (субстраті), а й підтримка необхідних рівнів і співвідношення елементів живлення. Останнє досягається короткочасним коригуванням поживного розчину, більш широким використанням дренажу.
Розглянемо взаємодію між елементами живлення в ґрунтовому розчині і їх доступності для рослин, залежно від вмісту елементів, факторів рН, ЕС, мікроклімату.
Показник кислотності ґрунтового розчину необхідно постійно контролювати і коригувати через значний вплив рН на доступність багатьох елементів живлення. При збільшенні показника рН вище оптимального - у межах 5,1 -5,9 - знижується доступність таких елементів, як Р, В, Си, Ре, Мп, Ти, а в кислому середовищі - доступність Мо. Часто причиною неправильного чи недостатнього живлення є не нестача елементів живлення у субстратному розчині, а неможливість їх поглинання при лужній реакції ґрунтового розчину, використанні води з лужною реакцією, високому вмісті у ній № і СІ. При рН ґрунтового розчину вищому 7,0 у ґрунтовій культурі мікроелементи і Р стають менш до-ступними, а макроелементи — К, Б - поглинаються в надмірних кількостях.
На супіщаних, легко- і середньосуглинкових ґрунтах через низький рівень поглинаючого комплексу проводять при необхідності вапнування - до рівня рН 5,5-6. На суглинкових і глинистих ґрунтах з малим вмістом гумусу вапнувати ґрунт можна до показника рН 6,5. Вміст легкодоступного Са в ґрунті має складати не менше 1500-2000 мг/л у кислотній витяжці. Не можна допускати перевапнування, що також зменшує доступність мікроелементів. З ростом рН від 5,5 до 6,7 концентрація доступного фосфору швидко знижується, зокрема, вміст Р в листках падає до ЗО % від норми. Також знижується вміст у листках В, Си, Мп, Ти. У залежності від використовуваного субстрату показник рН субстрату і ґрунтового розчину варто підтримувати у межах 5,1-5,9.
Для регулювання рівня рН>6, сіль КН^О,, у робочому розчині заміняють на ортофосфорну кислоту. Низький показник рН<5 спостерігається при використанні великої кількості амонію (фосфат амонію, аміачна селітра). У цьому разі рН робочого розчину підвищують до рН=6, а вміст ІМН^ у розчині дають не більше 10 мг/л. Також варто зменшити дозу К, зменшують разову дозу краплинного зрошення до 70 мол. При високому рН трохи збільшують дозу І\ІН4 - до 20 мг/л, норму Ре збільшують до 2-2,5 мг/л розчину.
При використанні малооб'ємних субстратів застосовують систематичне і багаторазове протягом дня зрошення рослин розчином мінеральних добрив відповідної концентрації. У залежності від виду рослин, а в межах культури - від виду вирощування і складу поживного розчину - використовують певний рівень загальної концентрації солей. Останнє пов'язане із здатністю культури засвоювати з ґрунтового розчину воду й елементи живлення (солестійкість).
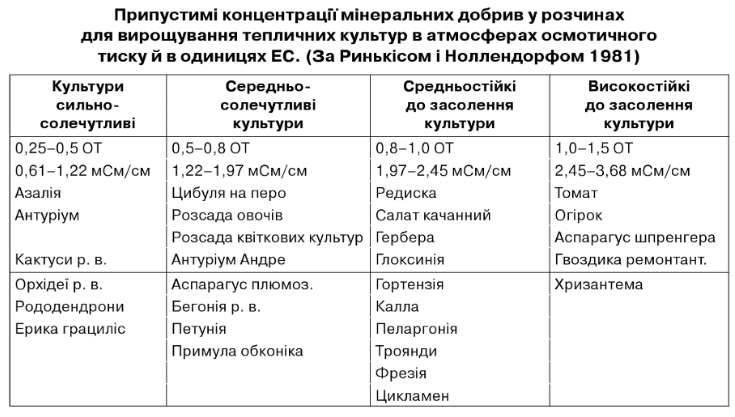
Раніш солестійкість рослин оцінювали в атмосферах осмотичного тиску (ОТ) і враховували здатність кореневої системи поглинати з ґрунтового розчину елементи живлення при визначеній гранично припустимій засоленості субстрату. Нині в практиці тепличного рослинництва оперують поняттям електропровідності робочого і ґрунтового розчинів з показником у мілісименсах на 1 см (тБіп/зт, мСм/см). існують рекомендації з середнім показником для різних культур.
Оптимальні концентрації солей у робочих розчинах варіюють за фазами росту і розвитку культур, за рівнями температури й освітленості, плодового навантаження. Але, виходячи із стійкості до засолення ґрунтового розчину, завжди потрібно контролювати і коригувати його.
Таблиця 7.2
У томата при малооб'ємному вирощуванні оптимальними показниками рН і ЕС у період вегетації є такі:
- просочення матове: зниження рН у дренажі до 4,8-5;
ЕС поживного розчину близько 2,8 мСм/см;
- установка рослин на мати: рН поживного розчину 5,5;
ЕС поживного розчину-2,7 мСм/см, одноразова доза зрошення - близько 200 мол розчину на одну рослину;
- установка рослин в отвори для укорінення: рН поживного розчину 5,5, ЕС поживного розчину близько 2,6 мСм/см;
-цвітіння 1-3 китиці: рН поживного розчину 5,5, ЕС поживного розчину2,8-3 мСм/см, водоспоживання - 0,8-1,2 л/рослина;
- цвітіння 4-5 китиці: рН - 5,5-5,8, ЕС - 2,6-2,8 мСм/см, водоспоживання 1,2- 1,8 л/рослина;
- масове плодоношення: рН - 5,5-5,8, ЕС - 2,5-2,6 мСм/см, водоспоживання 1,8- 2,5 л/рослина і більше;
- осінній період: рН - 5,5, ЕС - 2,7-2,8 мСм/см.
Для кожної культури за періодами вирощування визначені оптимальні показники ЕС. У період вирощування не допускають рН у дренажі вище від 6,2, для чого можна використовувати ортофосфорну кислоту в кількості норми Р в розчині. На піку плодоношення томатів ЕС розчину може бути на рівні 2,8-4,2 мСм/см. Але не можна допускати нагромадження солей у матах, при якому доступність катіонів і аніонів різко знижується, відбувається ушкодження кореневих волосків. Допустиме перевищення показника ЕС у ґрунтовому розчині на 0,5 мСм/см у порівнянні з подаваним робочим розчином. Варто збільшити норму дренажу і трохи знизити показник ЕС робочого розчину. У літні місяці норму ЕС можна знизити до 3,2 мСм/см.
Не можна допускати рН дренажу нижче від 5. Варто зменшити кількість ІМН4 у робочому розчині до 7-10 мг/л, зменшити дозу К, рН робочого розчину підвищити до 6, за рахунок зменшення кількості кислоти при підлужуванні розчину - збільшити кількість І\ІН4 тимчасово до 20-25 мг/л, збільшити норму хелата заліза на 20 %, але не більше 2 мг/л.
Нормування живлення рослин при малооб'ємній технології базується на агрохімічному моніторингу дренажу, вижимки із субстрату, субстрату, у рослинному матеріалі (листкова діагностика). При проведенні аналізу ґрунту в теплицях одна змішана проба береться з площі не більше 400 кв. м., відбираючи по одній окремій пробі з кожних 100 кв. м. При малооб'ємному вирощуванні у процесі інтенсивного зростання чи масового достигання концентрація елементів живлення швидко змінюється через їх поглинання, вимивання із дренажем, сорбцією тощо. Тому повний агрохімічний аналіз проводять кожні 3-4 тижні, у період інтенсивного зростання - кожні 2 тижні, показники рН і ЕС визначають 2-3 рази на тиждень.
Найбільш інтенсивне поглинання води і мінеральних добрив із ґрунтового розчину відбувається при початкових показниках концентрації солей у ґрунтовому розчині і постійно знижується при його максимальних показниках. Тому в програму оптимізації живлення входить використання добрив і води, які найменше засолюють ґрунтовий розчин.
Кількість азоту необхідно постійно контролювати, роздільно нітратного й аміачного азоту в ґрунтовому розчині (дренажі). Надлишок азоту сприяє надмірному розвитку вегетативної маси, рихлості рослин, ослабленню і запізненню одержання продукції, зав'язуванню плодів в овочевих рослин. Надмірна кількість азоту порівняно легко видаляється промиванням субстрату, правильним нормуванням дренажу.
У процесі вирощування різних культур необхідно контролювати й рівні співвідношення різних катіонів і аніонів у робочих і особливо ґрунтових розчинах. Коригування робочих розчинів має підтримувати кількість катіонів і аніонів в однакових кількостях.
При вирощуванні певної культури, насамперед, необхідно стежити за співвідношенням - азотжалій у ґрунтовому розчині (вижимка із субстрату, дренаж на початку його виділення), щоб підтримувати потрібне співвідношення. У молодих рослин до по-чатку зав'язування плодів чи бутонізації підтримують співвідношення ІМ:К=1: 1-1,2. У міру росту плодового навантаження, наприклад, у томатів, співвідношення поступово змінюється ІЧ:К < 1-1,2 до 1,5, потім до 1,8, іноді вище - до 3.
Дефіцит магнію спостерігається на різнихтепличних рослинах, але частіше трапляється у томатів при високих рівнях N і К. Низький рівень азоту при вапнуванні субстрату частіше виявляється в ґрунтовій культурі. Середній рівень N у цьому разі кращий. При низьких рівнях К при середній і високій кількості азоту в ґрунтовому розчині порушується дозрівання томатів. В умовах низької освітленості кількість пустотілих плодів збіль-шується при надмірному застосуванні фосфору і знижується при високих рівнях калію. Підвищення рівня азоту знижує вміст у листках калію, хоча він може міститися у ґрунтовому розчині в помірній кількості. Збільшення кількості К в розчині знижує споживання магнію через антагонізм незбалансованих кількостей К та Мg. Тому при малооб'ємній культурі томата застосовують такі співвідношення КІ:К до утворення першого суцвіття - 1:1,1; від однієї до трьох кистей - 1:1,3; від 3-й до 5-ї китиці - 1:1.5, у період плодоношення - 1:1,8. При поганому освітленні навесні і восени підтримують більш високий рівень Мg. Підвищена кількість магнію в ґрунтовому розчині не позначається негативно на рості рослин. При підвищеній кількості фосфору в ґрунтовому розчині - вище норми - стримується надходження магнію в рослину, його місце займає калій. Наприклад, на чутливих сортах троянд у цьому разі обпадає листя. Високі концентрації амонійного азоту (норма до 10-14 мг/л) знижують надходження із ґрунтового розчину в рослини Са і Мg. При надмірному підвищенні кількості N8 і СІ в ґрунтовому розчині також збіль-шується надходження в рослини фосфору, калію, знижується вміст Са. З іншого боку, якщо багато хлоридів у ґрунтовому розчині, то збільшення кількості азоту помітно знижує надходження хлору в листя. Підвищені дози фосфору в ґрунтовому розчині знижують надходження Мп, у листки. Зрослі кількості Мп у ґрунтовому розчині потребують підвищення кількості внесеного заліза, щоб співвідношення Ре:Мп = 2-5: І. У культур з підвищеним споживанням заліза (троянди, гербери) його кількість підвищують до 2,5 мг/л розчину, одночасно знижуючи кількість Мп до 0,2-0,3 мг/л. У томата деякі сорти вимагають до 0,7 мг/л Мп, у такому разі кількість Ие також варто підвищити до 2 мг/л. Варто враховувати, що високі рівні Мg, Со, у ґрунтовому розчині знижують надходження Ие у рослини. Постійний контроль вмісту макро- і мікроелементів у ґрунтовому розчині - шлях до оптимізації умов вирощування високоврожайних рослин.
Інтенсивність засвоєння елементів живлення з ґрунтового розчину залежить і від таких факторів, як температура й освітленість, вологість повітря і субстрату.
Низькі температури субстрату і повітря стримують ріст рослин і поглинання поживних елементів. Хоча збільшення рівня азоту в ґрунтовому розчині до 220 мг/л при температурі в кореневій зоні 22-27 °С збільшує сиру вагу плодів томата при постійній оптимальній температурі повітря в 20-25 °С, більш високі дози азоту в кореневій зоні не дають приросту врожаю. При температурі субстрату 13 °С і вищій вага рослин збільшується при вищевказаному рівні N. при нижчій від 13 °С високі дози азоту не впливають позитивно. В міру підвищення температури необхідно збільшувати кількість азоту, але не більше 220 мг/л. Якщо температура зростає, а рівень азоту низький, у томатів спо-стерігається скидання квіток. Низька температура субстрату (8 °С і нижча) не сприяє транспортуванню N і К в надземну частину рослин, веде до нагромадження їх у кореневій системі. Ріст рослин сповільнюється. При 10-13 °С у зоні коренів сповільнюється надходження фосфору в рослину. Надходження К, Са, Мg знижується при температурі 13 °С в зоні коренів, а при підвищенні температури в кореневій зоні збільшується надходження в листи Р, К, Мg, Си, Ре, Мп. Пристрої підсубстратного обігріву дозволяють трохи знижувати температуру повітря в теплиці, заощаджуючи енергетичні витрати. Ця система - "теплі ноги і холодна голова" - застосовується при недостатньому рівні обігріву теплиці з технічних чи інших причин. З іншого боку, високі температури повітря вночі (21 °С і вищі) збільшують надходження Са, № в листя, але зменшують у них вміст фосфору.
Застосування екранів для захисту теплиць від перегріву влітку може дати сильне затінення (до 65 %), що призводить до зниження поглинання ЇМ, Р, К, Са, Мg, за умови, що азотне живлення на 90-95 % ведеться за рахунок ІМ03. Досвічування рослин в осін- ньо-зимово-весняний період збільшує поглинання ЇМ, К, Са, Мg, Мп. Дуже важливоу цей час підтримувати збалансований рівень К в субстратному розчині.
Тривале штучне освітлення в умовах зимових коротких днів при високому вмісті кальцію в ґрунтовому розчині призводить до зниження сухої ваги рослин, а в міру подовження дня навесні збільшується нагромадження сухої речовини.
Поглинання N і К зростає від низького рівня вночі до максимального вдень, знову знижуючись протягом вечора і ночі. Тому брати пробу ґрунтового розчину на аналіз краще о 13-14 годині дня. Поглинання N і К тісно пов'язане не тільки з рівнем освітлення і температурою повітря, а і з збільшенням кількості споживаної води.
Вологість повітря - також важливий фактор засвоєння із ґрунтового розчину катіонів і аніонів. Вміст Са в молодих листках при відносній вологості повітря 95 % значно нижчий, ніж при 50 %, оскільки кальцій, що надходить, перебуває в транспіраційному потоці.
Прояв верхової гнилизни томатів посилюється навіть при низькій вологості, при високому рівні ЕС ґрунтового розчину. Крім того, підвищена висока вологість уночі сприяє руху Са до молодих листків і плодів, а при низькій вологості протягом дня призводить до нагромадження Са в зрілих листках. У сортів і рослин з високою стійкістю до верхової гнилизни плодів спостерігається більш інтенсивне засвоєння К. У чутливих до верхової гни- лизни сортів спостерігається нестача К, а також значне нагромадження Са в листках, а не в плодах. Нестача Са пов'язана і з іншими іонами-антагоністами з ґрунтового розчину.
Велика кількість № у ґрунтовому розчині при підвищених дозах сірки знижує надходження Са. У такій ситуації варто підвищувати кількість Са в ґрунтовому розчині, регулюючи одночасне співвідношення К:Са.
Надлишок К стримує надходження Са, так само, як ІМН^. При кількості ІМН^ у ґрунтовому розчині понад 10 мг/л блокується надходження Са. Одночасно такий рівень ІМН,, ушкоджує кореневі волоски, особливо в зимово-весняний та осінній періоди. При появі перших ознак верхової гнилизни на початку наливу плодів томатів співвідношення К:Са підтримують на рівні 0,8-1,5:1. Для поліпшення смакових якостей томатів при підвищених кількостях К в ґрунтовому розчині необхідно, у свою чергу, підвищити концентрації Са до певного співвідношення К:Са.
На молодих листках рослин при нестачі Са з'являється жовтизна, а краї листків стають бурими, точка росту може відмерти, а плоди стають чорними навколо рубця (початок верхової гнилизни). Верхова гнилизна часто виникає через низьку вологість, засоленість субстрату, порушення водопостачання рослин томата. При перших ознаках нестачі Са у рослинах варто провести кілька обприскувань раз на 4-5 днів 0,4-0,5 % розчином Са(І403)2. При появі верхової гнилизни обприскують ретельніше - наносять розчин по всій поверхні рослини. Одночасно збільшують норму Са(МОд)2 у поживному розчині: кількість Са у субстратному розчині може в 10 разів перевершувати нормальний вміст Мg.
Перші ознаки нестачі Мg проявляються на старих листках у вигляді світлих мармурових плям, знебарвленням листків між прожилками, хоча головна і бічна прожилки залишаються зеленими. При тривалому магнієвому голодуванні може припинитися ріст плодів. Тож при нестачі магнію проводять кожні 5-7 днів обприскування рослин 0,5- 0,7 % розчином сульфату магнію чи магнієвої селітри. На сортах із підвищеною чутливістю до нестачі Мg позакореневі підживлення практикують один раз на тиждень, профілактично починаючи їх від зав'язування плодів на 4-й китиці. Прояв хлорозу посилює плодове навантаження. Необхідно стежити за співвідношенням К:Мg, оскільки високий рівень К стримує поглинання Мg, тож норми Мg підвищують.
Для регулювання співвідношення К:Са для посилення вегетативного чи генеративного розвитку томатів та інших культур застосовують зміни співвідношення Са:К=1:1,2- 1 до 7-10 днів. Для генеративного розвитку використовують співвідношення Са:К= 1,2-1 при концентрації катіонів близько 235 мг/л К і 200 мг/л Са. Для посилення вегетативного розвитку оптимальне співвідношення - 1:1,6-1,7 при концентрації катіонів близько 235 мг/л К та 320-400 мг/л Са. Крім зазначених співвідношень К:Са, необхідно підтримувати відповідний рівень відносної вологості повітря для кращої транспірації.
Засвоєння фосфору в оптимальній постійній кількості до 40-45 мг/л робочого розчину й у ґрунтовому розчині до 50 мг/л у томатів стимулює засвоєння Са. Крім оптимальної кількості фосфору і кальцію, необхідний показник рН розчину від 5 до 5,9. Одночасно треба стежити, щоб фосфор не накопичувався у більших концентраціях, що гальмує надходження Мg і викликає магнієвий хлороз. Якщо показник рН > 6,2-6,7, то Р стає важкодоступним.
Наявність у ґрунтовому розчині СІ в кількості 1-3 мМо/л, тобто 30-90 мг/л і максимально до 150 мг/л, сприяє засвоєнню Са. Так само посилюється засвоєння Са й інших елементів живлення при оптимальному показнику ЕС ґрунтового розчину до 2,6-2,8 мСм/см і при максимально припустимому в період плодоношення томатів - до 3,5 мСм/см, чи трохи більшому.
Мікроелементи. Відхилення рН у бік кислоти призводить до підвищення розчинності сполук Мп, Ре, АІ, що містяться в ґрунті. Високі концентрації цих іонів можуть зашкодити кореневій системі. При значному підвищенні рН Ре, Мп, Си утворюють нерозчинні сполуки - гідрооксиди, які не засвоюються кореневою системою. В такому разі замість сірчанокислих солей краще застосувати хелати - органічні сполуки, доступні для рослин. На лужних ґрунтах також різко знижується розчинність бору. Тому тривале зрошення водою з рН вищим 7 призводить до підлужування ґрунтів і знижує доступність внесених мікроелементів.
При надміру фосфору (зафосфачування ґрунтів) Zn і Fe вступають у реакцію з фосфором і утворюють погано розчинні фосфати цих елементів, які випадають в осад. Оскільки Zn є антагоністом Fe, при підвищеній кількості Zn норму заліза збільшують до 2-2,5 мг/л робочого розчину.
При малооб'ємному вирощуванні доступність іонів мікроелементів у прикореневому шарі визначається за тими ж факторами, що і при вирощуванні на ґрунтах. Важливою є підтримка всіх поживних речовин у розчинному стані за рахунок внесення у хелатах таких елементів, як Fe, Zn, Cu, Мп. Оскільки хелати більш доступні для рослин, їх витрата невелика в порівнянні із сірчанокислими солями, які ще часто рекомендують до застосування.
З огляду на високу стабільність Fe - ДТРА при рН від 1,5 до 7 у робочих розчинах (у тому числі й концентрованих) його переважно використовують як основний хелат заліза, у порівнянні з хелатом Fe - ЕДТА, ефективним при рН нижчим 6, тобто робочі розчини повинні мати рН нижче 6, наприклад, рН 5,5.
При використанні поліхелатів у формі ЕДТА необхідно підтримувати показник рН у ґрунтовому (дренажному) розчині на рівні нижче від рН=6, інакше норму Fe - ДТРА треба підвищувати на 0,4-0,5 мг/л з урахуванням внесеного Fe - ЕДТА разом з іншими поліхелатами ЕДТА, котрі стабільні при рН 3,5-10.
7.3. Вимоги до якості води для краплинного зрошення, методика коригування поживного розчину залежно від хімічного складу води
Хімічний склад води, краплинне зрошення, макро- і мікроелементи, забруднюючі
речовини, мінералізація води, коригування, маточний і робочий розчини кислот,
поживні розчини, розведення, розрахунки
При використанні краплинного зрошення якість води є одним із основних факторів, що забезпечують успіх тепличного виробництва. Тому так важливо знати хімічний склад використовуваної в господарстві води. Це необхідно як для розрахунку вмісту солей і кислоту поживному розчині, так і при його корекції. У кожному тепличному комбінаті використовувана поливна вода має певний хімічний склад, і придатність конкретної води варто враховувати ще на стадії проектування систем краплинного зрошення.
Різна за походженням вода - це складний розчин, що містить усі відомі хімічні елементи у вигляді простих і складних іонів, комплексних сполук, розчинених чи газоподібних молекул, стабільних і радіоактивних ізотопів, а також певний набір бактерій.
Її склад визначається наявністю великої кількості хімічних елементів, різним вмістом і розмаїтістю форм кожного з них.
У воді визначають 6 основних груп хімічних компонентів:
1 ) головні іони (макроелементи) К Na+, Mg2+, Са2+, CI \ S042 , НС03 \ CO,,-;
2) розчинені гази - кисень, азот, сірководень, вуглекислота;
3) біогенні елементи - сполуки N, Р, Fe, Si;
4) органічні речовини - органічні кислоти, складні ефіри, феноли, гумусові речовини;
5) мікроелементи;
6) забруднюючі речовини.
Сумарний вміст мінеральних речовин називається мінералізацією води, що виражається в мг/дм3, г/дм3, г/кг, % (проміле (від лат. Pro mille - за тисячу) - тисячна частка, позначається - %).
За ступенем мінералізації вода буває прісною до 1 %, солонуватою (1-25 %), солоною (25-50 %), дуже солоною (понад 50 %). Для краплинного зрошення краще використовувати воду із вмістом мінеральних речовин до 0,5-1 %.
Підвищене надходження солей із поливною водою призводить до засолення субстратів, що негативно позначається на продуктивності рослин. Томати більш солестійкі, ніж огірки, але на засолених субстратах сильніше уражаються верховою гнилизною.
Хімічний склад води для приготування поживних розчинів не повинен перевищувати значень показників, зазначених в таблиці 7.4.
На основі хімічного складу води проводиться корекція поживного розчину. Існує правило, за яким концентрація елементів у поливній воді не повинна перевищувати їхній вміст у стандартних поживних розчинах. Особливо це стосується мікроелементів, тому що вирощування рослин в обмеженому кореневому об'ємі може призвести до їх нагромадження й отруєння рослин чи до антагонізму елементів.
Поживний розчин обов'язково коригується на вміст наявних у воді К, Са, Мg, БОR, М03 . Реакція його доводится до оптимального рівня рН, що для більшості культур складає 5,5-6,0. Оскільки вода найчастіше слаболужна чи лужна, для зниження рН використовують ортофосфорну (Н3Р04) чи азотну (НМ03) кислоти.
Кількість кислоти розраховується за вмістом бікарбонатів (НС03 ). У принципі, на 1 мМоль НС03 у воді потрібен 1 мМоль кислоти. Однак у нейтралізації беруть участь не всі бікарбонати, тому для забезпечення буферності розчину залишають 1 мМоль НС03 = 61 мгбез нейтралізації 0,5-1 мМоль/л.
Кислоти і бікарбонати взаємодіють в еквівалентних кількостях:
1 мМ0 НС03 = 61 мг/л
1 мМ0 Н3Р04 = 98 мг/л
1 мМ0 нКі03 = 63 мг/л
НЗРО„ + НС03- = Н2РО„- + Н20 + С02,
НІ403 + НС03: = N03- + н2о + со2
У практиці використовують розведені кислоти і відповідно витрачають їх розчини у більшій кількості. Для розрахунку необхідної кількості кислоти можна використовувати такі формули:
Для ортофосфорної кислоти:
Дата добавления: 2016-12-26; просмотров: 1206;
