Химиялық реакциялардың кинетикалық жіктелуі
Химиялық реакциялар молекулалардың санына және реакциялардың ретіне байланысты жіктеледі.
Бір мезгілде әрекеттесетін молекулалардың санына баланысты реакциялар моно-, би- және үшмолекулалық болып бөлінеді.
Реакцияның реті кинетикалық теңдеу бойынша әрекеттесуші заттардың концентрацияларының дәреже көрсеткіштерінің қосындысымен анықталады. Химиялық реакциялар нөлінші, бірінші, екінші және үшінші ретті болып бөлінеді.
Нөлінші ретті реакцияның жылдамдығы тұрақты болады, яғни 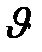 = K (const).
= K (const).
Мысалы:
С6H12O6(к) → 2C2H5OH + 2CO2
Бұл реакция моно молекулалық және нөлінші ретті болып есептеледі (V = K), себебі химиялық кинетиканың негізгі заңы бойынша қатты заттың концентрациясы өзгермейтіндіктен есепке алынбайды.
C12H22O11(c) + H2O → C6H12O6 + C6H12O6
Реакция бимолекулалық және бірінші ретті, себебі 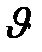 = K[C12H22O11]. Судың концентрациясы өте аз мөлшерде өзгеретін болғандықтан есепке алынбайды.
= K[C12H22O11]. Судың концентрациясы өте аз мөлшерде өзгеретін болғандықтан есепке алынбайды.
С6H12O6(c) + C6H22O6(c) → C12H22O11 + H2O
реакция би молекулалық және екінші ретті, себебі:
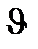 = K [С6H12O6] [C6H12O6]
= K [С6H12O6] [C6H12O6]
Үш молекулалық және үшінші ретті реакцияға мына процесті жатқызуға болады:
2 NO(г) + О2(г) → 2NO2(г)
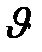 = K [NO]2[O2]
= K [NO]2[O2]
Дата добавления: 2016-12-16; просмотров: 4334;
