Способи добування оксикислот
Способи добування: гідроліз a-галогензаміщених карбонових кислот; гідратація ненасичених кислот; ціангідринний синтез; окиснення діолів; відновлення оксокислот тощо.
4. Фізичні властивості гідроксикислот
Уявлення про поляризацію світла, площину поляризації, величину кута обертання. Схема будови поляриметра. Питоме обертання. Молярне обертання.
Оптична активність - здатність речовин обертати площину поляризації променю поляризованого світла. Речовини, які мають такі властивості є оптично-активними речовинами.
Здатність обертання площини поляризації світла пов’язана з асиметрією в просторовій будові молекул оптично активних речовин. Якщо в молекулі речовини є хоч один атом Карбону, який з’єднаний із чотирма різними атомами або групами, то такі молекули асиметричні, тобто не мають площини симетрії. Це є причиною оптичної активності речовин.
Атоми Карбону, з’єднані з чотирма різними атомами або групами атомів називають асиметричними (хіральними) атомами Карбону. Асиметричний атом Карбону в формулі молекули позначається зірочкою.
Уявлення про оптичні ізомери, рацемічну суміш. Оптичні ізомери відрізняються різним розташуванням атомів або груп атомів у просторі навколо асиметричного атому Карбону. Їх кількість (N) дорівнює  , де n- кількість асиметричних атомів Карбону в молекулі.
, де n- кількість асиметричних атомів Карбону в молекулі.
Оптичні антиподи - це оптичні ізомери, які подібні між собою як предмет і його дзеркальне відображення. Їх ще називають дзеркальними ізомерами або енантіомерами. Енантіомери виявляють однакові фізичні, хімічні властивості, але різну фізіологічну дію.
Для просторового відображення оптичних ізомерів, крім тетраедричних моделей, широко використовуються проекційні формули Фішера:

| 
|
Розглянемо оптичні ізомери на прикладі молочної кислоти:
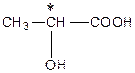
|
Між кількістю асиметричних атомів Карбону в молекулі (n)і кількістю оптичних ізомерів (N) існує певна залежність:  .
.
У молочній кислоті один асиметричний атом Карбону, тому її молекула існує у вигляді двох оптичних ізомерів:

| 
|
Ці ізомери обертають площину поляризованого світла на один і той же кут, але один ліворуч (-), а другий праворуч (+).
Суміш однакової кількості ліво- і правообертаючих ізомерів — рацемічна суміш, або рацемат, оптично неактивна і позначається dl або r.
Оптичні ізомери розрізняють не тільки за напрямком обертання, але й за конфігурацією, тобто за розташуванням замісників навколо останнього асиметричного атому Карбону, відносячи їх до D- або L-ряду. Оптично активні сполуки, в молекулах яких гідроксогрупа –OH біля останнього асиметричного атому Карбону розміщується праворуч, відносять до D-ряду, і відповідно, речовини, в молекулах яких вона розміщена ліворуч — до L-ряду.
5. Хімічні властивості гідроксикислот
Хімічні властивості гідроксикислот обумовлені наявністю карбоксильної та гідроксильної груп. Також характерні реакції, що обумовлені взаємний впливом цих функціональних груп.
Специфічні реакції оксикислот
До таких реакцій, які дозволяють розрізняти a-, b-, g-, d-оксикислоти, відносяться реакції, що перебігають із виділенням води в умовах нагрівання.
a-Оксикислоти за умов нагрівання, втрачаючи дві молекули води, утворюють міжмолекулярні циклічні естери - лактиди.
b-Оксикислоти дуже легко відщеплюють воду, утворюючи етиленовий зв’язок (a-, b-ненасичені кислоти).
g- і d-оксикислоти відщеплюють воду від однієї молекули кислоти і утворюють сполуки, які називають лактонами.
Характерною реакцією тільки для a-оксикислот є розклад їх за умов нагрівання з мінеральними кислотами:

|
У результаті утворюється альдегід (або кетон) і мурашина кислота.
6. Окремі представники
Гліколева (оксиоцтова), молочна (a-оксипропіонова), b-оксимасляна, рицинолева кислоти. Яблучна, винна кислоти. Реактив Фелінга. Лимонна кислота і її розклад за умов нагрівання в присутності сульфатної кислоти. Мигдальна кислота.
Фенолокислоти — похідні ароматичних кислот, в яких атом Гідрогену в бензольному ядрі заміщено на гідроксогрупу.
Найпростішим представником є орто-оксибензойна або саліцилова кислота. Саліцилова кислота за умов швидкого нагрівання може декарбоксилуватися (реакція, зворотна добуванню), з 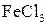 дає фіолетове забарвлення (як феноли). Саліцилова кислота виявляє антисептичні (консервуючі), протиревматичні та жарознижуючі властивості. Подібні властивості характерні і похідним саліцилової кислоти: натрій саліцилату (сіль), ацетилсаліциловій кислоті (естер)— аспірину. Саліцилову кислоту добувають дією
дає фіолетове забарвлення (як феноли). Саліцилова кислота виявляє антисептичні (консервуючі), протиревматичні та жарознижуючі властивості. Подібні властивості характерні і похідним саліцилової кислоти: натрій саліцилату (сіль), ацетилсаліциловій кислоті (естер)— аспірину. Саліцилову кислоту добувають дією 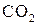 на сухий натрій фенолят за умов нагрівання під тиском (синтез Кольбе):
на сухий натрій фенолят за умов нагрівання під тиском (синтез Кольбе):

|
Галова кислота. Танін, уявлення про дубільні речовини.
Література: [2] с. 13 - 33; [3] с. 420 - 432
Дата добавления: 2016-12-16; просмотров: 1108;
