Витамины молока и их биологическая роль
Витамины – это сложные органические соединения, необходимые для нормального функционирования организма. Часть витаминов образуется в организме из провитаминов. Провитамины – это органические соединения, которые в результате ферментативных реакций или энергетических воздействий переходят в витамины. Например, витамин А образуется из провитамина – β-каротина.
По признаку растворимости в жирах или в воде витамины делятся на две группы: жирорастворимые и водорастворимые. Содержание витаминов в молоке выражают либо в международных единицах МЕ), либо в микрограммах или миллиграммах на 100 г молока. За международную единицу принято количество витамина, проявляющее определенное биологическое действие. В молоке содержатся все жизненно необходимые витамины. Их содержание не постоянно и зависит от кормовых рационов, активности микрофлоры рубца коров, стадии лактации, состояния здоровья и др.
Роль витаминов в молоке и молочных продуктах заключается в их влиянии на окислительно-восстановительные процессы (витамины группы Е, С), стимулировании роста молочнокислых бактерий (витамины В1, В2, В3, Н), участии в составе коферментов в ферментативных процессах (В1, В2, В3, В6, РР, Н). Кроме этого, каротиноиды и витамин В2 являются природными красителями молочных продуктов. Содержание витаминов меняется в процессе хранения молока: окисление витаминов А, Е, С, В1 и снижение их содержания, частичное разрушение при световом воздействии, особенно УФ-лучей (витамины А, В2, В6, С, Е, РР), потери при тепловых воздействиях (В1, С).
К жирорастворимым витаминам молока относятся витамины групп А, Д, Е, в незначительном количестве витамин К и витамин F. Из всей группы витаминов А в молоке преобладает ретинол – витамин А1, который в основном образуется из β-каротина кормов. Витамин А1 и β-каротин обусловливают желтую окраску сливочного масла и повышают устойчивость молочного жира к окислению. Витамин А1 участвует в регулировании секреторных функций поджелудочной, потовых и сальных желез,. А также в комплексе с белком участвует в возникновении зрительного ощущения (в процессах фоторецепции). Содержание витамина А1 вместе с β-каротином от 50 до 100 мкг в 100 см3 молока.
Из витаминов группы Д в молоке преобладает Д3 – холекальциферол. В организме регулирует обмен кальция и фосфора. Молоко содержит сравнительно мало витамина Д3 – от 0,03 до 0,2 мкг в 100 см3.
Витамин Е – это группа соединений токоферолов (α- ,β-, γ- и др). В молоке главным образом содержится α-токоферол (от 0,02 до 0,35 мкг в 100 г молока). В молоке и молочных продуктах выполняет роль активного естественного антиокислителя липидов, витамина А и β-каротина, в организме участвует в регулировании обмена веществ. Высокое содержание витамина Е в сливочном масле ограничивает его самоокисление и повышает стойкость при хранении.
Витамин К по химической природе аналогичен витамину Е и имеет аналогичную биологическую активность. Содержание его в молоке в среднем – 0,03 мкг/100 см3.
Витамином F принято называть группу незаменимых ненасыщенных жирных кислот (линолевая, линоленовая и арахидоновая), которые являются биологически активными веществами и не синтезируются в организме. Содержание этих кислот в молочном жире не высокое по сравнению с растительными маслами и в среднем составляет около 3% от общего содержания жирных кислот.
К водорастворимым витаминам молока относятся следующие.
Витамин В1 (тиамин) стимулирует развитие и рост молочнокислых бактерий в молоке. Биологическая функция его заключается в том, что он являясь коферментом декарбоксилазы, участвует в синтезе белка и нуклеиновых кислот и регулирует углеводный и белковый обмен в организме. Содержание витамина В1 в сборном молоке составляет в среднем от 40 до 60 мкг/100 см3.
Витамин В2 (рибофлавин) обладает свойствами желто-зеленого пигмента (окраска молочной сыворотки), стимулирует рост молочнокислой микрофлоры, входит в состав коферментов окислительно-восстановительных ферментов, принимает участие в обмене белков, жиров, углеводов. Содержание витамина В2 в молоке от 100 до 280 мкг/100 см3.
Витамин В3 (пантотеновая кислота) выполняет функцию фактора роста для дрожжей и пропионовокислых бактерий; входит в состав кофермента А, при участии которого выполняет свою функцию в обмене веществ, в синтезе липидных компонентов в организме. Диапазон колебаний в содержании пантотеновой кислоты в молоке достаточно широк – от 200 до 500 мкг/100 см3 и зависит в большей степени от стадии лактации.
Витамин В6 (пиридоксин) – это группа соединений (пиридоксин, пиридоксаль, пиридоксамин и их фосфорные эфиры, обладающие близкой биологической актвиностью. В виде фосфорных эфиров входит в состав многих ферментов, в том числе трансфераз, катализирующих переаминирование и декарбоксилирование аминокислот. Молоко и молочные продукты являются существенным источником пиридоксина в организме человека. Содержание пиридоксина в молоке колеблется от 20 до 170 мкг/100 см3.
Витамин В9 (фолацин, фолиевая кислота) – это группа соединений, включающих фолиевую кислоту и ее производные, обнаруживающие биологическую активность фолиевой кислоты. Фолиевая кислота является фактором роста для многих микроорганизмов, как и дургие витамины группы В синтезируется микрофлорой рубца жвачных. При ее недостатке в молоке, так же, как и ниацина, пантотеновой кислоты (В3) и биотина (Н), особенно в весенний период, наблюдается замедленное развитие заквасочной микрофлоры. В сборном молоке содержание витамина В9 колебле тся от 0,4 до 260 мкг/100 см3 и зависит главным образом от микробного синтеза в рубце животных и в меньшей степени от содержания в кормах.
Витамин В12 (кобаламин) – сложное органическое соединение, относящееся к классу порфинов, содержит в своем составе кобальт, синтезируется в организме жвачных при участии микрофлоры и частично поступает в организм с кормами животного происхождения. Кобаламин в виде кофермента принимает участие в биосинтезе и обмене аминокислот, жиров, нуклеиновых кислот, белков, оказывает влияние на процесс кроветворения. В молоке витамин В12 как и В9 (фолиевая кислота) связан с иммуноглобулинами. Молоко и молочные продукты являются существенным источником витамина В12 для организма человека. В молоке содержится от 150 до 600 мкг/100 см3 этого витамина.
Витамин РР (ниацин, никотиновая кислота) – по своей химической природе является никотиновой кислотой или ее производным – амидом никотиновой кислоты, синтезируется в организме жвачных микрофлорой рубца. В молоке содержится в свободном состоянии и в составе коферментов НАД и НАДФ дегидрогеназ в относительно небольшом количестве – от 70 до 170 мкг/см3. При его недостатке в организме человека нарушаются синтез белковых компонентов дегидрогеназ, что приводит к нарушению окислительных процессов.
Витамин Н (биотин) – сложное органическое соединение, основу которого составляет тиофеновое кольцо, к которому присоединены остатки валерьяновой кислоты и мочевины. Биотин входит в состав активного центра ферментов, катализирующих реакции карбоксилирования, поэтому принимает участие в биосинтезе липидов, нуклеиновых кислот, углеводов и в других реакциях обмена веществ в организме. В молоке является необходимым компонентом для развития дрожжей и молочнокислых бактерий. Молоко является хорошим источником биотина, содержание его в 100 см3 молока колеблется в пределах от 2 до 10 мкг.
Витамин С (аскорбиновая кислота) – по своей химической природе близка к гексозам (лактон гексоновой кислоты). Активно участвует в окислительно-восстановительных процессах, происходящих как в организме, так и в молоке, легко подвергается окислению. Продукт обратимого окисления ее – дегидроаскорбиновая кислота – также биологически активное соединение, которая может вновь легко восстановиться в аскорбиновую кислоту. Дегидроаскорбиновая и аскорбиновая кислоты обладают витаминной активностью. В свежем молоке содержится около 70% аскорбиновой кислоты и около 30% дегидроаскорбиновой, всего в молоке содержится от 1200 до 3500 мкг/100 см3 витамина С.
Витамин С участвует во многих окислительно-восстанови-тельных реакциях организма: синтез некоторых гормонов, утилизация липидов, превращения аминокислот и др.
В молоке витамин С оказывает влияние на окислительно-восстановительный потенциал, от чего зависят его органолептические свойства и стойкость при хранении. Окисление аскорбиновой кислоты ускоряется в присутствии металлов (железа, меди), света, воздуха, а также при нагревании.
Характеристика ферментов молока. Использование свойств ферментов в оценке качества молока
Ферменты (энзимы) – вещества белковой природы, являющиеся биологическими катализаторами. Действие ферментов строго специфично. Определяющими условиями активности ферментов являются определенная температура, диапазон рН, а также наличие активаторов. Для большинства ферментов максимум активности наблюдается в интервале температур от 40 до 50оС.
При пастеризации молока происходит инактивация ферментов, что предохраняет его от возможных ферментативных процессов и порчи.
В настоящее время известно более 1000 ферментов, которые подразделяют на шесть классов:
1 – оксидоредуктазы, катализирующие окислительно-восста-новительные реакции;
2 – трансферазы (ферменты, переносящие группы);
3 – гидролазы (гидролитические ферменты);
4 – лиазы (ферменты отщепления групп);
5 – изомеразы (ферменты изомеризации);
6 – лигазы (синтетазы).
Из всех классов ферментов в практике производства молока и молочных продуктов наибольшее значение имеют оксидоредуктазы и гидролазы.
Из молока, полученного при нормальных условиях от здоровых животных, выделено более 20 истинных или нативных ферментов. Часть их образуется (синтезируется) непосредственно в секреторных клетках молочной железы и переходит в молоко во время секреции (щелочная фосфатаза, ксантиноксидаза, лизоцим и др.). Другая часть пероксидаза, каталаза, альдолаза, протеиназа и др.) переходит в молоко из крови животного.
Кроме нативных ферментов в молоке присутствуют бактериальные ферменты, образующиеся в результате жизнедеятельности микроорганизмов молока и бактериальных заквасок. Они могут быть внеклеточными и внутриклеточными. Внеклеточные ферменты (экзоферменты) выделяются в окружающую среду как продукты жизнедеятельности клеток. Внутриклеточные (эндоферменты) действуют внутри клетки и выделяются только после ее отмирания и автолиза (распада). При производстве отдельных молочных продуктов вносят некоторые ферментные препараты: в производстве сыров, белковых концентратов, творога – сычужный фермент и его заменители, пепсин; в производстве гидролизованной сыворотки – β-галактозидазу и др.
Нативные и микробные ферменты, содержащиеся в молоке и молочных продуктах, имеют большое практическое значение. Так, на действии ферментов гидролаз, оксидоредуктаз и других основано производство кисломолочных продуктов и сыров. Многие липолитические, протеолитические и другие ферменты наряду с участием в биохимических превращениях составных частей молока и формировании вкусовых характерситик продукта (например, сыров), вызывают глубокие изменения компонентов молока во время выработки и хранения молочных продуктов, что может привести к появлению пороков и снижению их питательной ценности. Кроме того, по активности некоторых нативных и бактериальных ферментов можно судить о санитарно-гигиеническом состоянии сырого молока или эффективности его пастеризации.
Активность ферментов выражают в стандартных единицах – Е, которые соответствуют количеству фермента, катализирующего превращение субстрата со скоростью 1 мкмоль в 1 мин при стандартных условиях. В последнее время активность ферментов выражают в ноых единицах – катал (кат). 1 кат соответствует количеству фермента, катализирующего превращение субстрата со скоростью 1 моль в 1 с (1 кат = 6.107 Е).
Оксидоредуктазы. К этому классу относятся все ферменты – переносчики электронов и водорода, которые катализируют процессы биологического оисления. В основном применяется термин «дегидрогеназа» и «редуктаза». Наименование ферментов этого класса составляются по форме «донор : акцептор оксидоредуктаза». Например: лактатдегидрогеназа – катализирует реакцию восстановления пирувата до молочной кислоты; ксантин: О2 – оксидоредуктаза (ксантиноксидаза); Н2О2:Н2О2 – оксидоредуктаза (каталаза).
Из оксидоредуктаз (нативных) в молоке в соновном присутствуют ксантиноксидаза, каталаза, лактопероксидаза, в небольшом количестве – лактотдегидрогеназа, пируватдегидрогеназа.
Перенос атомов водорода осуществляют коферменты: у анаэробных дегидрогеназ – никотинамидадениндинуклеотид (НАД) или никотинамидадениндинуклеотидфосфат (НАДФ), у аэробных - флавинадениндинуклеотид (ФАД). Дегидрогеназы принимают активное участие в молочнокислом, пропионовокислом и спиртовом брожениях. Анаэробные дегидрогеназы (редуктазы) почти не вырабатываются клетками молочной железы, а накапливаются в молоке при размножении в нем бактерий. С увеличением количества бактерий в молоке увеличивается и количество редуктаз, возрастает их активность, которую определяют по продолжительности восстановления (обесцвечивания) добавленного к молоку метиленового синего или по изменению окраски при добавлении резазурина (проба на редуктазу). По этой пробе на предприятиях молочной промышленности определяют бактериальную обсемененность молока.
Из аэробных дегидрогеназ в молоке содержится ксантиноксидаза, катализирующая окисление альдегидов и пуриновых оснований до соответствующих карбоновых кислот.
Пероксидаза (лактопероксидаза) катализирует окисление различных органических соединений с помощью перекиси водорода, а также может окислять неорганические соединения (например, йодид калия).
2Н2О2 пероксидаза 2Н2О + 2О АН2 + О Н2О + А`
окисляемое
вещество
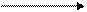 2КJ + H2O2 пероксидаза 2 KOH + J2
2КJ + H2O2 пероксидаза 2 KOH + J2
Пероксидаза довольно термостабильна, инактивируется при 80оС. По реакции на пероксидазу в молочной промышленности определяют эффективность пастеризации. Пробу на пероксидазу проводят с солянокислым парафенилендиамином или йодистокалиевым крахмалом. Первый метод основан на разложении добавленной к молоку перекиси водорода пероксидазой и окислении выделившимся атомарным кислородом парафенилендиамина, с появлением темно-синего окрашивания (при попадании в пастеризованное молоко сырого или при недопастеризации). Проба с йодистокалиевым крахмалом основана на разложении перекиси водорода пероксидазой, содержащейся в молоке. Освободившийся при этом атомарный кислород окисляет йодид калия, освобождая йод, образующий с крахмалом соединение синего цвета.
Каталаза осуществляет окисление перекиси водорода.
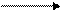 2Н2О2 каталаза 2Н2О + О2
2Н2О2 каталаза 2Н2О + О2
Каталаза в основном вырабатывается бактериями. В свежем молоке от здоровых коров каталазы очень мало. В молозиве и молоке от больных животных ее количество резко увеличивается. Поэтому определение активности каталазы используют как метод обнаружения молока от больных животных. Контроль основан на определении количества кислорода, выделившегося из добавленной к 15 см3 молока перекиси водорода. Натуральное молоко выделяет 1,5-3,0, анормальное – от 8 до 15 см3 кислорода.
Гидролазы. К гидролитическим ферментам относятся ферменты, катализирующие гидролитические расщепления жиров, углеводов, белков и других сложных органических соединений. Из этого класса в молоке присутствуют: липазы, фосфолипазы, β-галактозидаза (лактаза), фосфатазы, протеиназы, лизоцим, рибонуклеаза, амилазы и др.
В молоке содержатся нативные и бактериальные липазы, катализирующие гидролиз триацилглицеринов молочного жира. Нативные липазы инактивируются при температуре 74-80оС, бактериальные – 85-90оС. В нормальном молоке содержание нативных липаз невелико и их актвиность достаточно низкая. В стародойном молоке, в молозиве, в молоке от больных животных повышается содержание нативных липаз, происходит перераспределение их с белков на оболочку жировых шариков. Следствием чего является гидролиз молочного жира и накопление продуктов гидролиза (в избыточном количестве летучих жирных кислот).
Активизация нативных липаз может произойти и вследствие механических воздействий, а также насыщения молока кислородом воздуха.
Бактериальные липазы, выделяемые посторонней микрофлорой молока (плесневые грибы, микрококки), отличаются высокой активностью, следствием чего может явиться появление прогорклого вкуса молока, масла или других продуктов.
Бактериальные липазы заквасочных культур молочнокислых и пропионовокислых бактерий, микроскопических грибов (в производстве рокфора, русского камамбера) принимают участие в формировании специфических органолептических показателей молочных продуктов. По этой причине при подборе бактериальных культур в состав заквасок учитывают их липолитическую активность.
Фосфолипазы катализируют гидролиз фосфолипидов. В молоке содержатся нативные фосфолипазы, не обладающие высокой активностью и бактериальные, в том числе продуцируемые как заквасочной микрофлорой, так и посторонней микрофлорой молока.
Фосфолипазная активность молочнокислых бактерий заквасок достаточно изучена и ее учитывают при выборе отдельных штаммов как молочнокислых, так и пропионовокислых бактерий в их состав, поскольку продукты гидролиза фосфолипидов, по-видимому, принимают участие в формировани вкуса сыров.
Фосфатазы катализируют гидролиз фосфорорганических соединений с образованием неорганического фосфата. В молоке обнаружены щелочная фосфатаза (оптимум рН 9,6) и кислая (оптимум рН около 5). Щелочная фосфатаза чувствительна к повышенной температуре. Она полностью инактивируется при 72-74оС, а кислая фосфатаза термостабильна. Высокая чувствительность щелочной фосфатазы к нагреванию положена в основу контроля эффективности пастеризации молока и сливок.
Проба на фосфатазу по реакции с 4-аминоантипирином основана на гидролизе динатриевой соли фенилфосфорной кислоты ферментом фосфатазой. Выделившийся при гидролизе свободный фенол в присутствии окислителя дает розовое окрашивание с 4-аминоанти-пирином.
Проба на фосфатазу по реакции с фенолфталеинофосфатом натрия основана на его гидролизе ферментом фосфатазой, содержащейся в молоке или молочных продуктах. Освобождающийся при гидролизе фенолфталеин в щелочной среде дает розовое окрашивание.
Гликозидазы. К ним относятся β-галактозидаза, амилазы, лизоцим и др.
β-Галактозидаза (лактаза)катализирует гидролитическое расщепление лактозы на моносахариды: глюкозу и галактозу. Эта реакция является первой стадией сложных многоэтапных процессов молочнокислого, пропионовокислого, спиртового брожений, положенных в основу производства большого количества кисломолочных продуктов.
Кроме этого, β-галактозидазу используют для ферментативного гидролиза лактозы в молоке с целью получения низколактозных продуктов (молока, кефира, йогурта и др) для детей и взрослых, организм которых недостаточно усваивает лактозу. С использованием β-галактозидазы проводят ферментативный гидролиз лактозы и в молочной сыворотке, позволяющей перевести молочный сахар в некристаллизуемую и хорошо сбраживаемую смесь глюкозы и галактозы. Моносахара более сладкие на вкус, чем лактоза, поэтому гидролизованную молочную сыворотку используют в кондитерской и хлебобулочной промышленности.
Амилазы. В молоке содержится в основном α-амилаза. Фермент катализирует расщепление полисахаридных цепей крахмала, гликогена, полисахаридов. Содержание амилазы в молоке повышается при заболевании животных. Фермент связан с лактоглобулиновой фракцией молока и инактивируется при всех режимах пастеризации.
Лизоцим (мурамидаза). Фермент относят к антибактериальным факторам молока, в некоторой степени обусловливающим и его бактерицидные свойства. Это объясняется тем, что лизоцим катализирует гидролиз 1,4-β-связей между остатками N-ацетилмурамовой кислоты и N-ацетилглюкозамина в полисахаридах клеточных стенок некоторых видов бактерий, в первую очередь грамположительных (патогенные стафилококки и другие возбудители мастита у лактирующих коров). Содержание лизоцима в коровьем молоке в среднем составляет около 13 мкг в 100 см3, а в женском – значительно выше: от 10 до 100 мг в 100 см3. Лизоцим стабилен в кислой среде и выдерживает нагревание молока до высоких температур.
Протеазы (протеиназы) - это ферменты, катализирующие гидролиз белков и продуктов их распада (полипептидов, пептидов), разрывая их пептидные связи. В молоке содержатся нативные и бактериальные протеазы. К нативным протеазам относится, главным образом, щелочная протеаза – плазмин. Микрофлора молока продуцирует щелочные и кислые протеазы.
Плазмин попадает в молоко из крови, содержится в низких концентрациях (около 0,3 мг/дм3), связан с мицеллами казеина и лишь частично – с оболочками жировых шариков. Фермент наиболее активен при рН от 6,5 до 9,0 и температуре от 5 до 55оС, довольно термостабилен: полная инактивация его наступает при нагревании молока до 90оС в течение 5 мин.
Плазмин проявляет определенную субстратную специфичность по отношению к фракциях казеина. Наиболее чувствительны к плазмину β- и αS2- казеины; αS1- и κ-казеины гидролизуются намного медленнее; β-лактоглобулин и α-лактальбумин устойчивы к действию фермента. Этим объясняются изменения в соотношении фракций казеина при длительном хранении охлажденного молока. Под действием плазмина происходит частичный необратимый гидролиз β-казеина с образованием фрагментов, обозначаемых γ-казеинами (γ1-, γ2-, γ3-),а также горьких пептидов и других продуктов, придающих молоку горький вкус. Кроме того, при изменении фракционного состава казеина ухудшаются технологические свойства молока – способность свертываться под действием сычужного фермента. Вследствие этого ухудшаются свойства сычужных сгустков и снижается выход сыров и других белковых продуктов (γ-казеин не свертывается под действием сычужного фермента и переходит в сыворотку).
Наряду с плазмином (нативная протеаза) в молоке содержатся и бактериальные протеазы, образующиеся в результате жизнедеятельности молочнокислых стрептококков и палочек, но в большей степени – психротрофных бактерий, выделяющих активные термостабильные протеазы, относящиеся к щелочным и кислым видам протеолитических ферментов. Они активны при рН от 6,8 до 8,0, более активны по отношению к κ- и β-казеинам. Результатом их действия является ухудшение технологических свойств молока и появление пороков вкуса.
Деятельность протеаз бактериального происхождения, вырабатываемых заквасочными культурами, положена в основу созревания сыров. Степень и глубина протеолиза, а следовательно накопление его продуктов: полипептидов, пептидов, аминокислот, участвующих в формировании вкуса и аромата сыров, обусловлена, главным образом, активностью бактериальных протеаз заквасочных культур.
Кроме гидролитических и окислительно-восстановительных ферментов в молоке содержатся ферменты других классов. При производстве кисломолочных продуктов и сыров микрофлора бактериальных заквасок вырабатывает очень важные ферменты, относящиеся к классам лиаз, трансфераз, изомераз.
Например, при спиртовом брожении в кефире и кумысе расщепление пировиноградной кислоты на уксусный альдегид и углекислый газ осуществляет фермент класса лиаз – декарбоксилаза.
В процессе созревания сыров декарбоксилирование аминокислот с образованием аминов происходит под действием декарбоксилаз, а переаминирование осуществляют ферменты класса трансфераз – аминоферазы. В последнее десятилетие отечественной научной школой, возглавляемой академиком РАСХН И.А.Роговым (МГУПБ) проведены исследования ферментов подгруппы рибонуклеаз (класса гидролаз) в молоке, играющих важную роль в регулировании клеточного метаболизма, среди которых по своей биологической функции выделен ангиогенин как активный иммуномодулятор и фактор роста кровеносных сосудов. Ангиогенин получен из вторичного молочного сырья в составе белковой фракции. Результатом исследований явилось создание биологически активной добавки ангиогенина, которая рекомендована для использования в кчаестве самостоятельной БАД, а также для обогащения традиционных молочных продуктов; в качестве БАД к парафармацевтическим молочным продуктам (продуктам для лиц, страдающих различными заболеваниями); к детским молочным продуктам.
Гормоны и газы
Среди биологически активных соединений молока в нем обнаружены гормоны: эндогенные гормоны, выделяемые эндокринными железами животного, и экзогенные – гормоны, применяемые в виде препаратов для стимулирования молочной продуктивности, усвоения кормов и т.д.
По химическому строению некоторые из них являются пептидами и белками, большая группа имеет стероидную структуру, отдельные представляют собой производные аминокислот и жирных кислот.
Из гормонов пептидной природы в молоке обнаружены пролактин, окситоцин, соматропин; из стероидных гормонов – кортикостероиды и андрогены; из гормонов – производных аминокислот – тироидные гормоны (производные тирозина) и группа простогландинов – производных полиненасыщенных жирных кислот.
Из обнаруженных в молоке гормонов не все определены количественно, но по содержанию отдельных имеются существенные различия в зависимости от стадии лактации. Например, содержание пролактина в молозиве в 2-7 раз больше, чем в нормальном молоке, а андрогенов – в 10-100 раз.
Характеризуя компонентный состав молока, следует назвать газы: углекислый, кислород и азот. Общее содержание газов в молоке составляет от 60 до 120 мг в 1 дм3, из них на долю углекислого газа приходится от 60 до 70%, кислорода – от 6 до 10%, азота – от 25 до 30%. В молоке содержится также незначительное количество аммиака (около 0,2.10-3 М).
Содержание газов в молоке зависит от способов доения, хранения, транспортировки и обработки молока, при которых молоко соприкасается с воздухом и содержащиеся в нем газы растворяются в молоке.
После дойки содержание газов в молоке устанавливается на определенном уровне. При последующих хранении, транспортировке и обработке молока содержание отдельных газов в нем меняется. Так, в процессе хранения молока вследствие развития микроорганизмов повышается содержание аммиака, а кислорода – понижается. Поэтому по содержанию этих газов возможен контроль качества молока-сырья.
При очистке, перекачивании, транспортировке молока содержание кислорода в нем может повыситься, что повлечет за собой увеличение окислительно-восстановительного потенциала и, как следствие, появление в молоке во время хранения окисленного привкуса. При пастеризации молока, наоборот, растворенный кислород и углекислый газ улетучиваются, что сопровождается снижением окислительно-восстановительного потенциала и титруемой кислотности молока.
Контрольные вопросы
1. Какие соединения в молоке относят к биологически активным?
2. Какова роль витаминов в молоке и молочных продуктах?
3. Какие витамины объединяют в группу жирорастворимых, в чем заключается их биологическая роль?
4. Какую роль играют водорастворимые витамины в молоке и молочных продуктах?
5. Какие ферменты имеют наибольшее значение в практике производства молочных продуктов?
6. Что такое нативные и бактериальные ферменты?
7. Какие ферменты молока относят к классу оксидоредуктаз, какое значение они имеют в производстве молочных продуктов?
8. Какие свойства оксидоредуктаз положены в основу методов контроля молока?
9. Какие ферменты молока относят к классу гидролаз, каковы их основные свойства?
10. Как изменяется фракционный состав казеина под действием плазмина при длительном хранении молока?
11. Как изменяется содержание газов в молоке при хранении, транспортировке и обработке?
Дата добавления: 2016-12-08; просмотров: 1622;
