Электродные потенциалы. Гальванические элементы. ЭДС
При соприкосновении двух химически или физически разнородных материалов (металл 1 (проводник I рода) – металл 2 (проводник I рода), металл (проводник I рода) – раствор соли металла (проводник II рода), раствор электролита 1 (проводник II рода) – раствор электролита 2 (проводник II рода) и т. д.) между ними возникает двойной электрический слой (ДЭС). ДЭС является результатом упорядоченного распределения противоположно заряженных частиц на границе раздела фаз.
Образование ДЭС приводит к скачку потенциала φ, который в условиях равновесия металл (проводник I рода) – раствор соли металла (проводник II рода) называется галъвани-потенциалом.
Система: металл (Me) – водный раствор соли данного Me – называется электродом или полуэлементом и схематически изображается следующим образом:
Меn+ | Me
Электрод (п/э) записывается так, чтобы все вещества, находящиеся в растворе, были помещены слева, а электродный материал – справа от вертикальной черты.
φ > 0, если на электроде протекает реакция восстановления Меn+ + nе¯ ↔ Ме0,
φ < 0, если на электроде протекает реакция окисления Ме0 ↔ Меn+ + nе¯.
Электродным потенциалом Е Меn+/Ме называется равновесная разность потенциалов, возникающая на границе фаз проводник I рода/проводник II рода и измеренная относительно стандартного водородного электрода.
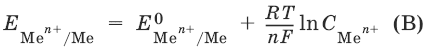
уравнение Нернста, где n – число электронов, участвующих в электродной реакции; С Меn+ – концентрация катионов; Е Меn+/Ме – стандартный электродный потенциал.
Контактный потенциал φχ – равновесный скачек потенциалов, возникающий на границе раздела двух проводников I рода.
Диффузионный потенциал φ диф – равновесная разность потенциалов, возникающая на границе фаз проводник II рода/проводник II рода.
Гальванический элемент (г. э.) – электрическая цепь, состоящая из двух или нескольких п.э. и производящая электрическую энергию за счет протекающей в ней химической реакции, причем стадии окисления и восстановления химической реакции пространственно разделены.
Электрод, на котором при работе гальванического элемента протекает процесс окисления, называется анодом, электрод, на котором идет процесс восстановления, – катодом.
Дата добавления: 2016-04-23; просмотров: 828;
