Типы гибридизации атома углерода в органических соединениях
ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Органические соединения – это соединения углерода (кроме наиболее простых), в которых он проявляет валентность IV.
Органическая химия – это химия углеводородов и их производных.
Атом углерода в органических соединениях находится в возбужденном состоянии и имеет четыре неспаренных электрона:

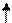
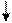
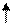

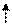








 6С 1s22s22p2 → 6С* 1s22s12p3
6С 1s22s22p2 → 6С* 1s22s12p3
sp3
Атом углерода в возбужденном состоянии способен:
1) образовывать прочные связи с другими атомами углерода, что приводит к формированию цепей и циклов;
2) вследствие различного типа гибридизации орбиталей формировать простые, двойные и тройные связи между атомами углерода и с другими атомами (H, O, N, S, P и др.);
3) соединяться с четырьмя различными атомами, что приводит к образованию разветвленных углеродных цепочек.
Типы гибридизации атома углерода в органических соединениях
sp3 – гибридизация
Все четыре валентные орбитали участвуют в гибридизации. Валентный угол 109о28’ (тетраэдр). Атомы углерода образуют только простые (σ) связи – соединение насыщенное.
sp2 – гибридизация
Образуются три гибридные и одна негибридная орбиталь. Валентный угол 120о (плоские структуры, правильный треугольник). Гибридные орбитали образуют σ–связи. Негибридные орбитали образуют p-связи. sp2–Гибридизация характерна для непредельных соединений с одной p - связью.
sp – гибридизация
Образуются две гибридные и две негибридные орбитали. Валентный угол 180о (линейные структуры). Атом углерода в состоянии sp-гибридизации принимает участие в образовании двух двойных связей или одной тройной связи.
Теория строения органических соединений сформулирована в 1861 г А.М. Бутлеровым и включает следующие положения:
1. Все атомы, входящие в состав молекулы, связаны между собой в строго определенной последовательности в соответствии с их валентностями. Порядок соединения атомов в молекулу обусловливает ее химическое строение.
2. Свойства органических соединений зависят не только от качественного и количественного состава веществ, но и от порядка их соединения (химического строения молекулы).
3. Атомы в молекуле оказывают взаимное влияние друг на друга, т.е. свойства групп атомов в молекуле могут изменяться в зависимости от природы других атомов, входящих в состав молекулы. Группа атомов, определяющая химические свойства органических молекул, носит название функциональная группа.
4. Каждое органическое соединение имеет лишь одну химическую формулу. Зная химическую формулу, можно предсказать свойства соединения, а изучая на практике его свойства, установить химическую формулу.
 Органическая молекула
Органическая молекула
| углеродная цепочка атомов –углеродный скелет | + | функциональная группа –выделяет классы органических соединений |
Типы углеродного скелета:
- Ациклический:
· разветвленный;
· нормальный (линейный).
- Циклический:
· карбоциклический (цикл только из атомов углерода);
· гетероциклический (кроме атомов углерода в цикл входят некоторые другие атомы – азота, кислорода, серы).
Типы атомов углерода в углеводородной цепи:






 СН3
СН3

 Н3С-СН2-СН-С- СН3
Н3С-СН2-СН-С- СН3


 СН3 СН3
СН3 СН3
- первичные атомы углерода (соединены в цепи только с одним атомом углерода, является концевым);
 - вторичный атом углерода (соединен с двумя соседними атомами углерода, находится в середине цепи);
- вторичный атом углерода (соединен с двумя соседними атомами углерода, находится в середине цепи);

 - третичный атом углерода (находится на разветвлении углеродной цепи, соединен с тремя атомами углерода);
- третичный атом углерода (находится на разветвлении углеродной цепи, соединен с тремя атомами углерода);
- четвертичный атом углерода (не имеет других заместителей, кроме атомов углерода).
Функциональная группа– особая группа атомов, которая определяет химические свойства соединений.
Примеры функциональных групп:
-ОН–гидроксильная группа (спирты, фенолы);
 С=О– карбонильная группа (кетоны, альдегиды);
С=О– карбонильная группа (кетоны, альдегиды);
 ОН
ОН
 С- карбоксильнаягруппа (карбоновые кислоты);
С- карбоксильнаягруппа (карбоновые кислоты);
О
-NH2 –аминогруппа (амины);
-SH –тиольная группа (тиоспирты)

 органическое соединение
органическое соединение
 состав состав
| свойства | химическое строение |
Атомы, входящие в состав органического соединения, могут по-разному соединяться в молекулы. Например, соединению состава С2Н6О может отвечать два химических соединения, имеющих разные физические и химические свойства:
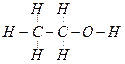
| 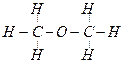
|
| Этанол (этиловый спирт) | Диметиловый эфир |
| (tкип. = 78°C, реагирует с натрием) | (tкип. = –24°C, не реагирует с натрием) |
Состав органического соединения – число атомов различных элементов входящих в его молекулу. Изомеры– соединения, имеющие одинаковый состав, но разное химическое строение. Изомеры обладают различными химическими свойствами.
Типы изомерии
Дата добавления: 2016-11-02; просмотров: 5975;
