Химические свойства антрацена
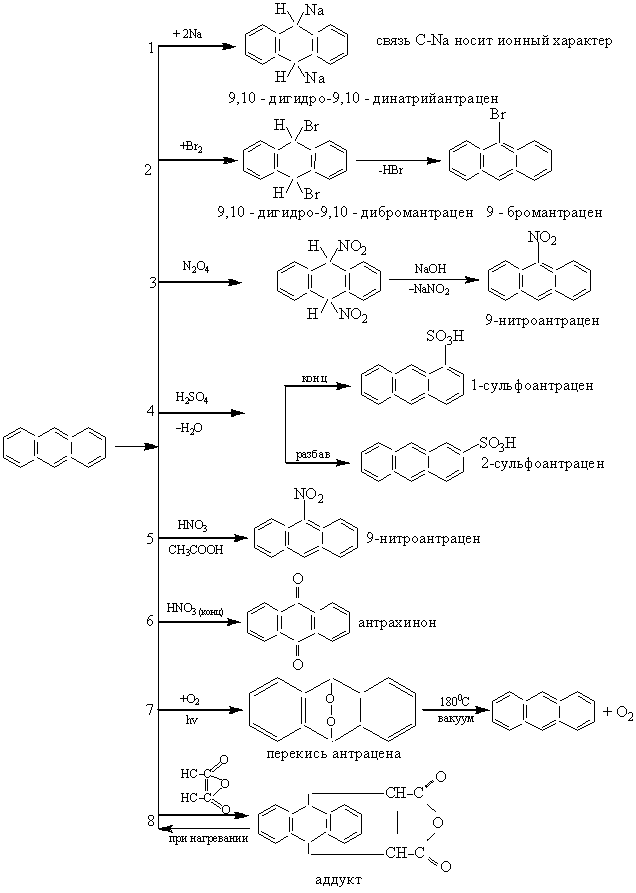
1. Антрацен, подобно диеновым углеводородам, присоединяет щелочные металлы в положение 9, 10.
2. Галогенирование (CI2, Br2) протекает также через стадию присоединения по положению 9, 10 с последующим отщеплением галогеноводорода.
3. Двуокись азота присоединяется по 9, 10. Щелочь отщепляет от продукта присоединения элементы азотистой кислоты и образуется 9-нитроантрацен.
4. Действие серной кислоты зависит от концентрации. Концентрированная H2SO4 сульфирует антрацен в a-положение, а разбавленная – в b-положение.
5. Концентрированная азотная кислота окисляет антрацен до антрахинона, но азотная кислота, растворенная в уксусной, нитрует его в положение 9.
6. Молекулярный кислород при освещении поглощается антраценом – присоединяется по 9, 10-положению, образуя перекись, которая при нагревании в вакууме до 1800С отдает молекулярный кислород. Антрацен при этом выделяется в свободном виде.
7. Антрацен легко присоединяет малеиновый ангидрид и другие диенофилы. Эта реакция используется для количественного определения антрацена в смесях. Полученный аддукт легко разлагается при слабом нагревании с образованием исходных продуктов. Эта реакция используется для очистки антрацена.
Производные антрацена
Антрахинон
Наибольшее значение из соединений ряда антрацена имеет антрахинон и его производные
Антрахинон – сравнительно высокоплавкое (tпл = 284,80С), нелетучее прочное соединение, сходное по свойствам с бензофеноном.
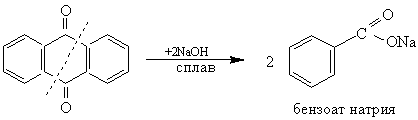
При сплавлении со щелочью разлагается с образованием бензойной кислоты.
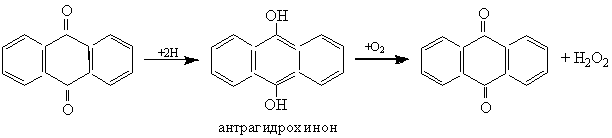
Антрахинон может восстанавливаться до антрагидрохинона, который может окисляться воздухом. При этом образуется перекись водорода. На практике таким путем получают концентрированную перекись водорода
В промышленности большое применение нашла реакция сульфирования

При действии H2SO4 первая сульфогруппа вступает в b-положение одного из ядер, последующее сульфирование идет в a-положение другого ядра. Если в реакционную массу добавить соли 2-х валентной ртути, то первая сульфогруппа направляется в a-положение, а следующая тоже в a-положение, но соседнего ядра.
Ализарин
При нагревании сульфопризводных антрахинона со щелочами, например с Ca(OH)2 сульфогруппы замещаются на гидроксилы с образованием оксиантрахинонов, наибольшее значение из которых приобрел ализарин (1, 2-диоксиантрахинон)
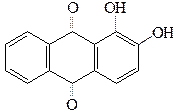
Наиболее обычный способ получения ализарина состоит в одновременном действии на антрахинон - b-сульфокислоту щелочи и окислителя (продувают воздух, или добавляют в плав хлорат натрия)
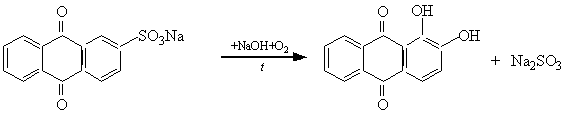
Ализарин – протравной краситель, который с 3-х валентными металлами (AI3+, Cr3+, Fe3+ и т.д.) дает внутрикомплексные окрашенные нерастворимые соединения, так называемые «лаки» следующего строения.
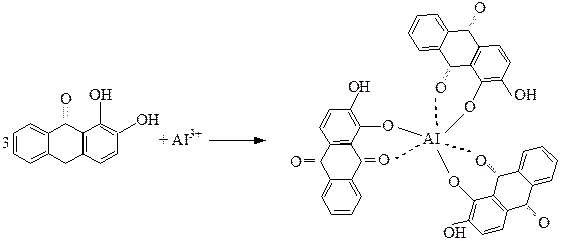
Крашение ализарином производят по «протраве». Для этого вначале ткань пропитывают раствором соли трехвалентного металла. При кипячении такой ткани с ализарином, последний образует с Ме3+ нерастворимый лак. AI3+ - красный (кумачовый); Cr3+ - фиолетовый, коричневый; Fe3+ - фиолетово-черный.
Дата добавления: 2016-02-16; просмотров: 7807;
