Важнейшие реакции электрофильного присоединения
по связи С = С
| № | Реакции | Примечания |
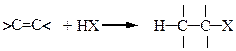
| Присоединение HCl, HBr, HI с образованием алкилгалогенидов | |
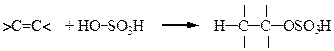
| Присоединение H2SO4 c образованием кислых сульфатов | |
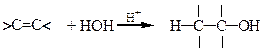
| Кислая гидратация с образованием спиртов | |
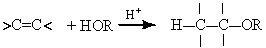
| Присоединение спиртов с образованием простых эфиров (алкоксипроизводных) | |
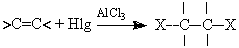
| Присоединение галогенов и смешанных галогенов | |
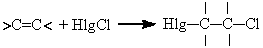
| ||
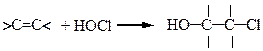
| Присоединение HOHlg с образованием галогенгидринов | |

| Синтез Дильса – Альдера | |
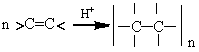
| Катионная полимеризация |
Данные реакции могут протекать через полярные или ионные переходные состояния.
В настоящее время известны три разновидности механизма электрофильного присоединения в зависимости от характера атакующего реагента.
1. Атакующий реагент А+ – В- диссоциирует на ионы
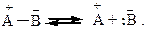
Алкен атакует А+, образуя свободный карбкатион:
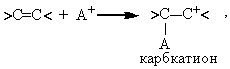
который реагирует с ионом 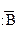
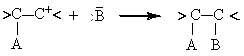
2. Нет предварительной диссоциации атакующего реагента А-В. Тогда разрыв связи А-В инициирует сам алкен
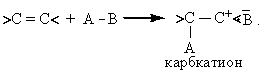
Образующийся карбкатион находится в паре с анионом, который затем переходит в устойчивое состояние:
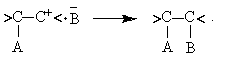
Оба механизма относятся к реакциям бимолекулярного присоединения (AdE2). В стадии, определяющей скорость реакции, участвуют и электрофильный реагент, и алкен.
3. В реагенте 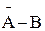 связь достаточно прочная и очень медленно распадается после образования карбкатионов. То тогда в процесс включается еще одна молекула реагента
связь достаточно прочная и очень медленно распадается после образования карбкатионов. То тогда в процесс включается еще одна молекула реагента
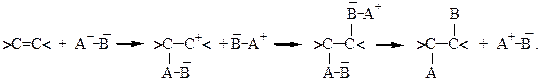
То есть в реакции участвуют одновременно три молекулы, тогда реакция присоединения представляется как AdE3.
Дата добавления: 2016-02-16; просмотров: 1663;
