Присоединение галогеноводородов
Обычно этот процесс протекает в три стадии (рассмотрим на примере присоединения к этену бромоводорода (HBr).
Стадия 1. Образование π–комплекса
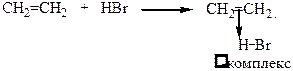
Эта стадия протекает быстро.
Стадия 2. Образование карбкатиона
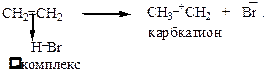
Эта стадия самая медленная – лимитирующая.
Стадия 3. Присоединение бромидиона 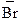 (нуклеофила)
(нуклеофила)
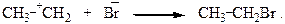
Эта стадия протекает быстро.
Если в реакцию вступает несимметричный алкен, то выполняется правило Марковникова:
| При присоединении несимметричных молекул к несимметричным алкенам положительная часть молекулы присоединяется к наиболее гидрогенизированному углеродному атому при двойной связи в отсутствии перекисей и кислорода воздуха. |
В этом случае можно предположить, что π–комплекс может образовывать два промежуточных карбкатиона

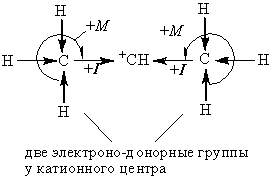
Карбкатионы I и II отличаются по устойчивости. Устойчивость карбкатиона зависит от его строения. Рассмотрим устойчивость карбкатионов.
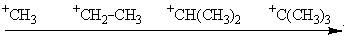
Устойчивость таких карбкатионов возрастает слева направо. Это объясняется делокализацией положительного заряда в третбутилкатионе за счет индуктивного (+I) эффекта и эффекта сверхсопряжения (+М) трех метильных групп:
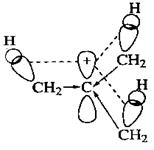
В изопропилкатионе такая делокализация происходит за счет (+I) и (+М) двух метильных групп, в этилкатионе – одной метильной группы. В метилкатионе положительный заряд локализован на углеродном атоме, что и приводит к его нестабильности.
Рассмотрим гидрогалогенирование на конкретном примере – гидробромирование пропена.
Реакция начинается с образования π-комплекса
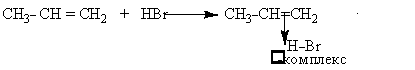
Переход π-комплекса в карбкатион может идти по двум направлениям:
1) образование изопропилкатиона (I);
2) образование пропилкатиона (II).
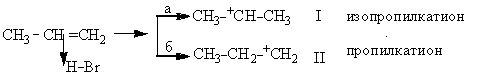
Но изопропилкатион значительно устойчивее пропилкатиона
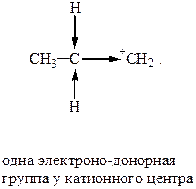
Устойчивость промежуточного карбкатиона определяет энергию активации процесса. Чем устойчивее карбкатион, тем меньшей энергией активации он обладает, тем легче протекает реакция, что наглядно можно представить диаграммой.
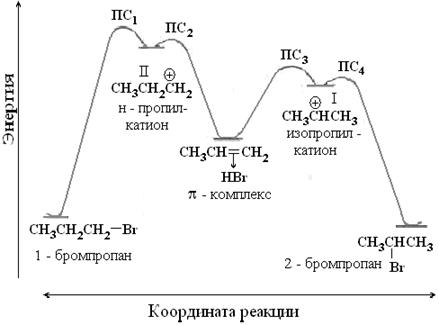
Рис. 9. Энергетическая диаграмма реакции гидробромирования пропена
Эта закономерность выполняется в том случае, если рядом с двойной связью имеются заместители – доноры: –СН3, –О–СН3 и т.д.
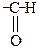 Если рядом с двойной связью имеются заместители–акцепторы (–NO2,
Если рядом с двойной связью имеются заместители–акцепторы (–NO2,  , и т.д.), которые дестабилизируют вторичный карбкатион,
, и т.д.), которые дестабилизируют вторичный карбкатион,
тогда более стабильным оказывается менее замещенный карбкатион, в котором дестабилизирующее действие электроноакцепторного заместителя слабее:
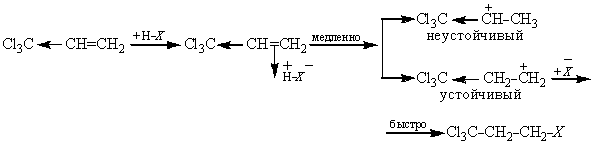
В этом случае присоединение  будет идти против правила Марковникова.
будет идти против правила Марковникова.
По выше рассмотренному механизму протекают реакции присоединения не только HHlg, но и Н2О, HNO3, H2SO4, R–OH, HOCl, HCN и т.д.
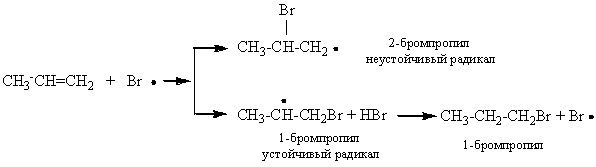
Присоединение бромоводорода к пропену в присутствии перекиси водорода тоже будет протекать против правила Морковникова (эффект Хараша), так как меняется механизм реакции

Механизм реакции – радикальное замещение AdR.
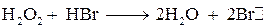
Дата добавления: 2016-02-16; просмотров: 2188;
