Химические свойства. В молекулах алканов атом углерода находится в sp3-гибридизации и имеет тетраэдрическое строение (рис
В молекулах алканов атом углерода находится в sp3-гибридизации и имеет тетраэдрическое строение (рис. 4 и 5).
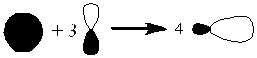
Рис. 4. sp3-Гибридизация
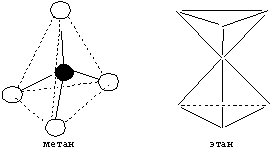
Рис. 5. Тетраэдрические модели метана и этана
Четыре sp3-гибридизованные орбитали атома углерода (рис.6) перекрываются или с s-орбитами атома водорода, образуя σ-связь С-Н (а) или с sp3-гибридизованными орбиталями другого атома углерода, образуя σ-связь С-С (б).
С – Н С – С
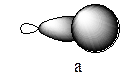

Рис. 6. σ-Связь
Таким образом, алканы содержат σ-связи двух типов С-Н и С-С. Это типичные ковалентные двухцентровые двухэлектронные неполярные химические связи. Дипольный момент алканов равен нулю, что свидетельствует о неполярном характере связей.
Так как в алканах существует 2 типа σ-связей, следовательно, и реакции будут протекать в 2-х направлениях:
а) реакции с разрушением связей С-Н;
б) реакции с разрушением связей С-С (табл. 3).
Таблица 3
Энергия разрыва связей алканов (кДж/моль, 250С)
| Связь | Энергия | Связь | Энергия |
| Н-СН3 | 426,8 | СН3-СН3 | 369,4 |
| Н-СН2СН3 | 405,8 | СН3-СН2 СН3 | 355,6 |
| Н-СН(СН3)2 | 397,5 | СН3 СН2-СН(СН3)2 | 335,6 |
| Н-СН(СН3)3 | 376,6 | СН3 СН2-СН2 СН3 | 342,2 |
Реакции с разрушением σ-связи С-Н (замещение водорода)
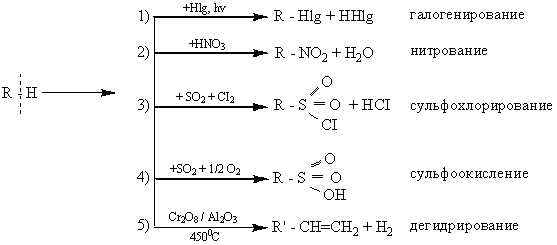
Разрушение связей С-Н требует большой энергии активации и поэтому алканы при обычной температуре не реагируют с концентрированными кислотами, сильными окислителями (KMnO4, HNO3).
Малая полярность связи С-Н предопределяет в основном гомолитический разрыв связи и радикальный характер химических реакций.
Рассмотрим примеры реакций замещения водорода в алканах.
ГАЛОГЕНИРОВАНИЕ
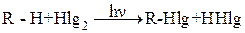 .
.
Механизм реакции – радикальное замещение (SR) протекает в 3 стадии.
Первая стадия. Инициирование:
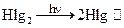 .
.
Вторая стадия. Развитие цепи:

Третья стадия. Обрыв цепи:

На галогенирование оказывает влияние как характер галогена, так и структура субстрата.
Характер галогена
Активность галогенов в рассматриваемых реакциях убывает в ряду
Cl > Br > I.
Из приведенных в табл. 4 галогенов видно, что наиболее активным является хлор, однако бром обладает наибольшей избирательностью.
Дата добавления: 2016-02-16; просмотров: 1336;
