Номенклатура и изомерия простейших предельных углеводородов парафинового ряда
| Эмпирическая формула | Структурная формула | Название | ||
| тривиальное | рациональное | систематическое | ||
| 1) СН4 | СН4 | метан | метан | метан |
| 2) С2Н6 | СН3-СН3 | этан | метилметан | этан |
| 3) С3Н8 | СН3-СН2-СН3 | пропан | диметилметан | пропан |
| 4) С4Н10 | СН3-СН2-СН2-СН3
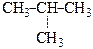
| бутан изобутан | метилэтилметан триметилметан | бутан 2-метилпропан |
| 5) С5Н12 | СН3-СН2-СН2-СН2-СН3
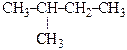
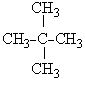
| пентан изопентан неопентан | диэтилметан диметилэтилметан тетраметилметан | пентан 2-метилбутан 2,2-диметилпропан |
В гомологическом ряду алканов число структурных изомеров быстро растет у:
гексана С6Н14 их будет 5,
октана С8Н18 – 18,
декана С10Н22 – 75,
эйкозана С20Н42 – 366317.
2. Стереоизомерия – пространственная конформационная изомерия.
3. Конформация –различные геометрические формы молекулы, переходящие друг в друга путем вращения вокруг σ-связей.
Пространственные конформационные изомеры алканов имеют малый энергетический барьер и в нормальных условиях не могут быть выделены в индивидуальном виде, т.к. они быстро переходят друг в друга. Рассмотрим на примере этана (СН3-СН3) (рис. 3).

Рис. 3. Конформационная изомерия
Энергетический барьер между заслоненной и заторможенной конфигурациями (барьер вращения) этана равен 12,5 кДж/моль (для предотвращения вращения требуется барьер порядка 84 – 130 кДж/моль), то есть теплового движения молекул при комнатной температуре с избытком хватает для преодоления этого барьера. По этой причине пространственные изомеры этана находятся в динамическом равновесии и их невозможно выделить в индивидуальном виде при нормальных условиях.
Дата добавления: 2016-02-16; просмотров: 3077;
