И абсолютной влажностью
Водяной пар подчиняется закону Менделеева–Клайперона
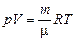 ,
,
где р – парциальное давление водяных паров; т – их масса в объеме V; Т – температура; m = 0,018 кг/моль – молярная масса воды. Тогда
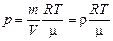 ,
,
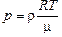 . (14.2)
. (14.2)
Парциальное давление водяных паров прямо пропорционально абсолютной влажности!
Заметим, что парциальное давление водяных паров называют упругостью водяного пара. Тогда если рп – это давление водяных паров при данной температуре, то
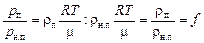 .
.
Итак,
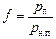 . (14.3)
. (14.3)
Формулой (14.3) можно пользоваться для вычисления относительной влажности.
СТОП! Решите самостоятельно: А2, А6, А7, В7.
Задача 14.4. В пустой сосуд объемом V = 1,0 л вводят т0 = 0,50 г воды, после чего температуру доводят до: 1) t1 = 50 °С; 2) t2 = 100 °С. Какая масса воды останется в сосуде в каждом случае? Чему будет равно давление паров воды в каждом случае? Объемом воды по сравнению с объемом сосуда пренебречь.
| V = 1,0 л = 1,0×10–3 м3 т0 = 0,50 г t1 = 50 °С Þ Т1 = 323 К t2 = 100 °С Þ Т2 = 373 К | Решение. Абсолютная влажность при испарении всей воды стала бы равна
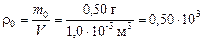 г/м3 =
= 0, 50 кг/м3. г/м3 =
= 0, 50 кг/м3.
|
| т1, т2 = ? р1, р2 = ? |
Найдем по табл. 14.1 давления насыщенного пара при 50 °С и 100 °С:
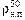 = 83 г/м3 < r0 = 0,50×103 г/м3;
= 83 г/м3 < r0 = 0,50×103 г/м3;
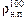 = 597 г/м3 > r0 = 0,50×103 г/м3.
= 597 г/м3 > r0 = 0,50×103 г/м3.
В первом случае для насыщения пара требуется испарить воды
Dт1 = 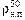 V = 83 г/м3 × 1,0×10–3 м3 = 0,083 г.
V = 83 г/м3 × 1,0×10–3 м3 = 0,083 г.
У нас же целых 0,50 г. Значит, останется воды
т1 = т0 – Dт1 = 0,50 г – 0,083 г » 0,42 г;
Давление насыщенных паров составит
р1 = 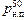 =
= 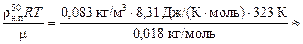
» 12×103 Па = 12 кПа.
Во втором случае испарится вся вода, поэтому т2 = 0. Давление ненасыщенного пара будет равно
р2 = 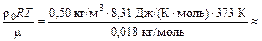
» 86×103 Па = 86 кПа.
Ответ: т1 » 0,42 г; р1 = 12 кПа; т2 = 0; р2 = 86 кПа.
СТОП! Решите самостоятельно: В6, В8, В9.
Задача 14.5. В закрытый сосуд объемом V = 1,0 м3, в котором содержался сухой воздух при давлении р0 = 1,0×105 Па и температуре Т0 = 293 К, ввели воду: 1) т1 = 15 г; 2) т2 = 150 г, после чего температуру в сосуде довели до Т1 = 323 К. Найти давление в сосуде в каждом случае. Объемом воды пренебречь.
| V = 1,0 м3 р0 = 1,0×105 Па Т0 = 293 К т1 = 15 г т2 = 150 г Т1 = 323 К | Решение. По табл. 14.1 найдем плотность насыщенного пара три Т = 323 К = 50 °С:
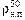 = 83 г/м3.
Плотность пара при условии полного испарения введенной воды будет равна: = 83 г/м3.
Плотность пара при условии полного испарения введенной воды будет равна:
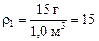 г/м3 < г/м3 < 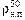 = 83 г/м3. = 83 г/м3.
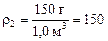 г/м3 > г/м3 > 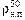 = 83 г/м3. = 83 г/м3.
|
| р1 = ? р2 = ? | |
Значит, в первом случае вся вода испарится, а во втором случае не вся вода испарится. Давление в сосуде будет складываться из суммы парциальных давлений воздуха и водяного пара.
Для первого случая: 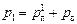 . Давление пара найдем из уравнения Менделеева–Клайперона:
. Давление пара найдем из уравнения Менделеева–Клайперона:
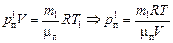 .
.
Давление воздуха найдем из уравнения Шарля:
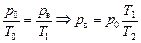 .
.
Тогда 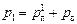 =
= 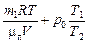 .
.
Подставим численные значения:
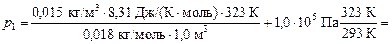
= 2,236×103 Па + 110,23×103 Па » 1,1×105 Па.
Для второго случая: 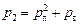 . Во втором случае давление
. Во втором случае давление 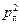 пара будет равно давлению насыщенных паров при 50 °С, а парциальное давление воздуха рв останется таким же.
пара будет равно давлению насыщенных паров при 50 °С, а парциальное давление воздуха рв останется таким же.
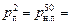
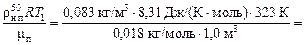
= 12,376×103 Па.
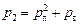 = 12,376×103 Па + 110,23×103 Па =
= 12,376×103 Па + 110,23×103 Па =
= 122,5×103 Па » 1,2×105 Па.
Ответ: р1 » 1,1×105 Па; р2 » 1,2×105 Па.
СТОП! Решите самостоятельно: С3, С5.
Автор: Что тяжелее: 1 м3 сухого воздуха или 1 м3 влажного воздуха при нормальных условиях?
Читатель: Конечно, влажного. Ведь в нем, кроме молекул воздуха, есть еще и молекулы воды, которые тоже имеют массу.
Автор: Вы немного поторопились с ответом. В самом деле, согласно закону Авогадро при нормальных условиях моль любого газа занимает одинаковый объем 22,4 л, и в этом объеме содержится одно и то же число молекул NA = 6,02×1023 (штук). Ясно, что в 1 м3 влажного и сухого воздуха будет содержаться одинаковое число молекул. Но! Средняя масса молекул воздуха »29 а.е.м., а масса молекулы воды 18 а.е.м. Значит, во влажном воздухе какую-то часть молекул воздуха (азота, кислорода) заменят более легкие молекулы воды. А так как число молекул влажного и сухого воздуха одинаково в 1 м3, то влажный воздух имеет меньшую массу!
Задача 14.6. Давление насыщенного водяного пара при t = =36 °С равно 44,6 мм рт. ст. Какую массу имеет при этой температуре V = 1,00 м3 влажного воздуха при относительной влажности f = 0,80 и давлении р0 = 1,013×105 Па. Найти также массу сухого воздуха при этой температуре.
t = 36 °С = 309 К
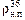 = 44,6 мм рт. ст. =
= 5,93 кПа
V = 1,00 м3
f = 0,80
р0 = 1,013×105 Па = 44,6 мм рт. ст. =
= 5,93 кПа
V = 1,00 м3
f = 0,80
р0 = 1,013×105 Па
| Решение. Общее давление складывается из давления воздуха и паров воды:
р0 = рвоз + рп.
Так как
рп = f 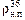 ,
тогда
рвозд = р0 – рп = р0 – f ,
тогда
рвозд = р0 – рп = р0 – f 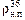 . .
|
| твл = ? тс = ? |
Запишем уравнение Менделеева–Клайперона для пара и воздуха отдельно:
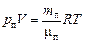 ;
; 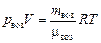 .
.
Масса влажного воздуха твл равна сумме масс воздуха и водяного пара:
твл = тп + твоз = 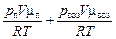 =
=
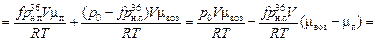
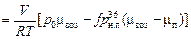 .
.
Подставим численные значения:
твл = 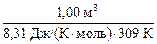 ×[1,013×105 Па ×0,029 кг/моль –
×[1,013×105 Па ×0,029 кг/моль –
– 0,80 × 5,93×103 Па × (0,029 – 0,018) кг/моль] » 1,12 кг.
Массу сухого воздуха найдем из уравнения Менделеева–Клайперона
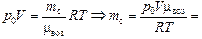
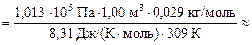 1,13 кг.
1,13 кг.
Действительно, масса сухого воздуха больше!
Ответ: твл » 1,12 кг; тс » 1,13 кг.
СТОП! Решите самостоятельно: В16, С2, С6.
Дата добавления: 2016-04-11; просмотров: 1085;
