Теплоемкости газов при 20 °С
| Газ | μ, кг/моль | 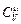 ,
Дж/(моль×К) ,
Дж/(моль×К)
| 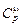 ,
Дж/(моль×К) ,
Дж/(моль×К)
| 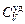 ,
Дж/(кг×К) ,
Дж/(кг×К)
| 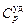 ,
Дж/(кг×К) ,
Дж/(кг×К)
|
| Не Аr Kr Ne Н2 O2 N2 Воздух СО2 | 0,004 0,040 0,084 0,020 0,002 0,032 0,028 0,029 0,044 | 12,5 12,5 12,5 12,7 20,6 21,0 20,8 20,7 28,8 | 20,8 20,8 20,8 21,1 28,9 29,3 29,1 29,0 37,1 | 654,5 |
Сравнивая табличные данные с теоретическими значениями молярной теплоемкости СV = 12,5 Дж/(моль×К) для одноатомных газов и СV = 20,8 Дж/(моль×К) для двухатомных, видим, что налицо неполохое соответствие теории и практики.
Задача 11.2. В вертикальном сосуде с подвижным тяжелым поршнем находится n = 10 моль одноатомного газа. Какое количество теплоты необходимо подвести к газу, находящемуся под давлением р = 1,0 МПа, чтобы повысить его температуру на 10 К?
р = 1,0 МПа
р = const
n = 10 моль
DТ = 10 К
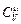 = 3/2 R = 3/2 R
| Решение.
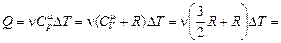
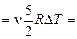 10 моль 10 моль 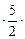 8,31 Дж/(моль×К)×10 К » 8,31 Дж/(моль×К)×10 К »
|
| Q = ? |
» 2,0×103 Дж.
Ответ: Q 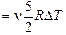 » 2,0×103 Дж.
» 2,0×103 Дж.
Читатель: А причем в задаче р = 1,0 МПа?
Автор: А не причем! Это лишнее данное. Чтобы Вы обратили внимание на то, что Q от давления не зависит.
СТОП! Решите самостоятельно: А3, А4, В1, В7.
Задача 11.3. При адиабатическом расширении т = 1 кг азота совершена работа А = 300 Дж. На сколько уменьшились внутренняя энергия газа и его температура? Удельная теплоемкость азота при неизменном объеме 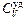 = 743 Дж/(кг×К).
= 743 Дж/(кг×К).
т = 1 кг
А = 300 Дж
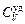 = 743 Дж/(кг×К)
μ = 0,028 кг/моль
Q = 0 = 743 Дж/(кг×К)
μ = 0,028 кг/моль
Q = 0
| Решение. Q = 0 = A + (U2 – U1), отсюда U1 – U2 = A = 300 Дж.
Изменение внутренней энергии DU = = U2 – U1 = т 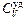 DТ, так как внутренняя энергия данного газа определяется только изменением его температуры и не зависит от процесса. А значит, оно точно такое же, как при изохорическом процессе. DТ, так как внутренняя энергия данного газа определяется только изменением его температуры и не зависит от процесса. А значит, оно точно такое же, как при изохорическом процессе.
|
| (U1 – U2) = ? (Т1 – Т2) = ? |
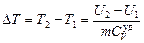 .
.
Тогда 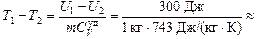 0,4 К.
0,4 К.
Ответ: U1 – U2 = A = 300 Дж; 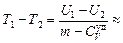 0,4 К.
0,4 К.
Читатель: Если одноатомный газ изотермически расширяется, то чему равна его теплоемкость?
Автор: 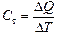 , так как
, так как 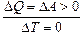 , то Ст ®¥ !
, то Ст ®¥ !
Читатель: А если одноатомный газ адиабатически расширяется, то в этом случае чему равна его теплоемкость?
Автор: 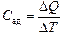 . При адиабатическом процессе температура понижается DТ < 0, а DQ = 0, поэтому
. При адиабатическом процессе температура понижается DТ < 0, а DQ = 0, поэтому 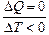 , Сад = 0 !
, Сад = 0 !
Дата добавления: 2016-04-11; просмотров: 2491;
