Связь строения с действием.
· Для проявления противомикробной активности необходимо наличие 4- аминобензолсульфамидного радикала, -NH2 и -SO2NH2 должны находиться в пара-положении. В противоположенном случае антимикробная активность не проявляется.
· Введение заместителей в аминогруппу позволяет получать препараты направленного действия (избирательного) – фталазол, салазопиридазин.
· При замене ариламиногруппы на -СН3, -Cl и другие заместители характер действия меняется, и вместо антибактериального действия проявляется гипогликемическая активность.
· Замена атома водорода в сульфамидной группе приводит к изменению характера действия, например, введение ацетильного радикала ускоряет действие препарата. Препараты с гетероциклическими радикалами оказывают более длительное действие. Продолжительность действия возрастает, если ввести электронодонорные заместители в гетероцикл (сульфален – сверхдлительное действие).
Получение
· Все препараты получают синтетически.
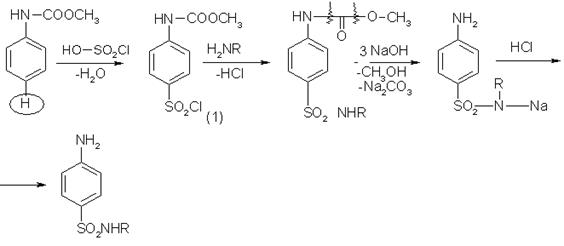
(1)-Реакция аминирования ацетильного производного n-аминобензол сульфохлорида
· Получение сульфацил-натрия
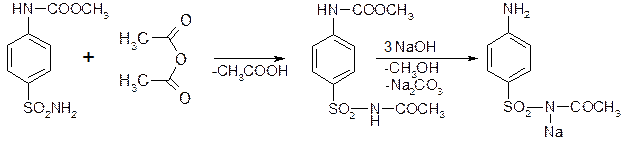
· Фталазол и фтазин получают из норсульфазола ацилированием фталевым ангидридом.
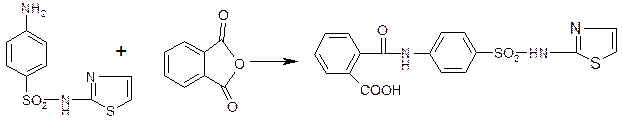
· Салазопиридазин получают из сульфапиридазина.

Химические свойства.
Все препараты проявляют амфотерные свойства.
Основные свойства проявляются за счет первичной ароматической аминогруппы, как основание они растворяются в минеральных кислотах с образованием солей. Основные свойства выражены слабо, соли неустойчивы и в воде легко гидролизуются.
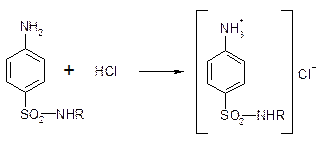
Кислотные свойства обусловлены сульфамидной группой, для которой характерна амид-иминная таутомерия:
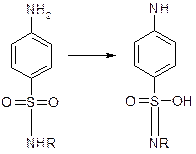
Амидная форма Ацифома
(р-p-сопряжение)
Считают, что в кристаллическом состоянии сульфаниламиды существуют в амидной форме, однако при действии на них раствора NaOH образуется ациформа. Атом водорода замещается на Na. Кислотные свойства выражены сильнее, препараты реагируют с СО32-. Na-соли ациформы устойчивы.
Растворимость.
Сульфаниламидные препараты в кислотной форме не растворяются в воде, растворимы в полярных органических растворителях, в растворах щелочей и карбонатов щелочных металлов.
Препараты в виде Na-солей легко растворимы в воде.
Т.к. сульфаниламидные препараты кислотные свойства проявляют сильнее, то это следует учитывать при назначении препарата. Во избежание побочных действий рекомендуется щелочное питье.
Идентификация.
Основана на наличии функциональных групп в молекуле.
· Первичная ароматическая группа
· SE-реакции (по бензольному кольцу)
· Замещенная аминогруппа
1. На первичную аминогруппу.
а) с ароматическими альдегидами (бензальдегидом, ванилином) образуется основание Шиффа. Реакцию можно проводить после гидролиза. Обычно наблюдаются желто-оранжевое окрашивание.
б) реакция диазотирования (красно-оранжевое окрашивание)
2. Реакции комплексообразования
с Fe3+(FeCl3), Cu2+(CuSO4), Co2+(СoCl2) с образованием окрашенных соединений. Атом водорода замещается на катион металла. В кислотно-основное взаимодействие вступает ациформа, которая получается при растворении препарата в 0,1М NaOH без избытка. На характер протекания реакции оказывает влияние заместители в сульфамидной группе. В случае гетероцикла, возможно образование внутримолекулярной связи и комплексные соединения не растворяются в воде.
3. Наличие серы в препарате доказывают путем окисления до S6+ кипячением в HNO3 до SO42-, который определяют с BaCl2.
4. На ароматический цикл.
Аминогруппа сульфаниламидного препарата – электронодонорный ориентант Ι рода, активирующий бензольное кольцо в реакции SE.
С количественным выходом протекает реакция бромирования (согласованная ориентация):
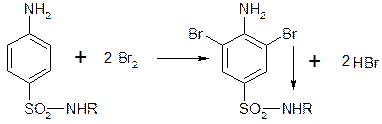
5. Реакция пиролиза (Селисеного) – разложение органических веществ, при длительном повышении температуры без доступа воздуха. Обычно эти реакции сопровождаются образованием плава, остатка характерного цвета, и выделением газообразных веществ. Цвет плава зависит от структуры препарата.
- стрептоцид образует плав фиолетового цвета, запах аммиака;
- норсульфазол, фталазол – плав бурого цвета, запах Н2S.
6. В солевых формах препаратов определяют катион Na+ (пламя горелки окрашивается в желтый цвет).
7. Физические свойства (Тпл., спектры)
Дата добавления: 2016-03-27; просмотров: 895;
