Анализдің физика – химиялық әдістері
Анализдің химиялық әдістері қазіргі таңның талабына сай емес. Технологиялық және биологиялық процесстерді басқару үшін анализдің жылдам әдістерін қажет етеді. Анализдің физика-химиялық әдістері (немесе инструментальдік) үлкен сезімталдығы мен жылдам орындалуымен ерекшелінеді. Олар заттардың физика химиялық қасиеттерін қолдануына негізделген [34].
Физика химиялық әдістермен анализдеуді орындау кезінде стехиометриялылық нүктені (эквиваленттік нүкте) визуальдік түрде емес, эквиваленттік нүктеде зерттелетін заттың физикалық қасиетінің өзгеруін тіркейтін прибор көмегімен анықтайды. Осы мақсат үшін күрделі оптикалық немесе электрлік схемалы приборлар қолданылады, сондықтан оларды инструментальдік анализдеудің әдістері деп атайды.
Анализдің инструментальді әдістері аналитикалық химияда маңызды орын алады, қоршаған ортаның ластануын бақылау кезінде маңызды роль атқарады. Қазіргі таңдағы аналитикалық химия физика, кванттық механика жетістіктерін кеңінен қолданады.
Негізгі физика химиялық әдістерінің ішінен анализдің электрохимиялық, оптикалық және хроматографиялық әдістері кеңінен қолданылады.
Анализдің электрохимиялық әдістері электрод бетінде немесе электрод алды кеңістігінде жүретін процестерді қолдануға негізделген. Анализденетін ерітінді концентрациясымен функциональді байланысқан және өлшеуге болатын кез келген электрлік параметр (потенциал, ток күші, кедергі және т.б.) аналитикалық сигнал бола алады [41].
Анализдеудің оптикалық әдістері анализденетін заттың оптикалық көрсеткіштерін өлшеуге, сәулеленумен, сіңірумен немесе сәуле (сәулелі) энергиясының шағылуымен бірге жүретін электромагниттік сәулеленудің заттың атомдары немесе молекулаларымен әрекеттесуін зерттеуге негізделген.
Хроматографиялық әдістер құрамы мен құрылымы жақын немесе ұқсас заттардың сорбенттермен сіңіруінде белгілі бір айырмашылығын анықтауға негізделген. Бұл қоспадағы жеке компоненттердің мөлшерін жылдам және анық анықтайтын заманауи әдіс компоненттерді концентрлейді және идентифицирлейді. Әдіс тамақ өнімдерін бақылауда, заттарды тазалауда, пестицидтерді табуды және т.б. кеңінен қолданылады.
Тамақ өнімін сертификациялау кезінде биологиялық құндылықтың, дәм және иістің анықтаушы мәні бар. Бұл сипаттаманың сенсорлық бағасы толық субъективті және белгілі бір уақытты талап етеді. Биологиялық құндылық өнімнің энергиялық қабілеттілігін, тамақ өнімдерінің құрамын (көмірсулар, ақуыздар, майлар, минералдық тұздар, микроэлементтер және т.б.) анықтайтын компоненттердің жиынтығымен анықталады. Тамақ өнімдерінің дәмі мен иісі негізінен молекулалық, иондық және атомдық деңгейдегі бейорганикалық және органикалық қосылыстардың (қышқылдар, спирттер, альдегидтер, кетондар және аз және өте аз дозадағы басқа да қосылыстар) үлкен жиынтығымен сипатталады [43].
Өнімнің дәмі мен иісін бағалау негізінен дегустацияның ғылыми негізін қамтамасыз ететін «сенсорлық анализ» жолымен және де химиялық құрал қолдану арқылы аналитикалық әдіспен жүргізіледі. Тамақ өнімдерінің (мысалы, нан өнімдері, шарап, сыра т.б.) дәмі мен ароматын (иісін) бағалаудағы сенсорлық әдісті қолдану адамзат органдарының сезу қабілеттерінің аналитикалық әдістермен салыстырғанда жетік екендігін білдіреді. Бұл артықшылық сезімталдығымен және спецификалығымен белгіленеді.
Алайда соңғы жылдағы өнеркәсіптік электроника, микропроцессорлық пен есептеу техникасының жетістіктері сенім туғызады. Ол тамақ өнімдерінің иісі мен дәмін бағалауды арнайы инструментальдік әдістердің (спектральді анализ, хроматография, жеткілікті объективтік бағалайтын масс-спектрометрия) көмегімен аналитикалық әдістер арқылы шешімін табуға мүмкіншілік бар.
Хроматографиялық әдісі физикалық-химиялық әдістердің қатарына жатады. Әдістің жетістігі қолдану қарапайымдылығы, іс жүзіндегі тиімділігі, талғамының жоғарылығы, сезімталдығы, дәлдігі, тез орындалуы, әмбебаптығы сияқты қасиеттері жиынтығында болса керек. Хроматография әдісімен көптекті заттардың кез келген агрегат күйдегі және кең концентрациялық диапозондағы қоспасын талдауға болады.
Хроматография әр түрлі объектілерді сандық және сапалық тұрғыдан талдауға, қосылыстың физикалық-химиялық қасиеттерін оқып-үйренуге кейбір реакциялардың кинетикасын зертеп білуге мүмкіндік береді. Тез жүргізілген - хроматографиялық талдаумен көптеген технологиялық процестер реттеледі [41].
Мұнымен қатар, хроматографияны қоспа құрамындағы керекті қосылысты таза күйінде бөліп алу үшін колданады. Заттарды хроматографиялық бөлу әдісі сорбциялық процестерге негізделген. Сорбция - сұйық не қатты сіңіргіштердің (сорбеттер мен эксфогенттермен) өзіне газды, буды, аэрозолъды, сұйықты, еріген затгы сіңіру процесі. Бұған кері процесті десорбция (кері сорбция) деп атайды. Сорбция адсорбция фаза бетіндей сіңіру және абсорбция (фаза көлемінде сіңіру) процестерін қамтиды. Сорбцияны статистикалық және динамикалық жағдайда да жүргізуге болады. Статистикалық сорбция екі фазада салыстырмалы тыныштықта тұрған кезде басталып, сорбция заңы бойынша фазалар арасында заттың таралу тепе-теңдігі орнағанда аяқталады. Динамикалық сорбция қозғалыссыз фазаға қатысты қозғалатын фазаның тиісті бағытта орын ауыстыруы нәтижесінде кері сорбция процесі кезінде басталады. Динамикалық жағдайдағы қоспаның бөлінуі әсерлі өтеді. Сорбциялық құбылыс таралу тұрақтылығымен сипатталынады:
КD=C1:C2
мұндағы С1 мен С2, - қозғалмайтын және қозғалысты фазаларға сәйкес бір пішіндегі заттардың тепе-теңдік концентрациясы. Әр түрлі фазадағы заттар әр түрде болатындықтан, таралу коэффициентін қолданған жөн.
К= 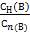
мұндағы СН(В) және Сn(В) - қозғалмайтын және қозғалысты фазалардағы сәйкес В затының жалпы аналитикалық концентрациясы. Хромаграфистер есептеу жүргізгенде сыйымдылық коэффициентін пайдаланады:
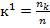
мұндағы nk мен n - қозғалмайтын және қозғалысты фазадағы құрылымның мольдік саны, k' - сыйымдылық коэффициенті. Бұл коэффициент берілген хроматографиялық жүйедегі құрама бөлікті ұстап тұру дәрежесін сипаттайды.
1 және 2 құрама бөліктің бөлу дәрежесі бөлу коэффициентімен өрнектеледі [43]:
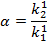
Қозғалмайтын фазада еріген заттың мөлшері неғұрлым көп болса, соғұрлым оны шаймалауға уақыт та көп кетеді. k'-тің индексі заттың шаймалау ретін көрсететіндіктен, α ылғи да бірден артық.
Үлгіні жақсы бөлу үшін, бағанаға сәл-пәл үлесін енгізу қажет. Бұл оның құрамындағы әр құрамдас бөліктердің бір мезгілде жылжи бастауына керек.
Қоспаның құрамдас бөліктерге бөлінуі олардың бағана бойымен жылжу процесі кезінде өтеді, сондықтан да ұзын бағана шоқтықтардың анық болуына септігін тигізеді, бірақ та бұл жағдай бойлық диффузияның әсерінен әрбір құрамдас бөліктердің орналасқан қозғалыс аймағының жайылып кетуіне келтіреді. Шоқтықтардың сүйірлену дәрежесі, құрамдас бөліктің бағанада болу уақытының квадратты түбіріне пропорционал, шоқтық неғұрлым енді болса, соғұрлым олардың жағдайы көмескілеу анықталады, сондықтан да іс жүзінде бағана ұзындығын шектейді.
Хроматографиялау процесінің басынан бастап осы берілген құрамдас бөлікке сәйкес шоқтықтың ең биігінің айқындалу уақытына әрбір құрамдас бөліктің ұсталу уақыты дәл келеді. Бұл t'A немесе t'В деп белгіленеді. Іс жүзінде анықталатып және қозғалыссыз фазамен әрекеттеспейтін құрамдас бөліктердің ұсталу уақыттарының айырмасын жиі пайдаланады және мұны өлі уақыт деп те айта береді:
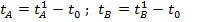
Суреттегі һ және h/2-мен белгіленген деңгейлер (биіктіктер) қисықтың иілу нүктесі арқылы жүргізілген жанама түзуден пайда болған үшбұрыштың толық және жартылай биіктігінде болады да, хроматографиялық шоқтық биіктігіне (жартылай биіктігіне) сәйкес келеді. Хроматографияда шоқтықтың толы өнін және жарты биіктігінің жартысына дейінгі деңгей ені W және w/2 арқылы белгілейді. W шамасы жекеленген молекулалардың ұсталу уақытының статистикалық өлшемі болып табылады. Орта мәннен ( 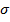 ) стандартты ауытқу, шоқтықтың жарты биіктігінің оның жарты еніне тең, яғни
) стандартты ауытқу, шоқтықтың жарты биіктігінің оның жарты еніне тең, яғни 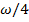 . Шоқтық ені мен ұсталу уақытының қатынасы мына теңдеу арқылы өрнектеледі:[1]
. Шоқтық ені мен ұсталу уақытының қатынасы мына теңдеу арқылы өрнектеледі:[1]
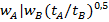
Хроматография тамақ өнімдерінің дәмі мен иісін анализдеудің әмбәбап инструментальдік әдістердің бірі. Наннан оның дәмі мен иісін түзуге қатысатын 211 қосылыс табылғаны, ал шарап құрамынан одан да көп қосылыс табылғаны белгілі.
Хроматография қозғалыста және қозғалмайтын фазадан тұрады; екі фаза арасында компоненттер тең таралады және қозғалмайтын фазада анализденетін ағынқозғалыста болады.
Сорбцияның 4 түрі белгілі:
- абсорбция – сұйық фазамен немесе барлық көлеммен газдарды буды сіңіру;
-адсорбция – қатты немесе сұйық сорбент бетімен затты сіңіру;
-хемосорбция – химиялық қосылыс түзетін қатты немесе сұйық сорбентпен заттарды сіңіру;
-капиллярлы конденсация – заттардың буын сіңіру кезінде қатты сорбент кеуегінде және капиллярында сұйық фазаның түзілуі.
Дата добавления: 2016-03-22; просмотров: 5394;
