Производные энергии Гиббса по температуре
и давлению
Выше шла речь об энергии Гиббса применительно только к изотермо- изобарным процессам в закрытых системах, где данная функция является термодинамическим потенциалом.
Однако величину ΔG можно рассматривать в любом процессе. От каких параметров и как тогда она зависит?
а) Согласно определению (4.7, а),
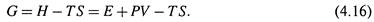
б) Отсюда изменение энергии Гиббса на микростадии произвольного процесса таково:

в) Пусть процесс является обратимым (т. е. на каждой микростадии система находится в состоянии равновесия) и пусть возможная работа совершается только против давления. Тогда, в соответствии с (1.7) и (3.4),
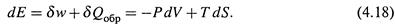
г) С учетом этого в выражении (4.17,б) три подчеркнутые члена сокращаются, давая в сумме ноль. Остается следующее:

Отсюда вывод: энергия Гиббса равновесного процесса (и равновесной системы) зависит от двух независимых переменных — давления и температуры (чего, в общем, и следовало ожидать).
д) Соответствующие частные производные таковы:

т.е. температурная зависимость энергии Гиббса определяется энтропией системы, а зависимость от давления — объемом системы.
Дата добавления: 2016-03-20; просмотров: 1519;
