Окисление циклоалканов до спиртов и кетонов
Наиболее важное промышленное значение имеет окисление циклогексана в циклогексанол и циклогексанон:
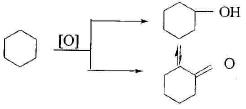
Оба продукта имеют самостоятельное значение. Циклогексанол используется для получения фенола и адипиновой кислоты. Циклогексанол для получения e-капролактама:

Так как целевые продукты окисления легко окисляются, процесс ведут в недостатке кислорода (3-4 %), конверсия ЦГ низкая 4-5%. Процесс протекает в каскаде 3-4 барботажных колони при 120-160 °С и 1-2 МПа. В качестве катализатора используются соли кобальта (III). Побочно образуются кислоты, гликоли, кетоспирты, сложные эфиры вплоть до СО2.
Кроме ЦГ окислению в спирты могут подвергаться и высшие нафтены.
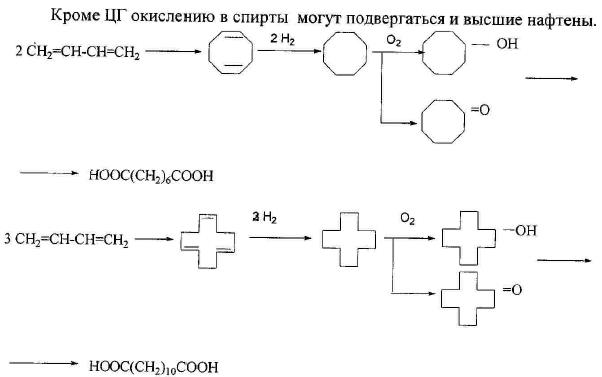
Циклодимеризация бутадиена-1,3 в циклооктадиен-1,5 протекает при 160-200 °С и 4 МПа в присутствии металлокомплексного катализатора (С6Н5)3Р*Ni(СО)4 и его циклотримеризация в циклододекатриен-1,5,9 - при 50-60 °С в присутствии катализатора Циглера-Натта Al(C2H5)2Cl*TiCl4. Эти продукты гидрируют, а затем окисляют кислородом воздуха до спиртов и кетонов C8 и С12. Из циклооктана получают пробковую кислоту, а из циклододекана - додекандикарбоновую кислоту.
Концентрация кислорода в смеси составляет 3-4 % Для предотвращения переокисления спиртов в смесь добавляют борную кислоту.

Конверсия 30 %. Соотношение спирт:кетон = 9:1.
Другие нафтены мало доступны, и высшие дикарбоновые кислоты получают при окислении или щелочном расщеплении высших ненасыщенных кислот, их сложных эфиров или содержащих их природных масел (касторовое).
Дата добавления: 2016-03-10; просмотров: 2742;
