Глинистые минералы, их строение, свойства и значение в почвоведении.
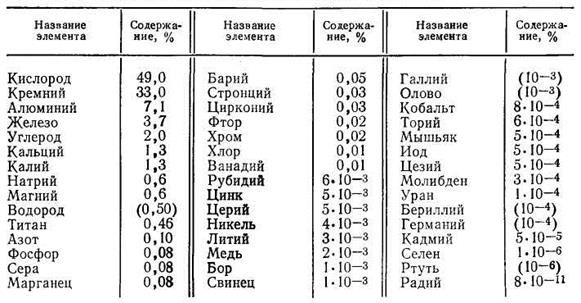
Почва более чем на девяносто процентов состоит из минеральных компонентов и содержит основной запас питательных веществ для растений. Почва является полидисперсной системой и имеет довольно сложный механический, минералогический и химический состав. В качестве примера в табл. 1.1 приведен средний химический состав твердой фазы почвы (по А. П. Виноградову).
Как видно из таблицы, почти половина твердой фазы почвы приходится на кислород, одна треть — на кремний, свыше 10% —на алюминий и железо и только 7% — на все остальные элементы. Из всех перечисленных элементов только азот (а также частично углерод, водород, кислород, фосфор и сера) содержится в органической части почвы. Все остальные элементы приходятся на минеральную часть почвы, которая состоит из большого числа различных минералов в виде частиц, имеющих размеры от 10-9 до 10-3 м и более.
Все минералы, содержащиеся в почве, по происхождению подразделяются на первичные и вторичные. Первичные минералы имеют преимущественно магматическое происхождение. Из них наиболее распространены в почвах кварц (окись кремния), полевые шпаты, амфиболы, пироксены и слюды, т. е. минералы, включающие
Таблица 1.1 Средний химический состав твердой фазы почвы
кислородные соединения кремния. Эти минералы составляют основную массу магматических и почвообразующих пород. В почвах первичные минералы обычно присутствуют в виде более или менее крупных частиц размером от 10-3 до 10-6 м, и только очень незначительная часть их имеет более высокую степень дисперсности.
Первичные минералы в условиях земной поверхности неустойчивы и под действием сил выветривания переходят в более устойчивые соединения — вторичные минералы. Процесс выветривания протекает под влиянием как чисто физических (колебания температуры, ветер, движущая сила воды), так и химических и биологических факторов. В результате этого из первичных минералов могут образоваться вторичные минералы простого состава: гидроксиды железа (II) и (III), алюминия, гидроксид кремния и некоторые другие соединения.
Кроме того, в процессе выветривания образуются также вторичные минералы более сложного строения (алюмо- и феррисиликаты). Эти последние более высокодисперсны, чем первичные, и имеют исключительно важное значение в создании основного свойства почвы — ее плодородия.
Все вторичные минералы сложного состава имеют пластинчатое строение и содержат химически связанную воду. Поскольку эти минералы являются важнейшей составной частью различных глин, они получили название глинистых или глинных минералов.
Число глинистых минералов довольно велико, но в почвах наиболее широкое распространение и значение для плодородия имеют в основном три группы минералов: каолинитовая, монтмориллонитовая и гидрослюдистая.
К минералам каолинитовой группы относятся каолинит [Al2Si2O5(OH)4] и галлуазит [Al2Si2O5(OH)4·2H2O], а также некоторые другие минералы. Каолинитовые глины содержат примерно 20—25% илистых частиц (меньше 0,001 мм), из них 5—10% частиц коллоидных размеров (меньше 0,25 микрона). Минералы этой группы довольно часто встречаются во многих типах почв. Они имеют сравнительно небольшую набухаемость и липкость.
Из минералов монтмориллонитовой группы в почвах наиболее распространены монтмориллонит [Al2Si4O10(OH)2·nH2O], бейделлит [Al2Si3O9(OH)3·nH2O], нонтронит [Fe2Si4O10(OH)3 ·nН2О] и некоторые другие. Монтмориллонитовые глины обладают в отличие от каолинитовых высокой набухаемостью, липкостью и связностью. Для них весьма характерным признаком является высокая степень дисперсности (до 80% частиц меньше 0,001 мм, из которых 40—45% меньше 0,25 микрона).
Среди глинистых минералов, встречающихся в почвах, большое место принадлежит минералам группы гидрослюд. В эту группу входят гидромусковит (иллит) {KAl2[(Si, Al)4O10](OH)2·nH2O}, гидробиотит {K(Mg, Fe)3 [(Al, Si)4O10] (OH)2·nH2O} и вермикулит {(Mg, Fe2+, Fe3+)2[(A1, Si)4O10](OH)2 ·4H2O}.
Глинистые минералы различаются по структуре.
Кристаллическая решетка различных глинистых минералов построена из одних и тех же элементарных структурных единиц, состоящих из атомов кремния и кислорода, а также из атомов алюминия, кислорода и водорода. Кроме перечисленных выше элементов в состав глинистых минералов могут входить Fe, Mg, К, Мn и др. В подавляющем большинстве глинистые минералы имеют слоистое строение и относятся к слоистым силикатам. Как показали новейшие рентгенографические и электронографические исследования, слои глинистых минералов состоят из сочетания кремнекислородных и кислород-гидроксилалюминиевых соединений.
Установлено, что важнейшие физико-химические и водно-физические свойства почвы — емкость поглощения, гидрофильность, связность, липкость, реакция среды и многие другие — находятся в прямой зависимости от минералогического состава. Теперь известно, что доступность для растений тех или иных питательных элементов в значительной мере зависит от вида минералов, содержащихся в почве, и от степени их дисперсности.
Глинистые минералы в основном сосредоточены в илистой (менее 1 мкм) фракции почв. Составом и строением минералов этой фракции в значительной степени определяется поглотительная способность почвы по отношению к катионам и анионам. Чем выше емкость поглощения почвы, тем больший запас питательных элементов в ней сосредоточен, следовательно, лучше ее потенциальное плодородие.
Минералы группы монтмориллонита обладают не только наибольшей степенью дисперсности, но и наибольшей поглотительной способностью (1,0—1,5 мкг-экв/кг). Эти минералы способны сильно набухать и содержат до 30% связанной воды, которая не может усваиваться растениями. Присутствие минералов монтмориллонитовой группы в почвах всегда положительно сказывается на растениях, обеспечивает большее содержание в них необходимых питательных элементов. Однако почвы, очень богатые монтмориллонитом, имеют невысокую агрономическую ценность. При высыхании таких почв образуются трещины, водопроницаемость их становится неодинаковой, на поверхности образуется прочная корка. Эти отрицательные свойства монтмориллонита особенно сильно проявляются на почвах, бедных гумусом. При достаточном количестве гумуса физико-химические свойства такой почвы значительно улучшаются за счет образования водопрочных органо-минеральных агрегатов. Практика показывает, что добавление в сильно деградированные песчаные почвы глин, содержащих минералы монтмориллонитовой группы, положительно сказывается на плодородии.
Минералы каолинитовой группы по своим свойствам резко отличаются от монтмориллонита. Каолинит обладает очень малой емкостью поглощения (0,07— 0,10 мкг-экв/кг); он практически не набухает и содержит весьма незначительное количество воды. Почвы, в которых много этого минерала, вследствие малой емкости поглощения отличаются низким плодородием. Сам каолинит не содержит поглощенных оснований и поэтому не является источником питания для растений. Почвы, содержащие много каолинита, хорошо отзываются на внесение в них калия и других оснований.
Минералы группы гидрослюд чрезвычайно богаты легкодоступным для растений калием (до 6—7%). Емкость поглощения гидрослюд в несколько раз выше, чем у каолинита, но в два-три раза меньше, чем у монтмориллонита. Почвы, содержащие много гидрослюдистых минералов, практически не нуждаются в калийных удобрениях.
В трудах многих ученых отмечается активное участие глинистых минералов в повышении степени доступности фосфатов почвы, калия и микроэлементов. Наличие в почвах полуторных оксидов, а также токсичного для растений подвижного алюминия обусловлено составом и строением высокодисперсных (в том числе и глинистых) минералов. Таким образом, качественный и количественный состав вторичных минералов имеет одно из первостепенных значений в создании основного свойства почвы — ее плодородия.
§7. Характеристика жидкого агрегатного состояния.
Жидкости по своим свойствам занимают промежуточное положение между твердыми телами и газами и сходны как с теми, так ис другими. По некоторым свойствам жидкости сходны с газами: они текучи, не имеют определенной формы, аморфны и изотропны, т. е. однородны по своим свойствам в любом направлении. С другой стороны, жидкости обладают объемной упругостью, как твердые тела. Они упруго противодействуют не только всестороннему сжатию, но и всестороннему растяжению. Молекулы их стремятся к некоторому упорядоченному расположению в пространстве, т. е. жидкости имеют зачатки кристаллического строения.
Жидкости отличаются высокой текучестью и принимают форму того сосуда, в котором они находятся.
Средней кинетической энергии молекулы жидкости вполне хватает, чтобы совершать перескоки из одного положения равновесия в другое, но этой энергии явно недостаточно для того, чтобы полностью преодолеть силы взаимодействия окружающих молекул. Из жидкости вырывается лишь небольшое число наиболее быстрых молекул (процесс испарения). Тепловые движения молекул жидкости не выходят за пределы действия когезионных сил, поэтому жидкости имеют постоянный объем.
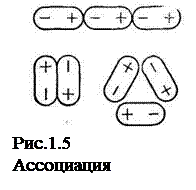 Огромную роль в свойствах жидкостей играет объем молекул, их форма и полярность. Если молекулы жидкости полярны, то происходит ассоциация (объединение) двух или более молекул в сложный комплекс (рис. 1.5). В таких жидкостях, как вода, жидкий аммиак, большую роль в ассоциации молекул играет наличие так называемой водородной связи.
Огромную роль в свойствах жидкостей играет объем молекул, их форма и полярность. Если молекулы жидкости полярны, то происходит ассоциация (объединение) двух или более молекул в сложный комплекс (рис. 1.5). В таких жидкостях, как вода, жидкий аммиак, большую роль в ассоциации молекул играет наличие так называемой водородной связи.
Свойства жидкостей в значительной мере зависят от степени ассоциации их молекул. Как показывает опыт, ассоциированные жидкости обладают более высокой температурой кипения, меньшей летучестью. С повышением температуры комплексы распадаются и тем сильнее, чем слабее силы взаимодействия молекул в комплексе.
Как уже упоминалось в начале этой главы, существуют и так называемые кристаллические жидкости или жидкие кристаллы, которые, будучи жидкостями, обладают, как и кристаллические вещества, анизотропными свойствами. Различают термотропные и лиотропные жидкие кристаллы.
Следует отметить, что частичная упорядоченность молекул характерна для целого ряда биологически важных веществ — белково-липидных систем, холестерина, некоторых солей жирных кислот и т. п. Строгая упорядоченность, вообще характерная для биологических систем, также определяется особым типом организации макромолекулярных структур и по своей сущности является динамической. В живом организме эта упорядоченность поддерживается за счет равновесия между непрерывно идущими процессами распада и образования вещества и связана с увеличением энтропии той системы, в которой находится организм.
§8. Внутреннее трение (вязкость) жидкостей.
Всякое тело при движении испытывает сопротивление среды, в которой оно движется. Если перемешивать стеклянной палочкой воду, сахарный сироп, глицерин, мед и т. п., ощущается сопротивление движению палочки. Сила, противодействующая движению тела, носит название силы трения.
Когда тело испытывает сопротивление движению со стороны своих же частиц, противодействующая сила называется внутренним трением или вязкостью. Таким образом, вязкость — это внутреннее трение, проявляющееся при относительном движении соседних слоев жидкости и зависящее от сил сцепления (взаимодействия) между молекулами. Во всех жидкостях при перемещении одних слоев относительно других возникают более или менее значительные силы трения, направленные по касательной к поверхности этих слоев. Сила внутреннего трения F прямо пропорциональна площади S трущихся друг о друга слоев жидкости и скорости их движения dU и обратно пропорциональна расстоянию этих слоев dx один от другого:
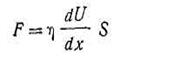
| 1.30 |
(формула Ньютона), где η) — коэффициент пропорциональности.
Если площадь S=l м2, dU/dx= 1, то F = η и носит название коэффициента вязкости или коэффициента внутреннего трения. Этот коэффициент зависит от природы жидкости и ее температуры. Из уравнения (I,30) определяем
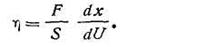
| 1.31 |
При выражении силы трения F в ньютонах, dx в м, dU в м/с, a S в м2, получим
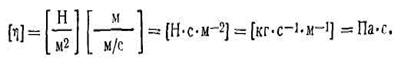
Вязкость является величиной, характерной для данной жидкости.
Жидкости, подчиняющиеся уравнению (I.31), получили название ньютоновских. Однако есть жидкости, которые не подчиняются этому уравнению, например растворы высокомолекулярных соединений.
Вязкость жидкостей в значительной степени зависит от температуры: с повышением её вязкость жидкости понижается.
Величина, обратная вязкости, т. е. 1/η, называется текучестью. Эфир, этиловый спирт являются легкотекучими или легкоподвижными, а глицерин, деготь — труднотекучими, или, иначе, малоподвижными жидкостями.
Значение вязкости в природе очень велико. В биологических системах она влияет на протекание ряда важнейших процессов в живом организме. Большую роль вязкость играет в различных технологических процессах в промышленности. В частности, скорость движения различных жидкостей по трубам в основном зависит от вязкости транспортируемой жидкости.
С понижением вязкости жидкости при нагревании связано повышение электрической проводимости растворов электролитов (проводников второго рода).
Дата добавления: 2016-02-20; просмотров: 5590;
