БИОТЕХНОЛОГИЧЕСКИЕ ПРОЦЕССЫ В ПИЩЕВОЙ ПРОМЫШЛЕННОСТИ 13 страница
6.6. МОРФОГЕНЕЗ В КАЛЛУСНЫХ ТКАНЯХ КАК ПРОЯВЛЕНИЕ ТОТИПОТЕНТНОСТИ РАСТИТЕЛЬНОЙ КЛЕТКИ
Дифференцировка каллусных тканей. Одна из наиболее интересных, но сложных проблем в биологии — развитие многоклеточных организмов. Изучение данного вопроса возможно несколькими путями. Так, большое распространение получило моделирование процессов онтогенеза на более простых системах. При этом используют изолированные ткани, клетки, протопласты, культивируемые в стерильных условиях. Преимущество этого процесса состоит в том, что нет необходимости постоянно учитывать результаты взаимодействия органов в целостной системе растительного организма. Кроме того, экспериментатор сам имеет возможность выбирать, изменять и повторять условия опыта в соответствии с поставленной задачей. После завершения дедифференци- ровки дальнейшее развитие каллусной клетки может идти в нескольких направлениях. Во-первых, это вторичная дифференци- ровка разной степени сложности. Во-вторых, в клетке может сформироваться состояние стойкой дедифференцировки («привыкание»), а следовательно, способность расти на безгормональной среде. В-третьих, каллусная клетка проходит свой цикл развития, завершающийся ее старением и отмиранием.
Наибольший интерес вызывает первый путь, фактически представляющий морфогенные процессы. В культуре каллусных тканей морфогенезом называют возникновение организованных структур из неорганизованной массы клеток.
Вторичная дифференцировка каллусной клетки может завершиться образованием в каллусной ткани отдельных дифференцированных клеток. Они имеют определенное строение и выполняют специфические функции. Примером служит образование эпибла- стов — клеток, в которых запасаются вторичные метаболиты. Это наиболее простой тип дифференцировки каллусной клетки. Более сложная гистологическая дифференцировка завершается образованием в каллусе различных тканей: млечников, волокон, трихом, элементов ксилемы (трахеи и трахеиды) и флоэмы (ситовидные трубки и клетки-спутницы). К самым сложным видам вторичной дифференцировки относятся органогенез — образование органов и соматический эмбриогенез — образование из соматических клеток эмбриоидов, биполярных зародышеподобных структур. Все эти типы дифференцировки возможны только благодаря тотипотентности: любая растительная клетка содержит полный набор генов, характерный для того организма, из которого она была выделена. Потенциальные возможности всех клеток этого растения одинаковы; каждая из них в определенных условиях может дать начало целому организму. Однако выяснено, что реально детерминируется только одна из 400—1000 клеток, что, вероятно, связано с физиологическим состоянием клетки, с ее компетентностью. Так, у эксплантов стеблевого происхождения компетентны к действию экзогенных фитогормонов и, следовательно, способны к морфогенезу только клетки эпидермальных и субэпидер- мальных тканей (Тран Тан Ван, 1981). Однако компетентность клеток может приобретаться ими в процессе культивирования каллусной ткани, в условиях, индуцирующих морфогенез. Время, в течение которого в каллусных клетках возникает это свойство, изменяется в широких пределах. Кроме того, существенную роль в дифференциации играют генотип растения-донора, условия и физические факторы культивирования.
Все каллусные клетки, готовые ко вторичной дифференциров- ке, т.е. детерминированные, характеризуются общими чертами. Эти клетки — «клетки-инициали»— образуют утолщенную клеточную стенку, обособляясь от остальных каллусных клеток. Для них характерно более крупное ядро, большее количество запасных веществ, меньшие размеры вакуолей. В «клетках-инициалях» начинается синтез определенных белков, интенсифицируется пенто- зофосфатный путь расщепления гексоз. Очень важно, что между этими клетками, формирующими меристематические очаги, восстанавливаются плазмодесмы, которые практически отсутствуют в массе каллусных клеток.
Интересное предположение было высказано JI. Саксом и С. Той- воненом (1963). Оно сводится к тому, что существует минимальная масса каллусных клеток, которая определяет способность уже детерминированных клеток к дальнейшему морфогенезу. Это подтвердилось в опытах с культурой семядолей ели: детерминация адвентивных побегов происходила в клеточных комплексах из 5 — 6 клеток (Б.С.Флинн и др., 1988). В исследованиях С.Номура и А. Комамине (1989) было показано, что развитие соматических зародышей детерминируется в 6 — 10-клеточном агрегате.
Гистогенез. Главную роль в преобразовании каллусных клеток в сосудистые элементы играют фитогормоны, в основном ауксины. Опыты по влиянию апикальной меристемы побега (место синтеза ауксинов) на гистогенез в каллусной ткани показали, что ниже места прививки апекса в каллусной ткани начинали образовываться сосудистые элементы. Тот же эффект наблюдался при нанесении на каллус ауксина с сахарозой. Интересно, что повышение концентрации сахарозы способствовало образованию элементов флоэмы, а понижение — образованию ксилемных элементов. Причем такое действие оказывала совместно с ауксином только сахароза, что позволяет говорить о ее регуляторной роли. Добавление к гормону других Сахаров гистогенеза не вызывало. В некоторых случаях стимуляторами гистогенеза помимо ауксинов могут быть и остальные фитогормоны. Так, было отмечено, что в каллусных тканях сои этот процесс начинается под действием гиббе- релловой кислоты и этилена.
Органогенез. Первые работы Ф.Скуга и С.Миллера по влиянию ауксинов и открытого ими кинетина на органогенез в каллусах растений показали прямую зависимость этого процесса от соотношения фитогормонов. Преобладание концентрации ауксина над цитокинином вызывает дифференцировку клеток, приводя-
протопласты — одни из наиболее ценных объектов в биотехнологии. Они позволяют исследовать различные свойства мембран, а также транспорт веществ через плазмалемму. Главное их преимущество состоит в том, что в изолированные протопласты достаточно легко вводить генетическую информацию из органелл и клеток других растений, прокариотических организмов и из клеток животных. Е. Коккинг установил, что изолированный протопласт благодаря механизму пиноцитоза способен поглощать из окружающей среды не только низкомолекулярные вещества, но и крупные молекулы, частицы (вирусы) и даже изолированные органеллы.
Большое значение в создании новых форм растений для изучения взаимодействия ядерного генома и геномов органелл имеет способность изолированных протопластов сливаться, образуя гибридные клетки. Таким способом можно добиться получения гибридов от растений с разной степенью таксономической удаленности, но обладающих ценными хозяйственными качествами.
Впервые протопласты были выделены Дж. Клернером в 1892 г. при изучении плазмолиза в клетках листа телореза (Stratiotes abides) во время механического повреждения ткани. Поэтому этот метод назван механическим. Он позволяет выделить лишь небольшое количество протопластов (выделение возможно не из всех видов тканей); сам метод длительный и трудоемкий. Современный метод выделения протопластов заключается в удалении клеточной стенки с помощью поэтапного использования ферментов для ее разрушения: целлюлазы, гемицеллюлазы, пектиназы. Этот метод получил название ферментативного.
Первое успешное выделение протопластов из клеток высших растений данным методом сделано Е. Коккингом в 1960 г. По сравнению с механическим ферментативный метод имеет ряд преимуществ. Он позволяет сравнительно легко и быстро выделять большое количество протопластов, причем они не испытывают сильного осмотического шока. После действия ферментов смесь протопластов пропускают через фильтр и центрифугируют для удаления неразрушенных клеток и их осколков.
Выделить протопласты можно из клеток растительных тканей, культуры каллусов и суспензионной культуры. Оптимальные условия для изоляции протопластов для разных объектов индивидуальны, что требует кропотливой предварительной работы по подбору концентраций ферментов, их соотношения, времени обработки. Очень важным фактором, позволяющим выделять целые жизнеспособные протопласты, является подбор осмотического стабилизатора. В качестве стабилизаторов обычно используют различные сахара, иногда ионные осмотики (растворы солей СаС12, Na2HP04, КС1). Концентрация осмотиков должна быть немного гипертонична, чтобы протопласты находились в состоянии слабого плазмолиза. В этом случае тормозятся метаболизм и регенерация клеточной стенки.
7 Г-'горова
Изолированные протопласты можно культивировать. Обычно для этого используют те же среды, на которых растут изолированные клетки и ткани. Сразу же после удаления ферментов у протопластов в культуре начинается образование клеточной стенки. Протопласт, регенерировавший стенку, ведет себя как изолированная клетка, способен делиться и формировать клон клеток. Регенерация целых растений из изолированных протопластов сопряжена с рядом трудностей. Получить регенерацию через эмбриогенез удалось пока только у растений моркови. Стимуляцией последовательного образования корней и побегов (органогенез) добились регенерации растений табака, петунии и некоторых других растений. Следует отметить, что протопласты, изолированные из генетически стабильной клеточной культуры, чаще регенерируют растения и с большим успехом используются при исследованиях генетической модификации протопластов.
6.8. ИСПОЛЬЗОВАНИЕ МЕТОДА КУЛЬТУРЫ
ИЗОЛИРОВАННЫХ КЛЕТОК И ТКАНЕЙ В СОЗДАНИИ СОВРЕМЕННЫХ ТЕХНОЛОГИЙ
Помимо фундаментальных исследований метод культуры изолированных тканей широко используется в сельском хозяйстве и промышленном производстве (рис. 6.5). Примером может служить массовое клональное микроразмножение плодовоовощных и декоративных растений, а также их оздоровление от вирусных и других инфекций. С помощью культуры in vitro можно расширить возможности селекционной работы: получать клоны клеток, а затем и растения с запрограммированными свойствами. Благодаря способности клеток синтезировать в культуре вторичные метаболиты возникла отрасль промышленности, осуществляющая биологический синтез веществ, необходимых человеку.
6.8.1. Синтез вторичных метаболитов
В настоящее время известно примерно 2-104 синтезируемых растениями веществ, которые используются человеком, и их количество постоянно увеличивается. Растения всегда служили источником пищи, эфирных масел, красителей и, конечно же, лекарственных соединений. Так, мак снотворный (Papaver somniferum)j является источником болеутоляющего вещества — кодеина; из на^ перстянки (Digitalis lanata) получают дигоксин, тонизирующий сер| дечную деятельность; из хинного дерева (Cinchona ledgeriana) -4 антималярийное средство «хинидин». Особое место занимают нар| котики и стимулирующие вещества. В небольших, строго контро! лируемых количествах их используют в медицине. Однако при сй|
Биотехнологическое применение
| Соматические эмбриоидьГ" |
| Клетки |
| 1 1 1 1г- | |
| II | |
| 1 1 | LlJi К |
| 11 | |
| И | |
| LU- |
| || L м н II___ |
. фундаментальные : исследования Вегетативное : размножение ■ Оздоровление
Искусственные семена
Вторичные продукты и биотрансформация
Гибридизация: половая,
соматическая
Гаплоидизация:
андро генная,
гиногенная
Селекция, мутации,
вариации
Замена органелл
| Меристемы, яйцеклетки, эмбрионы, микроспоры пыльники ===== н Каллус |

| Протопласты |
Молекулярно- генетическая инженерия растений
Рис. 6.5. Использование культуры клеток и тканей растений в биотехнологии (по Х.Борнман, 1991)
стематическом употреблении низких концентраций наркотиков возникают наркозависимость и стремление к увеличению употребляемой дозы. Применение высоких концентраций наркотика убивает человека. Наиболее известны опиум и героин из Papaver somniferum, кокаин из Erythroxylon, никотин из различных сортов табака. Наиболее известный стимулятор — кофеин, содержащийся в растениях чая и кофе. Стимуляторы не токсичны в концентрациях, рекомендуемых к применению. Однако высокие их концентрации негативно влияют на сердечно-сосудистую и нервную систему человека.
Большой интерес вызвало открытие пиретринов, выделенных из цветков Chrysanthemum cinerariaefolium. Эти вещества — мощные инсектициды. Особая их ценность заключается в том, что пиретрины не вызывают привыкания у насекомых, а также не проявляют кумулятивного токсического эффекта.
Способность интактных растений синтезировать различные соединения привела к предположению, что тем же свойством будут обладать клетки и ткани этих растений, выращиваемые в стерильных условиях. Для некоторых культур это оказалось справедливым. Но в отдельных случаях клетки либо не проявляли способности к синтезу необходимых веществ, либо синтезировали их в минимальных количествах. Понадобились долгие эксперименты по подбору питательных сред, условий культивирования, исследованию новых штаммов, полученных благодаря генетической гетероген
ности каллусных клеток или применению мутагенных фактороь чтобы добиться серьезных успехов в этой области.
В настоящее время промышленный синтез вторичных метабо литов — очень перспективное направление. Синтез вторичны: метаболитов происходит главным образом в суспензионной культуре клеток, в регулируемых условиях, поэтому он не зависит о~ климатических факторов, от повреждения насекомыми. Культурь выращивают на малых площадях в отличие от больших массивоь плантаций с необходимыми растениями. Культуры клеток растений могут синтезировать практически все классы соединений вторичного обмена, причем довольно часто в количествах, в нескольк< раз превышающих их синтез в целых растениях. Например, выхол аймалицина и серпентина в культуре клеток Catharanthus roseur составляет 1,3 % сухой массы, а в целом растении — 0,26 %. В культура- клеток Dioscorea deltoidea диосгенин синтезируется в количеств^ 26 мг на 1 г сухой массы, а в клубнях растений его содержание составляет 20 мг на 1 г сухой массы. Кроме того, в культурах ют- ток может начаться синтез веществ, не характерных для исходного растения, либо расширяется набор синтезируемых соединений В ряде случаев в клеточной культуре образуются вещества, которые синтезировались интактным растением на ювенильной фаз:- развития, либо вещества, содержавшиеся в клетках филогенетически более ранних групп растений. Так, в культуре клеток Papave bracteatum содержится сангвирин, характерный для ювенильны:. растений, и отсутствует тебаин, синтезируемый взрослыми растениями. А в культуре клеток живокости (Delphinium) синтезируются Д7-стерины, присутствующие у архаичных групп растений.
Синтез вторичных соединений может коррелировать с процессом дифференцировки в культуре клеток. Например, в суспензионной культуре Papaver somniferum максимальный синтез алкалоидов начинается после того, как в ней дифференцируется достаточна большое количество специализированных клеток млечников, предназначенных для депонирования метаболитов. С другой стороны, культуры клеток табака и моркови синтезируют большое количество никотина и антоцианина соответственно, хотя их клетки слабо дифференцированы. Не существует также однозначного ответа на вопрос, как связан синтез вторичных метаболитов с ростовым» процессами. У большого числа культур вторичные метаболиты син; тезируются и накапливаются в значительных количествах либо в? время экспоненциальной фазы, когда ростовые процессы особен* но активны, либо в период стационарной фазы роста культура клеток, когда прирост клеточной массы прекращается. Однако ecti культуры, например культура клеток Catharanthus roseus, у которь: синтез вторичных метаболитов сопровождает весь период роста. |
Важная особенность культивируемой популяции клеток — е стабильность в отношении синтеза и накопления продуктов вто| ричного синтеза. Так, в отделе биологии клетки и биотехнологии ИФР РАН под руководством Р. Г. Бутенко были получены разные штаммы клеток Dioscorea deltoidea, в том числе штамм-сверхпродуцент ИФР ДМ-0,5. Все эти штаммы сохраняли стабильность в отношении синтеза фуростаноловых гликозидов около 26 лет. Интересная особенность большинства клеток в культуре состоит в том, что обычно эти клетки не транспортируют синтезируемые метаболиты в питательную среду или другие клетки, хотя некоторые культуры составляют исключение, в частности культура клеток мака, которые депонируют алкалоиды в млечники. Синтез вторичных метаболитов в культивируемых клетках связан с внутриклеточными органеллами, в основном с пластидами и эндоплаз- матическим ретикулумом. В клетках, не способных к транспорту метаболитов, продукты вторичного синтеза обычно накапливаются в вакуолях и свободном пространстве (СП) клеток (табл. 6.3).
На синтез вторичных метаболитов влияет целый ряд факторов. Прежде всего выход продукта зависит от генотипа растения-до- нора. Показано, что культуры клеток, полученных от высокопродуктивных растений, продуцировали большее число метаболитов. Другой важный фактор — состав питательной среды и концентрация ее компонентов, которые должны обеспечивать, с одной стороны, увеличение количества клеток-продуцентов, с другой —
Таблица 6.3
Внутриклеточная локализация синтеза и накопления вторичных метаболитов (по Р.Г.Бутенко, 1999)
|
усиливать сам процесс синтеза. На рост, т.е. на увеличение биомассы, существенно влияет природа и количество углеводов, соединений азота и фосфора, на синтез метаболитов — природа и концентрация фитогормонов. Так, при замене одного ауксина на другой, например нафтилуксусной кислоты на 2,4-D, трехкратно увеличился синтез антрахинона суспензионной культурой Morinda citrifolia.
Очень большое влияние на рост суспензионной среды оказывает ее непрерывное перемешивание, которое обеспечивает хорошую аэрацию и предотвращает осаждение клеток. В лабораторных условиях перемешивание достигается благодаря использованию качалок или роллерных установок. При промышленном выращивании суспензионных культур применяют специальные системы, в которых идут увеличение биомассы и синтез вторичных соединений, — биореакторы. Эти системы обладают важными преимуществами: возможностью управлять процессом культивирования на основе показаний датчиков; кроме того, большой объем культивируемого материала позволяет забирать значительные пробы, при этом стрессовые реакции у культуры клеток не возникают. В зависимости от способа перемешивания культуральной жидкости биореакторы делят на две группы.
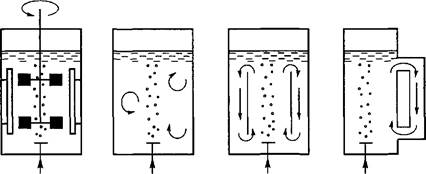
Первая группа включает биореакторы, в которых суспензионная культура перемешивается только за счет подачи воздуха; во второй группе биореакторов культура перемешивается механическим способом (рис. 6.6).
Выращивание культур растительных клеток в биореакторах проводят в двух режимах. Первый режим — периодическое культивиро-
 Воздух Воздух Воздух Воздух
1 2 3 4 \
}
Рис. 6.6. Схема работы основных типов биореакторов: f
Воздух Воздух Воздух Воздух
1 2 3 4 \
}
Рис. 6.6. Схема работы основных типов биореакторов: f
|
1 — биореактор с механическим перемешивающим устройством; 2 — барботаж-1 ный биореактор; 3 — аэролифтный биореактор; 4 — биореактор с вынесенной
циркуляционной петлей \
182 j вание — заключается в том, что по окончании процесса откачивают и используют всю суспензию клеток. При втором режиме — проточное культивирование — в биореактор постоянно добавляют свежую питательную среду и одновременно отбирают тот же объём либо суспензии (открытое проточное культивирование), либо одной отработанной питательной среды, оставляя клетки в реакторе (закрытое проточное культивирование).
Существуют две разновидности открытого культивирования. Первая — турбидостат — подразумевает измерение и автоматическое поддержание концентрации клеточной биомассы в реакторе на одном уровне путем изменения скорости протока. Вторая разновидность — хемостат — заключается в подаче в биореактор с постоянной скоростью питательного раствора при одновременном откачивании с той же скоростью клеточной суспензии.
Существует еще одна современная технология получения вторичных метаболитов с помощью иммобилизованных клеток культуры, т. е. помещение их в определенный носитель или адсорбция в нем. Носитель с клетками помещают в питательную среду. Клетки остаются живыми. Они прекращают рост, но продолжают синтез метаболитов, выделяя их в среду.
Довольно часто синтез вторичных метаболитов в суспензионной культуре останавливается на промежуточных этапах, не доходя до необходимого продукта. Получение продукта возможно благодаря процессу биотрансформации. Сущность его состоит в изменении промежуточных метаболитов с помощью культур других растений или клеток бактерий. Биотрансформация очень эффективна в бактериальных клетках, поэтому растительные клетки используют, когда процесс не осуществляется в клетках микроорганизмов. Вводимые в эти культуры вещества могут подвергаться гидроксилированию, эпоксидированию, глюкозилированию, этерификации, а также присоединяться к аминокислотам. Например, культура клеток женьшеня корневого происхождения способна трансформировать (гликозилировать) фенольные соединения — продукты деятельности суспензионной культуры клеток корня Panax ginseng. Культуры клеток лебеды и картофеля могут биотрансформировать индолил-3-уксусную кислоту в индолил-3- ацетил-Ь-аспарагиновую кислоту (Н. И. Рекославская и др., 1991).
Еще один пример — биотрансформация карденолидов, гликози- ды которых используют в медицине для лечения болезней сердца. Растения наперстянки (Digitalis lanata) в большом количестве синтезируют дигитоксин вместо необходимого дигоксина. Для соответствующей биотрансформации с успехом используют недифференцированную суспензионную культуру наперстянки. Иммобилизованные клетки этой культуры способны долгое время с постоянной скоростью трансформировать р-метилдигитоксин в р-метил- дигоксин (А. В.Альферманн и др., 1987).
Таким образом, использование суспензионных культур для синтеза вторичных метаболитов в промышленных масштабах имеет большие перспективы, и не только с точки зрения экономической выгоды получения более дешевой продукции в запланированных количествах. Важно, что использование культуры клеток спасет от уничтожения тысячи дикорастущих растений, ставших уже редкими, которые синтезируют необходимые человеку вещества. Увеличение выхода продукта может быть достигнуто благодаря дальнейшей исследовательской работе по селекции специализированных популяций клеток и оптимизации условий культивирования. Большой интерес представляет также дальнейшее развитие методов биотрансформации метаболитов и иммобилизации культивируемых клеток.
6.8.2. Биотехнологии в сельском хозяйстве
Ускорение и облегчение селекционного процесса, а также создание растений с новыми качествами — это направления, которые достаточно успешно развиваются с помощью технологий клеточной инженерии, культуры клеток и тканей.
Две группы методов, благодаря которым развиваются данные направления, представлены в табл. 6.4.
Некоторые из указанных технологий стали традиционными, другие находятся на начальных этапах разработки. Наконец, есть такие методы, которые явно вышли из ранга вспомогательных, ускоряющих селекцию технологий. К ним можно отнести крио- сохранение генофонда — технологию, в настоящий момент приобретшую экологическую направленность; или клональное микроразмножение растений, тесно связанное с проблемой их оздоровления от вирусных и других инфекций. Поэтому обзор этих технологий вынесен за рамки данного раздела.
Технологии, облегчающие селекционный процесс. Одна из наиболее важных технологий этой группы — оплодотворение in vitro, помогающее предотвратить прогамную несовместимость, которая может быть вызвана следующими причинами:
1) генетически детерминированное (определенное) несоответствие секрета рыльца материнского растения и пыльцы отцовского, которое тормозит рост пыльцевых трубок на рыльце пестика;
2) несоответствие длины столбика пестика и пыльцевой трубки, в результате чего пыльцевая трубка не достигает семяпочки (гетеростилия):
3) тканевая несовместимость партнеров, приводящая к остановке роста пыльцевой трубки в любой момент ее прорастания от рыльца пестика до микропиле семяпочки (гаметофитный тип несовместимости).
Таблица 6.4
Клеточные технологии в селекции растений (по Р. Г. Бутенко, 1999)
|
Преодоление прогамной несовместимости возможно благодаря выращиванию в стерильных условиях изолированной завязи с нанесенной на нее пыльцой или изолированных кусочков плаценты с семяпочками, рядом с которыми или непосредственно на ткани которых культивируется пыльца.
Значительным препятствием для селекции служит также пост- гамная несовместимость, вызванная разновременным развитием зародыша и эндосперма при отдаленной гибридизации. В результате образуются невсхожие щуплые семена. Получить растение из таких семян можно только при использовании метода эмбриокуль- туры, т.е. выращивания изолированного зародыша на искусственной питательной среде in vitro. Метод эмбриокультуры широко применяют при межвидовой гибридизации овощных растений, для микроразмножения ценных гибридов, для клеточной селекции.
Большое значение имеет создание гаплоидов, позволяющее ускорить процесс селекции в 2 — 3 раза. Использование гаплоидных клеток и гаплоидных растений способствует обнаружению экспрессии введенного в клетку генома, редких рекомбинаций, рецессивных мутаций, которые в диплоидных растениях, как правило, маскируются доминантными генами. Из гаплоидных клеток можно выделить протопласты; сливаясь, они образуют гибридные клетки и растения с диплоидным числом хромосом. Обрабатывая гаплоидные клетки колхицином, можно добиться удвоения числа хромосом и получить диплоидные гомозиготные растения. Все это значительно облегчает выявление и стабилизацию необходимых признаков. Кроме селекции гаплоиды применяются также в генно-инженерных исследованиях. Впервые возможность получения спонтанных гаплоидов при аномальном развитии пыльников, пыльцы и других объектов была показана в 1964 г. С. Гуха и С. Магешвари. В настоящее время в культуре гаплоидные растения получают из изолированных пыльников (андрогенез), изолированных семяпочек (гиногенез); из гибридного зародыша, у которого в результате несовместимости потеряны отцовские хромосомы (партеногенез). Новые сорта ячменя — Исток и Одесский-15 — были выведены благодаря комбинации партеногенетического метода с культурой изолированных зародышей за 4 года вместо 10—12 лет, необходимых для обычной селекции.
Создание генетического разнообразия исходных форм растений и скрининга генотипов. Сомаклональная изменчивость — прекрасный источник генетического разнообразия (сомаклональных вариаций), которое может быть реализовано в создании генетически измененных растений-регенерантов с новыми свойствами (со- маклональные варианты, или сомаклоны). Помимо повышения генетического разнообразия, использование сомаклональных вариантов в 2 раза может ускорить процесс выведения нового сорта даже для размножаемых семенами растений. Первые сомакло- нальные варианты табака были получены в Институте физиологии растений им. К.А.Тимирязева (Н.А.Загорина, З.П.Шамина, 1970).
Дата добавления: 2016-02-09; просмотров: 1530;
