Кристаллизация сплавов
Кристаллизация сплавов подчиняется тем же закономерностям, что и кристаллизация чистых металлов. Необходимым условием является стремление системы в состояние с минимумом свободной энергии. Равновесное состояние достигается при небольших скоростях охлаждения или достаточно длительном нагреве сплава. Реальные сплавы находятся, как правило, в неравновесном (метастабильном) состоянии. Основным отличием является большая роль диффузионных процессов между жидкостью и кристаллизующейся фазой. Эти процессы необходимы для перераспределения разнородных атомов равномерно распределенных в жидкой фазе. В сплавах в твердых состоянияхимеют место процессы перекристаллизации, обусловленные аллотропическими превращениями компонентов сплава, распадом твердых растворов, выделением из твердых растворов вторичных фаз. Когда растворимость компонентов в твердом состоянии меняется с изменением температуры. Эти превращения называются фазовыми превращениями в твердом состоянии. При перекристаллизации в твердом состоянии образуются центры кристаллизации и происходит их рост. Обычно центры кристаллизации возникают по границам зерен старой фазы, где решетка имеет наиболее дефектное строение, и где имеются примеси, которые могут стать центрами новых кристаллов. У старой и новой фазы в течение некоторого времени имеются общие плоскости. Такая связь решеток называется когерентной связью. В случае различия строения старой и новой фаз превращение протекает с образованием промежуточных фаз. Нарушение когерентности и обособление кристаллов наступает когда они приобретут определенные размеры. Процессы кристаллизации сплавов описываются диаграммами состояния.
Для сплавов фазовое состояние описывается диаграммой состояния.
Диаграмма состояния сплавов. Диаграмма состояния представляет собой графическое изображение фазового состояния сплавов данной системы в зависимости от температуры и концентрации компонентов (рис.1-42).
|
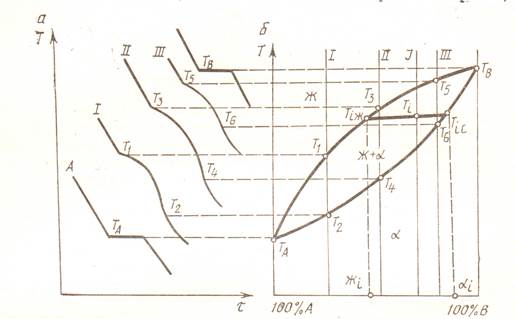
Рис. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого полностью растворимы в твердом состоянии
Диаграммы состояния показывают устойчивые состояния, т.е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы. Диаграммы состояния определяют экспериментально или рассчитывают теоретически по термодинамическим функциям. Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа.
|
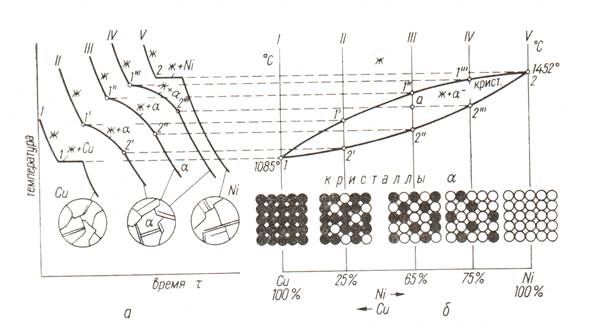
Рис. Построение диаграммы состояния медь – никель: а – кривые охлаждения сплавов I, II, III, IV, V; б – диаграмма состояния сплавов Cu – Ni и схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов.
Для экспериментального построения диаграммы состояний сплавов, образованных компонентами А и В, необходимо изготовить серию сплавов, содержащих различные количества компонентов А и В. Для каждого такого сплава экспериментально строят кривые охлаждения и определяют по ним критические точки, т.е. температуры фазовых превращений. Некоторые критические точки имеют названия, например, точки, отвечающие началу кристаллизации, называют точками ликвидус, а концу кристаллизации – точками солидус.
По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс – концентрация компонентов, по оси ординат – температура. Шкала концентраций показывает содержание компонента В. Левая крайняя точка на оси концентраций соответствует 100% содержанию компонента А. Процентное содержание второго компонента откладывается по этой оси слева направо. Правая крайняя точка соответствует 100 % содержанию второго компонента В. Основными линиями являются линии ликвидус (1) и солидус (2), а также линии, соответствующие фазовым превращениям в твердом состоянии (3,4) (рис.).
Рис.
По диаграмме состояния можно определить температуры фазовых превращений, изменение фазового состава. Свойства сплава, виды обработки, которые можно применять для сплава.
Дата добавления: 2016-02-02; просмотров: 1804;
