Классификация сплавов твердых растворов
По степеням растворимости компонентов различают:
- с неограниченной растворимостью компонентов;
- с ограниченной растворимостью компонентов.
При неограниченной растворимости компонентов кристаллическая решетка компонента растворителя по мере увеличения концентрации растворенного компонента плавно переходит в кристаллическую решетку растворенного компонента. Для образования растворов с неограниченной растворимостью компонентов необходимы:
1. Изоморфность (однотипность) кристаллических решеток компонентов;
2. Близость атомных радиусов компонентов, которые не должны отличаться более чем на 8-13%.
3. Близость физико-химических свойств подобных по строению валентных оболочек атомов.
Примерами таких сплавов являются сплавы Cu – Au, Cu – Ni, Ge – Si, Ag – Au, Mo – V.
При ограниченной растворимости компонентов возможна концентрация растворенного вещества до определенного предела. При дальнейшем увеличении концентрации однородный твердый раствор распадается с образованием двухфазной смеси.
По характеру распределения атомов растворенного вещества в кристаллической решетке растворителя различают твердые растворы:
- замещения: - внедрения; - вычитания.
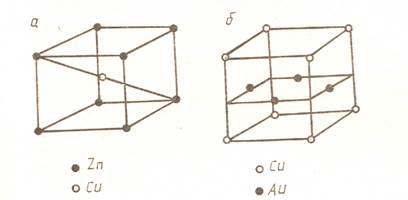
В растворах замещения в кристаллической решетке растворителя часть его атомов замещена атомами растворенного элемента (рис.а). замещение осуществляется в случайных местах, поэтому такие растворы называются неупорядоченными твердыми растворами. Однако в некоторых случаях при медленном охлаждении сплава или длительной выдержке при заданных температурах могут образоваться кристаллические решетки с упорядоченным расположением атомов компонентов (рис. П.с.89).
|
Кристаллическая решетка упорядоченных твердых растворов Zn+Cu (a) и Cu+Au (б)
Такие растворы называются упорядоченными или сверхструктурами. Сверхструктуры образуют компоненты сплава, находящиеся в соотношении АВ, АВ2, АВ3. они занимают промежуточное положение между твердыми растворами и химическими соединениями. При изменении температуры происходит их разупорядочивание с соответствующим изменением свойств. Температуру разупорядочивания Qк называют точкой Курнакова. При образовании растворов замещения периоды решеткиизменяются в зависимости от разности атомных диаметров растворенного элемента и растворителя. Если атом растворенного элемента больше атома растворителя, то элементарные ячейки увеличиваются. Если меньше – сокращаются. В первом приближении это изменение пропорционально концентрации растворенного компонента. Изменение параметров решетки при образовании твердых растворов – важный момент, определяющий изменение свойств. Уменьшение параметра ведет к большему упрочнению, чем его увеличение. Образование твердых растворов приводит к увеличению их электрического сопротивления, снижает пластичность и вязкость.
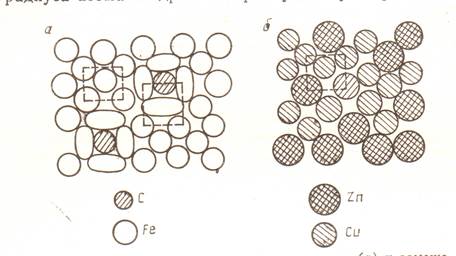
Твердые растворы внедрения образуются внедрением атомов растворенного компонента в междоузлия кристаллической решетки растворителя (рис. Б).
|
Рис. Схемы твердых растворов внедрения (а) и замещения (б)
Образование таких растворов возможно, если атомы растворенного элемента имеют малые размеры. Такими являются элементы, находящиеся в начале периодической системы – углерод, водород, азот, бор. Размеры атомов превышают размеры межатомных промежутков в кристаллической решетке металла, это вызывает искажение решетки и в ней возникают напряжения. Концентрация таких растворов не превышает 2-2.5 %. Типичным примером раствора такого типа является твердый раствор углерода в Fea и Feg. В Fea углерод имеет незначительную растворимость – до 0.02%, в Feg - до 2.14%.
Твердые растворы вычитанияили растворы с дефектной структурой образуются на базе химических соединений, при этом возможна не только замена одних атомов в узлах кристаллической решетки другими, но и образование пустых, не занятых атомами узлов в решетке. К химическому соединению добавляют один из входящих в формулу элементов, его атомы занимают нормальное положение в решетке соединения, а места атомов другого элемента остаются незанятыми.
Дата добавления: 2016-02-02; просмотров: 2433;
