Идеальные газы. Уравнение состояния идеального газа.
Техническая термодинамика.
Раздел науки, в которой рассматривается взаимное превращение тепловой и механической энергии.
Основу его составляет первый и второй законы термодинамики. Техническая термодинамика является основой тепловых двигателей. Основным понятием в термодинамике является понятие о термодинамической системе. ТДС представляет собой совокупность тел или частиц одного тела, находящихся во взаимодействии как между собой, так и с окружающей средой. Рабочими телами являются газы и пары и за счет них происходит преобразование тепловой энергии в механическую.
Непрерывно протекающие изменения состояния ТДС при взаимодействии ее с внешней средой называется термодинамическим процессом.
Основные термодинамические параметры состояния системы:
– абсолютное давление P=Pизб+Pб, где Pб – атмосферное давление.
– P=Pб+Pв, где Pв – давление вакуума. Па=Н/м2.
Нормальное атмосферное давление 105 Па =1 бар.
– объем Vудельный = V/m [м3/кг].
– абсолютная температура T[K].
Термодинамический процесс.
Основные параметры состояния P, V, T для однородного тела связаны зависимостью F(P,V,T)=0, которая в термодинамике называется уравнением состояния.

Процессы изменения состояния могут быть обратимыми и необратимыми.
Идеальные газы. Уравнение состояния идеального газа.
Под идеальным газом понимают совокупность физических молекул, не взаимодействующих между собой, т.е. пренебрегают силами притяжения и отталкивания между молекулами. Молекулы собственный объем не имеют.
Для m кг газа PV=mRT – уравнение Менделеева-Клапейрона,
для 1 кг газа PV=RT.
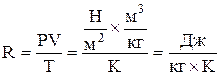 – газовая постоянная Ридберга,
– газовая постоянная Ридберга, 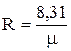 .
.
Дата добавления: 2016-02-02; просмотров: 1276;
