Тема лекции: Физико-химические методы анализа.
План лекции:
1. Общая характеристика физико-химических методов
2. Общие сведения о спектроскопических методах анализа.
3. Фотометрический метод анализа: фотоколориметрия, колориметрия, спектрофотометрия.
4. Общие сведения о нефелометрическом, люминесцентном, поляриметрическом методах анализа.
5. Рефрактометрический метод анализа.
6. Общие сведения о масс-спектральном, радиометрическом анализах.
7. Электрохимические методы анализа (потенциометрия, кондуктометрия, кулонометрия, амперометрия, полярография).
8. Хроматографический метод анализа.
Сущность физико-химических методов анализа. Их классификация.
Физико-химические методы анализа, как и химические методы, основаны на проведении той или иной химической реакции. В физических методах химические реакции отсутствуют или имеют второстепенное значение, хотя в спектральном анализе интенсивность линий всегда существенно зависит от химических реакций в угольном электроде или в газовом пламени. Поэтому иногда физические методы включают в группу физико-химических методов, так как достаточно строгого однозначного различия между физическими и физико-химическими методами нет, и выделение физических методов в отдельную группу не имеет принципиального значения.
Химические методы анализа были не в состоянии удовлетворить многообразные запросы практики, возросшие в результате научно-технического прогресса, развития полупроводниковой промышленности, электроники и ЭВМ, широкого применения чистых и сверхчистых веществ в технике.
Применение физико-химических методов анализа нашло свое отражение в технохимическом контроле пищевых производств, в научно-исследовательских и производственных лабораториях. Эти методы характеризуются высокой чувствительностью и быстрым выполнением анализа. Они основаны на использовании физико-химических свойств веществ.
При выполнении анализов физико-химическими методами точку эквивалентности (конец реакции) определяют не визуально, а при помощи приборов, которые фиксируют изменение физических свойств исследуемого вещества в точке эквивалентности. Для этой цели обычно применяют приборы с относительно сложными оптическими или электрическими схемами, поэтому эти методы получили название методов инструментального анализа.
Во многих случаях для выполнения анализа этими методами не требуется химическая реакция в отличие от химических методов анализа. Надо только измерить показатели каких-либо физических свойств анализируемого вещества: электропроводность, светопоглощение, светопреломление и др. Физико-химические методы позволяют вести в промышленности непрерывный контроль сырья, полуфабрикатов и готовых изделий.
Физико-химические методы анализа стали применять позднее, чем химические методы анализа, когда была установлена и изучена связь между физическими свойствами веществ и их составом.
Точность физико-химических методов сильно колеблется в зависимости от метода. Наиболее высокой точностью (до 0,001%) обладает кулонометрия, основанная на измерении количества электричества, которое затрачивается на электрохимическое окисление или восстановление определяемых ионов или элементов. Большинство физико-химических методов имеют погрешность в пределах 2-5 %, что превышает погрешность химических методов анализа. Однако такое сравнение погрешностей не вполне корректно, так как оно относится к разным концентрационным областям. При небольшом содержании определяемого компонента (около 10-3 % и менее) классические химические методы анализа вообще непригодны; при больших концентрациях физико-химические методы успешно соперничают с химическими. К числу существенных недостатков большинства физико-химических методов относится обязательное наличие эталонов и стандартных растворов.
Среди физико-химических методов наибольшее практическое применение имеют:
1. спектральные и другие оптические методы (рефрактометрия, поляриметрия);
2. электрохимические методы анализа;
3. хроматографические методы анализа.
Кроме этого выделяют еще 2 группы физико-химических методов:
1. радиометрические методы, основанные на измерении радиоактивного излучения данного элемента;
2. масс-спектрометрические методы анализа, основанные на определении масс отдельных ионизированных атомов, молекул и радикалов.
Наиболее обширной по числу методов и важной по практическому значению является группа спектральных и других оптических методов. Эти методы основаны на взаимодействии веществ с электромагнитным излучением. Известно много различных видов электромагнитных излучений: рентгеновское излучение, ультрафиолетовое, видимое, инфракрасное, микроволновое и радиочастотное. В зависимости от типа взаимодействия электромагнитного излучения с веществом оптические методы классифицируются следующим образом.
На измерении эффектов поляризации молекул вещества основаны рефрактометрия, поляриметрия.
Анализируемые вещества могут поглощать электромагнитное излучение и на основе использования этого явления выделяют группу абсорбционных оптических методов.
Поглощение света атомами анализируемых веществ используется в атомно-абсорбционном анализе. Способность поглощать свет молекулами и ионами в ультрафиолетовой, видимой и инфракрасной областях спектра позволила создать молекулярно-абсорбционный анализ (колориметрию, фотоколориметрию, спектрофотометрию).
Поглощение и рассеяние света взвешенными частицами в растворе (суспензии) привело к появлению методов турбидиметрии и нефелометрии.
Методы, основанные на измерении интенсивности излучения, возникающего в результате выделения энергии возбужденными молекулами и атомами анализируемого вещества, называются эмиссионными методами. К молекулярно-эмиссионным методам относят люминесценцию (флуоресценцию), к атомно-эмиссионным - эмиссионный спектральный анализ и пламенную фотометрию.
Электрохимические методы анализа основаны на измерении электрической проводимости (кондуктометрия); разности потенциалов (потенциометрия); количества электричества, прошедшего через раствор (кулонометрия); зависимости величины тока от приложенного потенциала (вольт-амперометрия).
В группу хроматографических методов анализа входят методы газовой и газожидкостной хроматографии, распределительной, тонкослойной, адсорбционной, ионообменной и других видов хроматографии.
Спектроскопические методы анализа: общие сведения
Понятие о спектроскопическом методе анализа, его разновидности
Спектроскопические методы анализа— физические методы, основанные на взаимодействии электромагнитного излучения с веществом. Взаимодействие приводит к различным энергетическим переходам, которые регистрируют инструментально в виде поглощения излучения, отражения и рассеяния электромагнитного излучения.
Классификация:
• Эмиссионный спектральный анализ основан на изучении спектров испускания (излучения) или эмиссионных спектров различных веществ. Разновидностью этого анализа является фотометрия пламени, основанная на измерении интенсивности излучения атомов, возбуждаемого нагреванием вещества в пламени.
• Абсорбционный спектральный анализ основан на изучении спектров поглощения анализируемых веществ. Если происходит поглощение излучения атомами, то абсорбция называется атомной, а если молекулами, то — молекулярной. Различают несколько видов абсорбционного спектрального анализа:
1. Спектрофотометрия — учитывает поглощение анализируемым веществом света с определенной длиной волны, т.е. поглощение монохроматического излучения.
2. Фотометрия – основана на измерении поглощения анализируемым веществом света не строго монохроматического излучения.
3. Колориметрия основана на измерении поглощения света окрашенными растворами в видимой части спектра.
4. Нефелометрия основана на измерении интенсивности света, рассеянного твердыми частицами, взвешенными в растворе, т.е. света, рассеянного суспензией.
• Люминесцентная спектроскопия использует свечение исследуемого объекта, возникающее под действием ультрафиолетовых лучей.
В зависимости от того, в какой части спектра происходит поглощение или излучение, различают спектроскопию в ультрафиолетовой, видимой и инфракрасной областях спектра.
Спектроскопия — чувствительный метод определения более 60 элементов. Его применяют для анализа многочисленных материалов, включая биологические среды, вещества растительного происхождения, цементы, стекла и природные воды.
Фотометрические методы анализа
Фотометрические методы анализа основаны на избирательном поглощении света анализируемым веществом или его соединением с подходящим реагентом. Интенсивность поглощения можно измерять любым способом, независимо от характера окрашенного соединения. Точность метода зависит от способа измерения. Различают колориметрический, фотоколориметрический и спектрофотометрический методы.
Фотоколориметрический метод анализа.
Фотоколориметрический метод анализа позволяет количественно определить интенсивность поглощения света анализируемым раствором с помощью фотоэлектроколориметров (иногда их называют просто фотоколориметрами). Для этого готовят серию стандартных растворов и вычерчивают зависимость светопоглощения определяемого вещества от его концентрации. Эта зависимость называется градуировочным графиком. В фотоколориметрах световые потоки, проходящие через раствор, имеют широкую область поглощения - 30-50 нм, поэтому свет здесь является полихроматическим. Это приводит к потере воспроизводимости, точности и избирательности анализа. Достоинства фотоколориметра заключается в простоте конструкции и высокой чувствительности благодаря большой светосиле источника излучения – лампы накаливания.
Колориметрический метод анализа.
Колориметрический метод анализа основан на измерении поглощения света веществом. При этом сравнивают интенсивность окраски, т.е. оптическую плотность, исследуемого раствора с окраской (оптической плотностью) стандартного раствора, концентрация которого известна. Метод весьма чувствителен и применяется для определения микро- и полумикроколичеств.
Для проведения анализа колориметрическим методом требуется значительно меньше времени, чем химическим путем.
При визуальном анализе добиваются равенства интенсивности окрашивания анализируемого и окрашиваемого раствора. Этого можно достигнуть 2 путями:
1. уравнивают окраску, изменяя толщину слоя;
2. подбирают стандартные растворы разных концентраций (метод стандартных серий).
Однако визуально невозможно установить количественно, во сколько раз один раствор окрашен интенсивнее другого. В этом случае можно установить только одинаковую окраску анализируемого раствора при сравнении его со стандартным.
Основной закон поглощения света.
Если световой поток, интенсивность которого I0, направить на раствор, находящийся в плоском стеклянном сосуде (кювете), то одна часть его интенсивностью Ir, отражается от поверхности кюветы, другая часть интенсивностью Iа поглощается раствором и третья часть интенсивностью It проходит через раствор. Между этими величинами имеется зависимость:
I0 = Ir + Iа + It (1)
Т.к. интенсивность Ir отраженной части светового потока при работе с одинаковыми кюветами постоянна и незначительна, то в расчетах ею можно пренебречь. Тогда равенство (1) принимает вид:
I0 = Iа + It (2)
Это равенство характеризует оптические свойства раствора, т.е. его способность поглощать ил пропускать свет.
Интенсивность поглощенного света зависит от числа окрашенных частиц в растворе, которые поглощают свет больше, чем растворитель.
Световой поток, проходя через раствор, теряет часть интенсивности – тем большую, чем больше концентрация и толщина слоя раствора. Для окрашенных растворов существует зависимость, называемая законом Бугера – Ламберта – Бера (между степенью поглощения света, интенсивностью падающего света, концентрацией окрашенного вещества и толщиной слоя).
По этому закону, поглощение монохроматографического света, прошедшего через слой окрашенной жидкости, пропорционально концентрации и толщине слоя его:
I = I0·10-kCh,
где I – интенсивность светового потока, прошедшего через раствор; I0 – интенсивность падающего света; С – концентрация, моль/л; h – толщина слоя, см; k – мольный коэффициент поглощения.
Мольный коэффициент поглощения k – оптическая плотность раствора, содержащего 1 моль/л поглощающего вещества, при толщине слоя 1 см. Он зависит от химической природы и физического состояния поглощающего свет вещества и от длины волны монохроматического света.
Метод стандартных серий.
Метод стандартных серий основан на получении одинаковой интенсивности окраски исследуемого и стандартного растворов при одинаковой толщине слоя. Окраску исследуемого раствора сравнивают с окраской ряда стандартных растворов. При одинаковой интенсивности окраски концентрации исследуемого и стандартного растворов равны.
Для приготовления серии стандартных растворов берут 11 пробирок одинаковой формы, размера и из одинакового стекла. Наливают из бюретки стандартный раствор в постепенно возрастающем количестве, например: в 1 пробирку 0,5 мл, во 2ую 1 мл, в 3ю 1,5 мл, и т.д. – до 5 мл (в каждую следующую пробирку на 0,5 мл больше, чем в предыдущую). Во все пробирки наливают равные объемы раствора, который дает с определяемым ионом цветную реакцию. Растворы разбавляют так, чтобы уровни жидкости во всех пробирках были одинаковы. Пробирки закрывают пробками, тщательно перемешивают содержимое и размещают в штативе по возрастающим концентрациям. Таким образом получают цветную шкалу.
К исследуемому раствору в одинаковой пробирке прибавляют столько же реактива, разбавляют водой до того же объема, как и в других пробирках. Закрывают пробкой, тщательно перемешивают содержимое. Окраску исследуемого раствора сравнивают с окраской стандартных растворов на белом фоне. Растворы должны быть хорошо освещены рассеянным светом. Если интенсивность окраски исследуемого раствора совпадает с интенсивностью окраски одного из растворов цветной шкалы, то концентрации этого и исследуемого растворов равны. Если же интенсивность окраски исследуемого раствора промежуточная между интенсивностью двух соседних растворов шкалы, то его концентрация равна средней концентрации этих растворов.
Применение метода стандартных растворов целесообразно только при массовом определении какого-нибудь вещества. Заготовленная серия стандартных растворов служит относительно короткое время.
Метод уравнивания интенсивности окраски растворов.
Метод уравнивания интенсивности окраски исследуемого и стандартного растворов производится путем изменения высоты слоя одного из растворов. Для этого в 2 одинаковых сосуда помещают окрашенные растворы: исследуемый и стандартный. Изменяют высоту слоя раствора в одном из сосудов до тех пор, пока интенсивность окраски в обоих растворах не станет одинаковой. В этом случае определяют концентрацию исследуемого раствора Сиссл., сравнивая ее с концентрацией стандартного раствора:
Сиссл. = Сст·hст / hиссл,
где hст и hиссл – высота слоя соответственно стандартного и исследуемого раствора.
Приборы, служащие для определения концентраций исследуемых растворов методом уравнивания интенсивности окраски, называются колориметрами.
Различают визуальные и фотоэлектрические колориметры. При визуальных колориметрических определениях интенсивность окраски измеряют непосредственным наблюдением. Фотоэлектрические методы основаны на использовании фотоэлементов-фотоколориметров. В зависимости от интенсивности падающего пучка света в фотоэлементе возникает электрический ток. Сила тока, вызванная воздействием света, измеряется гальванометром. Отклонение стрелки показывает интенсивность окраски.
Спектрофотометрия.
Фотометрический методоснован на измерении поглощения анализируемым веществом света не строго монохроматического излучения.
Если в фотометрическом методе анализа использовать монохроматическое излучение (излучение одной длины волны), то такой способ называют спектрофотометрией.Степень монохроматичности потока электромагнитного излучения определяют минимальным интервалом длин волн, который выделяется используемым монохроматором (светофильтром, дифракционной решеткой или призмой) из сплошного потока электромагнитного излучения.
К спектрофотометрииотносят также область измерительной техники, объединяющую спектрометрию, фотометрию и метрологию и занимающуюся разработкой системы методов и приборов для количественных измерений спектральных коэффициентов поглощения, отражения, излучения, спектральной яркости как характеристик сред, покрытий, поверхностей, излучателей.
Стадии спектрофотометрического исследования:
1) проведение химической реакции для получения систем, удобных для проведения спектрофотометрического анализа;
2) измерения поглощения полученных растворов.
Сущность метода спектрофотометрии
Зависимость поглощения раствора вещества от длины волны на графике изображается в виде спектра поглощения вещества, на котором легко выделить максимум поглощения находящийся при длине волны света, максимально поглощаемой веществом. Измерение оптической плотности растворов веществ на спектрофотометрах проводят при длине волны максимума поглощения. Это позволяет анализировать в одном растворе вещества, максимумы поглощения которых расположены при разных длинах волн.
В спектрофотометрии в ультрафиолетовой и видимой областях используют электронные спектры поглощения.
Они характеризуют наиболее высокие энергетические переходы, к которым способен ограниченный круг соединений и функциональных групп. В неорганических соединениях электронные спектры связаны с высокой поляризацией атомов, входящих в молекулу вещества, и обычно появляются у комплексных соединений. У органических соединений возникновение электронных спектров вызывается переходом электронов с основного на возбужденные уровни.
На положение и интенсивность полос поглощения сильно влияет ионизация. При ионизации по кислотному типу в молекуле появляется дополнительная неподеленная пара электронов, что приводит к дополнительному батох-ромному сдвигу (сдвигу в длинноволновую область спектра) и повышению интенсивности полосы поглощения.
В спектре многих веществ имеется несколько полос поглощения.
Для спектрофотометрических измерений в ультрафиолетовой и видимой областях применяется два типа приборов — нерегистрирующие(результат наблюдают на шкале прибора визуально) и регистрирующие спектрофотометры.
Люминесцентный метод анализа.
Люминесценция — способность к самостоятельному свечению, возникающему под различными воздействиями.
Классификация процессов, вызывающих люминесценцию:
1)фотолюминесценция (возбуждение видимым или ультрафиолетовым светом);
2)хемилюминесценция (возбуждение за счет энергии химических реакций);
3)катодолюминесценция (возбуждение электронным ударом);
4)термолюминесценция (возбуждение нагреванием);
5)триболюминесценция (возбуждение механическим воздействием).
В химическом анализе имеют значение первые два вида люминесценции.
Классификация люминесценции по наличию послесвечения.Оно может прекращаться сразу при исчезновении возбуждения — флюоресценцияили продолжаться определенное время после прекращения возбуждающего воздействия — фосфоресценция.В основном используют явление флюоресценции, поэтому метод назван флюориметрией.
Применение флюориметрии:анализ следов металлов, органических (ароматических) соединений, витаминов D, В6. Флюоресцентные индикаторы применяют при титровании в мутных или темно-окрашенных средах (титрование ведут в темноте, освещая титруемый раствор, куда добавлен индикатор, светом люминесцентной лампы).
Нефелометрический анализ.
Нефелометрияпредложена Ф. Кобером в 1912 г. и основана на измерении интенсивности света, рассеянного суспензией частиц, с помощью фотоэлементов.
С помощью нефелометрии измеряют концентрацию веществ, нерастворимых в воде, но образующих стойкие суспензии.
Для проведения нефелометрических измерений применяются нефелометры,аналогичные по принципу колориметрам, с той лишь разницей, что при нефелометрии
При проведении фотонефелометрическогоанализа сначала по результатам определения серии стандартных растворов строят калибровочный график, затем проводят анализ исследуемого раствора и по графику определяют концентрацию анализируемого вещества. Для стабилизации получаемых суспензий добавляют защитный коллоид — раствор крахмала, желатина и др.
Поляриметрический анализ.
Электромагнитные колебания естественного света происходят во всех плоскостях, перпендикулярных к направлению луча. Кристаллическая решетка обладает способностью пропускать лучи только определенного направления. По выходе из кристалла колебания луча совершаются только в одной плоскости. Луч, колебания которого находятся в одной плоскости, называется поляризованным. Плоскость, в которой происходят колебания, называется плоскостью колебания поляризованного луча, а плоскость, перпендикулярная к ней, - плоскость поляризации.
Поляриметрический метод анализа основан на изучении поляризованного света.
Рефрактометрический метод анализа.
В основе рефрактометрического метода анализа лежит определение показателя преломления исследуемого вещества, т.к. индивидуальное вещество характеризуется определенным показателем преломления.
Технические продукты всегда содержат примеси, которые влияют на величину показателя преломления. Поэтому показатель преломления может в ряде случаев служить характеристикой чистоты продукта. Например, сорта очищенного скипидара различают по показателям преломления. Так, показатели преломления скипидара при 20° для желтого цвета, обозначенные через n20D (запись означает , что показатель преломления измерен при 20°С, длина волны падающего света равна 598 ммк), равны:
Первый сорт Второй сорт Третий сорт
1,469 – 1,472 1,472 – 1,476 1,476 – 1,480
Рефрактометрический метод анализа можно применять для двойных систем, например для определения концентрации вещества на водном или органическом растворах. В этом случае анализ основан на зависимости показателя преломления раствора от концентрации растворенного вещества.
Для некоторых растворов имеются таблицы зависимости показателей преломления от их концентрации. В других случаях анализируют методом калибровочной кривой: готовят серию растворов известных концентраций, измеряют их показатели преломления и строят график зависимости показателей преломления от концентрации, т.е. строят калибровочную кривую. По ней определяют концентрацию исследуемого раствора.
Показатель преломления.
При переходе луча света из одной среды в другую его направление меняется. Он преломляется. Показатель преломления равен отношению синуса угла падения к синусу угла преломления (эта величина постоянная и характерная для данной среды):
n = sin α / sin β,
где α и β – углы между направлением лучей и перпендикуляром к поверхности раздела обеих сред (рис. 1)


 α
α
А





Б β
Показатель преломления – отношение скоростей света в воздухе и в исследуемой среде (если луч света падает из воздуха).
Показатель преломления зависит от:
1. длины волны падающего света (с увеличением длины волны показатель
преломления уменьшается);
2. температуры (с увеличением температуры показатель преломления уменьшается);
3. давления (для газов).
При обозначении показателя преломления указывают длины волны падающего света и температуру измерения. Например, запись n20D означает , что показатель преломления измерен при 20°С, длина волны падающего света равна 598 ммк. В технических справочниках показатели преломления приведены при n20D.
Определение показателя преломления жидкости.
Перед началом работы поверхность призм рефрактометра промывают дистиллированной водой и спиртом, проверяют правильность установления нулевой точки прибора и приступают к определению показателя преломления исследуемой жидкости. Для этого поверхность измерительной призмы осторожно протирают ваткой, смоченной исследуемой жидкостью, и наносят на эту поверхность несколько ее капель. Призмы закрывают и, вращая их, наводят границу светотени на крест нитей окуляра. Компенсатором устраняют спектр. При отсчете показателя преломления три десятичных знака берут по шкале рефрактометра, а четвертый – на глаз. Затем сдвигают границу светотени, снова совмещают ее с центром визирного креста и делают повторный отсчет. Т.о. производят 3 или 5 отсчетов, после чего промывают и вытирают рабочие поверхности призм. Исследуемое вещество снова наносят на поверхность измерительной призмы и проводят вторую серию измерений. Из полученных данных берут среднее арифметическое значение.
Радиометрический анализ.
Радиометрический анализ основан на измерении излучений радиоактивных элементов и применяется для количественного определения радиоактивных изотопов в исследуемом материале. При этом измеряют либо естественную радиоактивность определяемого элемента, либо искусственную радиоактивность, получаемую с помощью радиоактивных изотопов.
Радиоактивные изотопы идентифицируют по периоду их полураспада или по виду и энергии испускаемого излучения. В практике количественного анализа чаще всего измеряют активность радиоактивных изотопов по их α-, β- и γ-излучению.
Применение радиометрического анализа:
• Изучение механизма химических реакций.
• Методом меченых атомов исследуют эффективность различных приемов внесения удобрений в почву, пути проникновения в организм микроэлементов, нанесенных на листья растения, и т.п. Особенно широко используют в агрохимических исследованиях радиоактивные фосфор 32Р и азот 13N.
• Анализ радиоактивных изотопов, используемых для лечения онкологических заболеваний и для определения гормонов, ферментов.
Масс-спектральный анализ.
Основан на определении масс отдельных ионизированных атомов, молекул и радикалов в результате комбинированного действия электрического и магнитных полей. Регистрацию разделенных частиц проводят электрическим (масс-спектрометрия) или фотографическим (масс-спектрография) способами. Определение проводят на приборах – масс-спектрометрах или масс-спектрографах.
Электрохимические методы анализа.
Электрохимические методы анализа и исследования основаны на изучении и использовании процессов, протекающих на поверхности электрода или в приэлектродном пространстве. Аналитический сигнал— электрический параметр (потенциал, сила тока, сопротивление), который зависит от концентрации определяемого вещества.
Различают прямыеи косвенныеэлектрохимические методы.В прямых методах используют зависимость силы тока от концентрации определяемого компонента. В косвенных — силу тока (потенциал) измеряют для нахождения конечной точки титрования (точки эквивалентности) определяемого компонента титрантом.
К электрохимическим методам анализа относят:
1. потенциометрию;
2. кондуктометрию;
3. кулонометрию;
4. амперометрию;
5. полярографию.
Электроды, используемые в электрохимических методах.
1.Электрод сравнения и индикаторный электрод.
Электрод сравнения— это электрод с постоянным потенциалом, нечувствительный к ионам раствора. Электрод сравнения имеет устойчивый во времени воспроизводимый потенциал, не меняющийся при прохождении небольшого тока, и относительно его ведут отчет потенциала индикаторного электрода. Используют хлорсеребряный и каломельный электроды. Хлорсеребряный электрод — серебряная проволока, покрытая слоем AgCI и помещенная в раствор KCI. Потенциал электрода определяется концентрацией иона хлора в растворе:
Каломельный электрод состоит из металлической ртути, каломели и раствора KCI. Потенциал электрода зависит от концентрации хлорид-ионов и температуры.
Индикаторный электрод — это реагирующий на концентрацию определяемых ионов электрод. Индикаторный электрод изменяет свой потенциал с изменением концентрации «потенциалопределяющих ионов». Индикаторные электроды делят на необратимые и обратимые.Скачки потенциала обратимых индикаторных электродов на межфазных границах зависят от активности участников электродных реакций в соответствии с термодинамическими уравнениями; равновесие устанавливается достаточно быстро. Необратимые индикаторные электроды не удовлетворяют требованиям обратимых. В аналитической химии применяются обратимые электроды, для которых выполняется уравнение Нернста.
2. Металлические электроды: электронообменные и ионообменные.
Уэлектронообменногоэлектрода на межфазной границе протекает реакция с участием электронов. Электронообменные электроды делят на электроды первого родаи электроды второго рода.Электроды первого рода — металлическая пластина (серебро, ртуть, кадмий), погруженная в раствор хорошо растворимой соли этого металла. Электроды второго рода — металл, покрытый слоем малорастворимого соединения этого металла и погруженный в раствор хорошо растворимого соединения с тем же анионом (хлорсеребряный, каломельный электроды).
Ионообменные электроды— электроды, потенциал которых зависит от отношения концентраций окисленной и восстановленной форм одного или нескольких веществ в растворе. Такие электроды делаются из инертных металлов, например из платины или золота.
3. Мембранные электродыпредставляют собой пористую пластинку, пропитанную жидкостью, не смешивающейся с водой и способной к избирательной адсорбции определенных ионов (например, растворы хелатов Ni2+, Cd2+, Fe2+ в органическом растворе). Работа мембранных электродов основана на возникновении разности потенциалов на границе раздела фаз и установлении равновесия обмена между мембраной и раствором.
Потенциометрический метод анализа.
Потенциометрический метод анализа основан на измерении потенциала электрода, погруженного в раствор. При потенциометрических измерениях составляют гальванический элемент с индикаторным электродом и электродом сравнения и измеряют электродвижущую силу (ЭДС).
Разновидности потенциометрии:
Прямая потенциометрияприменяется для непосредственного определения концентрации по значению потенциала индикаторного электрода при условии обратимости электродного процесса.
Косвенная потенциометрияоснована на том, что изменение концентрации иона сопровождается изменением потенциала на электроде, погруженном в титруемый раствор.
В потенциометрическом титровании обнаруживают конечную точку по скачку потенциала, обусловленную заменой электрохимической реакции на другую в соответствии со значениями Е° (стандартный электродный потенциал).
Значение потенциала зависит от концентрации соответствующих ионов в растворе. Например, потенциал серебряного электрода, погруженного в раствор соли серебра, изменяется с изменением концентрации Ag+-ионов в растворе. Поэтому, измерив потенциал электрода, погруженного в раствор данной соли неизвестной концентрации, можно определить содержание соответствующих ионов в растворе.
Электрод, по потенциалу которого судят о концентрации определяемых ионов в растворе, называют индикаторным электродом.
Потенциал индикаторного электрода определяют, сравнивая его с потенциалом другого электрода, который принято называть электродом сравнения. В качестве электрода сравнения может быть применен только такой электрод, потенциал которого остается неизменной при изменении концентрации определяемых ионов. В качестве электрода сравнения применяют стандартный (нормальный) водородный электрод.
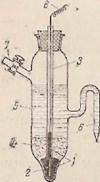
На практике часто в качестве электрода сравнения с известным значением электродного потенциала пользуются не водородным, а каломельным электродом (рис. 1). Потенциал каломельного электрода с насыщенным раствором КО при 20 °С равен 0,2490 В.
Кондуктометрический метод анализа.
Кондуктометрический метод анализа основан на измерении электропроводности растворов, изменяющейся в результате химических реакций.
Электропроводность раствора зависит от природы электролита, его температуры и концентрации растворенного вещества. Электропроводность разбавленных растворов обусловлена движением катионов и анионов, отличающихся различной подвижностью.
С повышением температуры электропроводность увеличивается, так как увеличивается подвижность ионов. При данной температуре электропроводность раствора электролита зависит от его концентрации: как правило, чем выше концентрация, тем больше электропроводность! Следовательно, электропроводность данного раствора служит показателем концентрации растворенного вещества и обусловливается подвижностью ионов.
В простейшем случае кондуктометрического количественного определения, когда в растворе содержится только один электролит, строят график зависимости электропроводности раствора анализируемого вещества от его концентрации. Определив электропроводность исследуемого раствора, по графику находят концентрацию анализируемого вещества.
Так, электропроводность баритовой воды изменяется прямо пропорционально содержанию в растворе Ва(ОН)2. Эта зависимость графически выражается прямой линией. Чтобы определить содержание Ва(ОН)2 в баритовой воде неизвестной концентрации, надо определить ее электропроводность и по калибровочному графику найти концентрацию Ва(ОН)2, соответствующую этому значению электропроводности. Если через раствор Ва(ОН)2, электропроводность которого известна, пропустить измеренный объем газа, содержащего диоксид углерода, то С02 реагирует с Ва(ОН)2:
Ва(ОН)2 + С02 → ВаС03 + Н20
|
В результате этой реакции содержание Ва(ОН)2 в растворе уменьшится и электропроводность баритовой воды понизится. Измерив электропроводность баритовой воды после поглощения ею С02, можно определить, насколько понизилась концентрация Ва(ОН)2 в растворе. По разности концентраций Ва(ОН)2 в баритовой воде легко рассчитать количество поглощенной С02, а следовательно, и содержание ее в исследуемом газе. Таким образом, определяют, например, содержание С02 в азото-водородной смеси, поступающей в колонны синтеза аммиака.
Наибольший интерес представляет измерение электропроводности в объемном анализе для определения точки эквивалентности при титровании.
Рис. 1. Каломельный электрод:
1 — ртуть; 2—платиновая проволока для контакта; 3 —стеклянная трубка; 4 — паста каломели с кристаллами KCI; 5—насыщенный раствор KCI; 6 — сифон; 7—боковая трубка; 8 — медная проволока для включения электрода в цепь.
Полярографический метод анализа.
В полярографическом методе анализа используют явление концентрационной поляризации, возникающее на электроде с малой поверхностью при пропускании электрического тока через растворы электролитов. Электролиз при этом ведут при помощи двух опущенных в раствор анализируемого вещества электродов: одного малого (поляризующийся) и другого большого (неполяризующийся).
Кривая силы тока во время электролиза поднимается резко вверх, образуя так называемую полярографическую волну. По потенциалу, при котором возрастает сила тока, можно судить о качественном составе электролита; по высоте полярографической волны — о концентрации определяемого иона.
Для проведения полярографического анализа достаточен небольшой объем анализируемого раствора (иногда 0,1—0,02 мл), Полярографирование продолжается 2—5 мин. Чувствительность определения составляет 10-3— 10_4 0/о, а метод так называемой амальгамной полярографии дает возможность определять примеси в особо чистых металлах от 10-5 до 10-6%.
Сущность метода. Если приложить разность потенциалов к электродам, опущенным в раствор электролита, и постепенно увеличивать эту разность потенциалов, то вначале ток через раствор протекать почти не будет. При увеличении разности потенциалов до значения, достаточного для разложения электролита, сила тока возрастает. Эту величину разности потенциалов называют потенциалом разложения.
Если взять один из электродов с малой поверхностью (обычно применяют капельный ртутный катод), другой — с большой поверхностью (обычно применяют ртуть), то при пропускании через раствор постоянного электрического тока основное изменение концентрации будет наблюдаться у электрода с малой поверхностью. Такое явление обусловлено большой силой тока, приходящейся в процессе электролиза на единицу поверхности малого электрода, т. е. высокой плотностью тока на электроде.
По мере повышения разности потенциалов между электродами увеличивается сила тока, протекающего через раствор, и плотность тока на малом электроде. При этом скорость обеднения раствора в непосредственной близости к поверхности малого электрода также возрастает и наступает концентрационная поляризация. Соответственно этому возрастает сопротивление прохождению тока на границе малый электрод — раствор.
В конечном итоге наступает такой момент, когда дальнейшее повышение разности потенциалов не вызывает заметного возрастания силы тока, протекающего через раствор.
При установившемся подвижном равновесии, когда количество восстановленных ионов становится равным количеству ионов, продиффундировавших к ртутному катоду, сила тока становится постоянной. Такую силу тока, при которой достигается полный разряд всех ионов анализируемого вещества, поступающих в приэлектродное пространство за счет диффузии, называют предельным или диффузионным током.
Кулонометрический анализ.
Кулонометрический анализ— группа методов, основанных на измерении количества электричества, необходимого для электрохимического превращения определяемого вещества.
Кулонометрический анализ основан на явлении электролиза. Измеряют количество электричества, затраченного на электрохимическое восстановление (окисление) определяемого иона. В основе определения лежит закон Фарадея. Метод широко применяется в аналитической химии с 40-х гг. XX в.
Основное условие кулонометрии:все затраченное на определение количество электричества должно расходоваться только на основную электрохимическую реакцию.
Амперометрия.
Амперометрия основана на измерении тока при фиксированном потенциале индикаторного электрода в перемешиваемых растворах. Ток возникает в результате электрохимического окисления или восстановления электроактивного вещества при наложении импульса на индикаторный электрод. В качестве индикаторного электрода в амперометрии используется ртутный, платиновый или графитовый микроэлектрод. Электродом сравнения может быть каломельный электрод (см. рис.1) или другой поляризуемый электрод. Варианты амперометрического титрования:
А) титрование с одним поляризуемым электродом;
Б) титрование с двумя поляризуемыми электродами.
Амперометрию можно применять для определения конечной точки титрования.
Хроматографический метод анализа.
Хроматографический метод анализа основан на избирательной способности поглощения различных компонентов некоторыми твердыми веществами. Этот метод применяется для разделения сложных смесей и близких по свойствам ионов (например, редкоземельных металлов).
Некоторые пористые вещества способны поглощать на своей поверхности жидкости или газы. Это явление называется адсорбцией, а поглотитель – адсорбентом.
Количество поглощенного вещества зависит от:
1. структуры адсорбента;
2. природы адсорбента;
3. природы поглощаемого вещества;
4. концентрации поглощаемого вещества;
5. температуры.
Хроматографическое разделение смесей основано на различии адсорбционных свойств компонентов, т.е. на способности по-разному адсорбироваться при прохождении через адсорбент.
Принцип хроматографического анализа состоит в следующем. Пропускают через стеклянную трубку с адсорбентом раствор, содержащий смесь различных веществ. Трубка, наполненная адсорбентом, называется адсорбционной, или поглотительной, колонкой. Сначала в верхнем слое адсорбента поглощаются все адсорбирующиеся вещества. При дальнейшем прохождении через этот слой новых порций раствора более сильно адсорбирующиеся вещества вытесняют с поверхности адсорбента вещества, которые адсорбируются слабее.
Т.о. компоненты располагаются по колонке отдельными зонами – происходит разделение компонентов. Если после анализируемого раствора пропустить через колонку растворитель (воду, бензол и т.д.), то разделение можно сделать еще более эффективным. В результате по высоте колонки образуются участки (зоны), занятые отдельными компонентами (рис. 2)



Рис.2. Зоны хроматографической колонки.
При полном разделении число зон соответствует количеству компонентов в смеси. Вследствие различной окраски ионов или их соединений эти зоны обычно различаются по цвету. Поэтому распределение зон называют хроматограммой (от греч. «хромос» - цвет), а поглотительную колонку - хроматографической колонкой.
Различают следующие виды хроматографического анализа:
1. адсорбционный;
2. осадочный;
3. ионно-обменный;
4. бумажный.
Осадочная хроматография.
Метод основан на различной степени растворимости малорастворимых соединений. Общий принцип осадочной хроматографии заключается в следующем. Осадитель, способный реагировать с несколькими ионами, при нанесении на высокодисперсное (мелкораздробленное) вещество – адсорбент - образует осадочную хроматограмму в соответствии с различной растворимостью осадков. Расположение зон в осадочной хроматограмме определяется произведениями растворимости труднорастворимых соединений.
Пусть осадочно-хроматографическая колонка, содержащая адсорбент, смешанный с нитратом серебра, обработана раствором, содержащем ионы Сl-, Br-, I-. Образуются труднорастворимые осадки AgCl, AgBr, AgI. Если концентрация ионов Сl-, Br-, I- примерно одинаковы, то вначале в осадок выпадает соединение, произведение растворимости которого меньше, т.е. AgI, затем AgBr, и,наконец, AgCl. Т.е. в данном случае порядок распределения зон сверху вниз таков: AgI, AgBr, AgCl. На полученную хроматограмму действуют солнечным светом. Через 5 – 10 минут четко выявляются три зоны: первая – желтого цвета – AgI, вторая – голубовато-серого – AgBr, третья – фиолетово-серого – AgCl.
Колонка, применяемая в осадочной хроматографии, состоит из адсорбента и оcадителя. К анализу колонку готовят, растирая адсорбент с осадителем или пропитывая адсорбент раствором оcадителя.
В качестве адсорбента в осадочной хроматографии используются твердые, хорошо очищенные дисперсные материалы, индифферентные к оcадителю, хроматографическим веществам и образующимся осадкам. Применяют силикагель, чистый оксид алюминия, гидроксид алюминия, сульфат бария. Могут применяться гипс, стекло, песок. Т.к. при осадочной хроматографии большей частью проводят визуальные наблюдения, т.е. осадки различаются по внешнему виду, адсорбент должен быть бесцветным или может иметь лишь слабую окраску, не искажающую общую картину хроматографии.
Ионно-обменная хроматография.
В случае электролитов происходит так называемая обменная адсорбция: ион из раствора поглощается адсорбентом, а взамен его в раствор переходит ион адсорбента; этот ион входит в состав адсорбента или содержится в нем в качестве примеси. Обменная адсорбция – перераспределение ионов между адсорбентом и раствором. Так, многие силикаты поглощают катионы из раствора и отдают ионы в раствор. Это объясняется тем, что силикат – электролит, и его катион более или менее подвижен, анион же неподвижен и составляет как бы скелет адсорбента.
 Адсорбенты, способные к обмену своих ионов на ионы электролита из раствора называют ионообменниками, или ионитами.
Адсорбенты, способные к обмену своих ионов на ионы электролита из раствора называют ионообменниками, или ионитами.
катиониты (обмен своих катионов катионы электролита) аниониты (обмен своих анионов)
В качестве катионитов применяют алюмосиликаты: природные (цеолиты) или искусственные (пермутиты) и синтетические смолы (органолиты).
Практически хроматография применяется в качественном анализе. Например, хроматографическое отделение Fe3+ от Аl3+ и Zn2+, предложенное Ю.Ю.Лурье и Н.А. Филипповой.
Соответственно с положением этих элементов в периодической системе ионы цинка и алюминия имеют более кислотный характер, чем ионы Fe3+; в щелочной среде Аl3+ и Zn2+ образуют анионы, а Fe3+ - гидроксид. Поэтому при пропускании через катионит раствора, содержащего перечисленные три катиона в кислой среде, они адсорбируются. При последующем же промывании катионита 5%-ным раствором натрий-гидроксида цинк и алюминий переходят в раствор в виде анионов, а железо остается в колонке.
Техника хроматографических работ.
Подготовка адсорбента и хроматографической колонки. Адсорбент размельчают в фарфоровой ступке на зерна такой величины, чтобы они проходили сквозь сито с отверстиями 0,25 мм. Приготовленный адсорбент в количестве 2 г помещают в бюретку емкостью 5 – 10 мл. Перед заполнением колонки адсорбентом нижнее отверстие закрывают небольшим тампоном из стеклянной ваты, затем заполняют бюретку адсорбентом. В трубку помещают всю порцию адсорбента. Адсорбент утрамбовывают сначала постукиванием трубки о поверхность стола до прекращения усадки, а затем дополнительно уплотняют (но не очень энергично) стеклянной палочкой. После уплотнения адсорбент должен занимать половину высоту колонки.
Для получения четких зон требуется равномерное заполнение колонки адсорбентом. Не допускаются видимые глазом неоднородности адсорбента. В правильно приготовленной колонке границы окрашенных зон горизонтальны.
Дата добавления: 2016-01-26; просмотров: 1269;
