Строение, общие свойства
Номенклатура
При составлении названия алкадиена по номенклатуре ИЮПАК главную цепь необходимо выбирать так, чтобы в нее входили обе двойные связи. Нумеровать атомы в цепи нужно таким образом, чтобы атомы углерода, связанные двойными связями, получили минимальные номера:
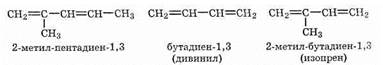
Некоторые простые алкадиены имеют тривиальные названия (на рисунке выше они приведены в скобках), однако их употребление (в отличие от названий простейших алканов) не рекомендуется в номенклатуре ИЮПАК. Тем не менее они используются, и их нужно знать.
Возможны три разных способа взаиморасположения двойных связей в диеновом углеводороде относительно друг друга:
1) Двойные связи расположены вплотную одна к другой:
СН2=С=СН-СН2-СН3
Такие углеводороды называются кумуленовыми. Рассмотрение химических свойств кумуленовых углеводородов выходит за рамки данного курса.
2) Двойные связи разделены более чем одной одинарной связью:
СН2=СН-СН2-СН=СН2
Такие алкадиены носят название изолированных. Их химические свойства ничем не отличаются от свойств обычных алкенов (разумеется, с учетом того, что в реакцию могут вступать две никак не зависящие друг от друга двойные связи).
3) Если двойные связи разделены в цепи только одной s-связью, то их называют сопряженными. В этом случае в молекуле двойные и одинарные связи чередуются, как, например, в бутадиене-1,3 СН2=СН—СН=СН2, который является простейшим сопряженным алкадиеном.
Соединения с чередующимся расположением двойных связей отличаются по свойствам как от алкенов, так и от других типов алкадиенов. Особенности химического поведения этих соединений объясняются наличием сопряжения.
Сопряжение — образование единого электронного облака в результате взаимодействия негибридизованных р-орбиталей в молекуле с чередующимися двойными и одинарными связями.
Большой интерес представляют диены с сопряженными двойными связями, так как они имеют некоторые свойства, обусловливающие их широкое применение в химической промышленности. Особые свойства таких диеновых углеводородов объясняются их электронным строением. Рассмотрим строение бутадиена. Экспериментально установлено расположение всех атомов углерода в одной плоскости, определены межатомные расстояния. Оказалось, что длина связи между углеродными атомами (в нм) такова:
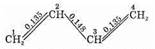
. Крайние связи (C1—С2 и С3—С4) имеют несколько большую длину, чем двойная связь в этилене (0,132 нм), центральная связь
С2—С3 короче простой связи О—С (0,154 нм). Чтобы объяснить это, обратимся к электронному строению бутадиена.
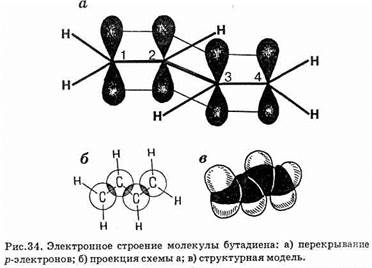
Укаждого атома углерода имеются три гибридные sp2-орбитали, которые при перекрывании образуют s-связи. Негибридиованные р-электронные орбитали (их четыре), образующие p-связи, перекрываются не только между первым и вторым, третьим и четвертым атомами углерода, но также между вторым и третьим. Хотя 2,3-перекрывание меньше 1,2- и 3,4-перекрывания (рис. 34), все же оно вызывает уменьшение длины центральной связи С2—С3.
При перекрывании р-орбиталей в бутадиене получаются не
отдельные, обособленные p-связи, а единое, общее p-электронное
облако. В этом случае говорят о сопряжении двойных связей,
приводящем к некоторому выравниванию связей. Сопряжение
связей часто изображают пунктиром:
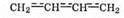
Основная особенность сопряженной системы заключается в том, что она реагирует как единое целое. Это можно проследить на примере присоединения хлороводорода к бутадиену. Данная реакция, подобно всем злектрофильным реакциям присоединения по двойной связи, начинается с присоединения протона к концевому атому углерода (по правилу Марковникова — см. §2.4).
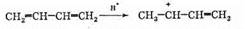
Положительный заряд в образовавшемся катионе не закреплен (локализован) на втором атоме углерода, так как к нему может смещаться p-электронная пара соседней двойной связи. В результате недостаток электронов (положительный заряд) переносится частично и на концевой атом углерода. Таким образом, катион имеет мезомерный эффект:
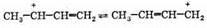
Мезомерный катион можно записать в виде одной структуры с распределенным зарядом (строго говоря, полной симметрии в; распределении заряда здесь нет):
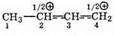
Если в мезомерном катионе анион хлора присоединится ко второму атому, то получится продукт 1,2-присоединения; если
Присоединение идет к четвертому атому углерода, то образуется продукт 1,4-присоединения.
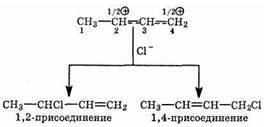
Обычно получается смесь продуктов присоединения. Процентный выход того или иного продукта зависит от условий, прежде всего от температурного режима, растворителя. При действии второй молекулы хлороводорода присоединение к оставшейся двойной связи идет по обычным законам, образуется дихлорпроизводное. Подобно реакции с хлороводородом, проходят реакции с бромом, хлором и др.
Реакция полимеризации тоже может протекать таким образом, что присоединение элементарных звеньев будет проходить в ^Вожениях 1,2 или 1,4. При полимеризации бутадиена по способу Лебедева (в присутствии металлического натрия) получаются макромолекулы нерегулярного разветвленного строения:
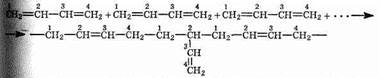
Такие макромолекулы не дают высококачественного материала: из-за их разветвленности нет плотной упаковки молекул в полимере и каучук получается с невысокими физико-механическими показателями. Поэтому в настоящее время в присутствии специальных катализаторов получают каучуки, в макромолекулax которых элементарные звенья соединены только в положениях 1,1; в этом случае цепь не имеет разветвлений.
Дата добавления: 2016-01-03; просмотров: 1076;
