Мезомерный эффект (эффект сопряжения, резонансный эффект).
Мезомерный эффект (М) представляет собой еще один механизм передачи взаимного влияния атомов, не связанных друг с другом. Под действием мезомерного эффекта происходит перераспределение электронной плотности в молекуле. Однако в отличие от индуктивного эффекта это перераспределение осуществляется не через систему σ – связей, а главным образом с участием π – и p – электронов (неподеленной электронной пары, НЭП). Более того, если при индуктивном влиянии σ – электроны лишь частично смещаются относительно исходных положений в пределах своих октетов, то в случае мезомерного эффекта происходит частичное перемещение электронных пар в соседние октеты, вызывающее аналогичное отталкивание взаимодействующих электронных пар следующих октетов далее вдоль цепи π – связей вплоть до крайнего атома, на котором локализуется передаваемый частичный избыток электронной плотности.
Мезомерный эффект можно определить как перераспределение электронной плотности путем перекрывания π – электронных облаков с соседними π -, p – или σ – С–Н – электронными облаками и образование в результате этого общего π – электронного облака в составе, которого происходят электронные смещения.
Условием такого перекрывания является параллельность осей соответствующих р – орбиталей, а так же их пространственная близость. Мезомерный эффект наблюдается в так называемых сопряженных системах, содержащих π – связи, неподеленные р – электронные пары или σ – С-Н – связи, отделенные от π – электронов или друг от друга.
Подобные системы обычно планарны. Планарными называют плоские молекулы, в которых оси р – орбиталей соседних атомов углерода перпендикулярны плоскости σ – связи, то есть, параллельны между собой (но обязательно располагаются на одной прямой).
Электронные облака π – связей и р – электронов характеризуются большой поляризуемостью, чем электронные облака σ – связей. Смещение электронов π – связей и р – электронов, находящихся в сопряжении с π – связями, может приводить в пределе к полному переходу электронных пар из октета одного атома в октет другого без распада молекулы, так как такой переход не затрагивает σ – связей. При этом на атомах могут возникать полные заряды. В соответствии с этим эффект сопряжения можно изобразить:
1) изогнутыми стрелками, которые показывают направление смещения
π – или р – электронов; возникающее в результате этого распределение электронной плотности называют мезомерым.
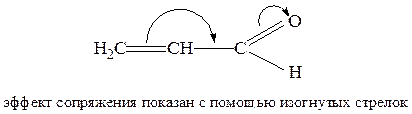
2) предельными (резонансными) структурами, которые соединяются обоюдоострыми стрелками (знак резонанса);
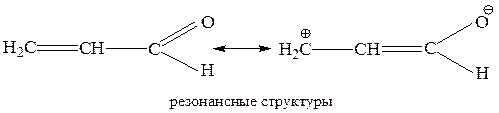
3) в форме резонансного гибрида, в котором пунктиром обозначают π – или р – электроны, делокализованные между атомами.
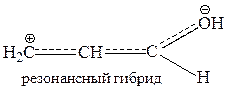
Группы, содержащие полярные π – связи, обладают – М-эффектом (ЭА). По системе сопряженных связей эффект сопряжения передается без изменения, происходит смещение всего делокализованного π – электронного облака:
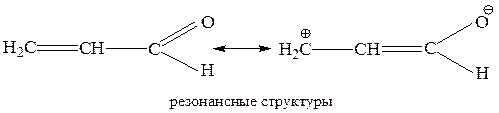
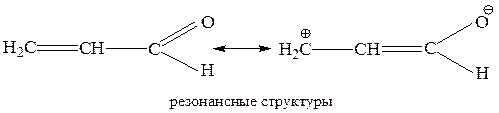
Атомы, содержащие свободные n – электроны, сопряженные с π – связью, обладают + М-эффектом.
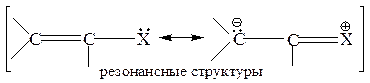
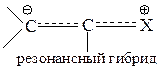
где Х – галоген, OH, NH2
В таких соединениях индуктивный эффект и эффект сопряжения действуют в противоположных направлениях. Сила этих эффектов зависит от электроотрицательности атомов и способности р – электронов к делокализации. Например:
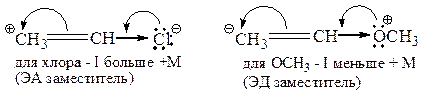
Характер распределения электронной плотности в молекулах и особенно в ионах (карбокатионах и карбанионах) обуславливает реакционную способность соединений и направление реакций.
Виды мезомерного эффекта:
1) π, π – Сопряжение (М) – две двойные связи разделены одинарной; М отсутствует, если двойные связи разделены более чем одной простой связью (бутадиен – 1,3).
2) р, π – Сопряжение (+М) – р – орбиталь с НЭП отделена от π – орбитали одной связью (винилхлорид).
3) σ, π – Сопряжение (гиперконъюгация) (+М) – каждая из углерод - водородных связей метильной группы отделена от π –МО – орбитали одной простой связью (пропен).
6. Классификация химических реакций в органической химии. Гетеро и гомолитический разрыв ковалентной связи. Нуклеофильные и электрофильные механизмы реакций.
Основные понятия. Химическая реакция.
Процесс превращения веществ, сопровождающийся изменением их состава и (или) строения, называется химической реакцией.
Суть этого процесса заключается в разрыве химических связей в исходных веществах и образовании новых связей в продуктах реакции. Реакция считается законченной, если вещественный состав реакционной смеси больше не изменяется.
В уравнениях реакций с участием органических соединений (органических реакциях) знак равенства заменяется стрелкой (т.к. символ равенства "=" совпадает с символом двойной связи):
CH4 + Cl2 ® CH3Cl + HCl;
CH2=CH2 + Br2 ® CH2Br-CH2Br.
Энергия активации.
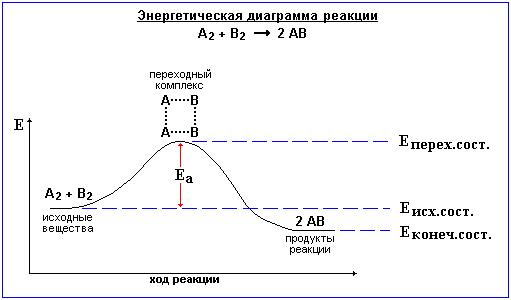
Энергия активации (Еа) - энергия, необходимая для достижения системой переходного состояния, называемого активированным (или переходным) комплексом, который превращается в продукты реакции уже самопроизвольно.
Дата добавления: 2015-11-06; просмотров: 4069;
