Атомно-орбитальные модели.
Для наглядного изображения пространственного и электронного строения молекул, ионов, свободных радикалов удобно использовать атомно-орбитальные модели, отражающие на основе электронных представлений взаимное расположение атомных орбиталей разного типа:
1) участвующих в образовании ковалентных связей;
2) с неспаренным электроном;
3) с неподеленной электронной парой;
4) вакантных (например, в карбокатионах).
В виде электронного облака изображают обычно р-АО и не участвующие в образовании s-связей гибридные АО; остальные АО обозначаются валентной чертой или клиньями в зависимости от их ориентации в пространстве.
Простая линия (валентная черта) изображает оси орбиталей, лежащие в плоскости рисунка; сплошной клин соответствует АО, расположенной над плоскостью рисунка; штрихованный клин изображает АО, направленную за эту плоскость.
Для построения АО-моделей сначала следует определить тип гибридизации каждого атома и затем последовательно, в порядке химического связывания атомов, изобразить их атомные орбитали с учетом образуемых углов.
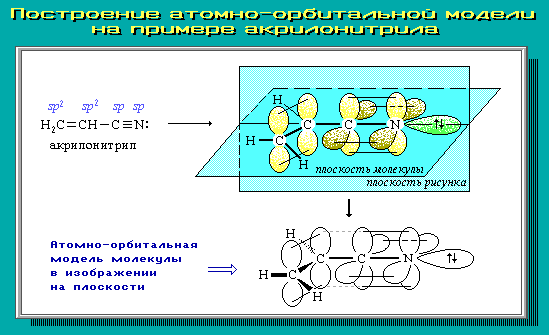
Примеры АО-моделей некоторых молекул:
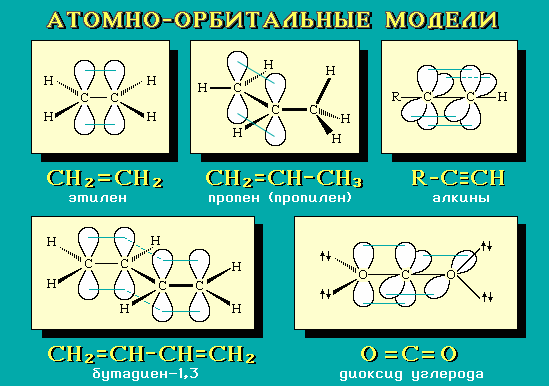
Умение представить молекулу в виде атомно-орбитальной модели помогает понять не только особенности ее электронного и пространственного строения, но и механизмы передачи взаимного влияния атомов (электронные и пространственные эффекты), которые определяют поведение органических соединений в химических реакциях. Кроме того, с помощью АО-моделей можно объяснить существование делокализованных p-связей.
Дата добавления: 2015-11-06; просмотров: 1962;
