Донорно-акцепторные связи.
Ковалентная связь, образующаяся за счет пары электронов одного из атомов, т.е. по донорно-акцепторному механизму, называется дoнорно-акцeпторной.
Например, такая связь образуется между атомом азота в молекуле метиламина CH3NH2 и протоном H+ кислоты HCl:
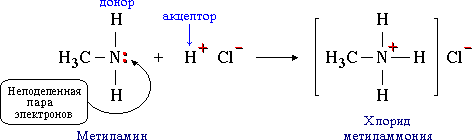
Атом азота отдает свою электронную пару на образование связи и выступает в роли донора, а протон предоставляет вакантную орбиталь, играя роль акцептора. Атом-донор при этом приобретает положительный заряд.
Донорно-акцeпторная связь отличается только способом образования; по свойствам она одинакова с остальными ковалентными связями.
Другой пример - протонирование спирта:
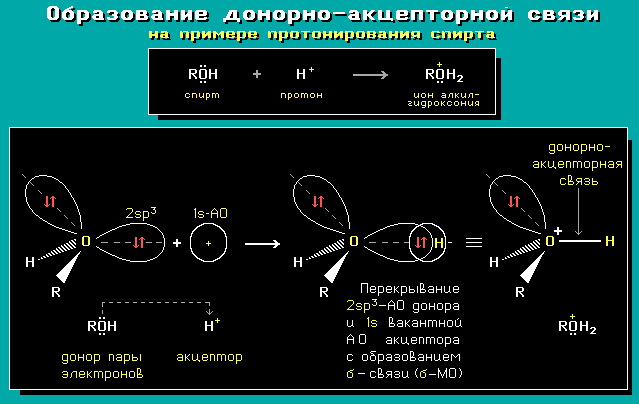
Разновидностью донорно-акцепторной связи является семиполярная связь.
Кратные связи.
Встречающиеся в органических соединениях кратные связи (двойные или тройные):
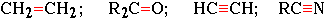
образуются при обобществлении двумя атомами более чем одной пары электронов:
Н2С : : СН2; R2С : : О; HС : : : CH; RС : : : N.
Кратные связи являются сочетанием s- и p-связей.
Двойная связь состоит из одной s- и одной p-связей и осуществляется 4-мя общими электронами.
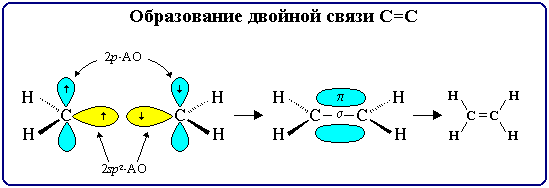
Тройная связь является комбинацией из одной s- и двух p-связей и включает в себя шесть электронов.
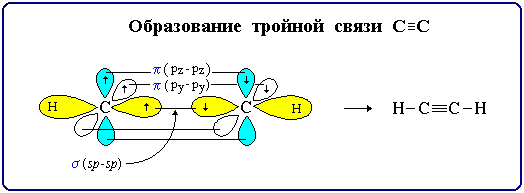
Число электронных пар, участвующих в образовании ковалентной связи называется порядком связи.
Таким образом, порядок простой связи равен 1, двойной – 2, тройной – 3. В случае сопряженных (делокализованных) связей порядок связи отличается от этих целочисленных значений.
Дата добавления: 2015-11-06; просмотров: 1468;
