Кавитационная эрозия 1 страница
Кавітаційна ерозія спостерігається при експлуатації гідротурбін, гребних гвинтів, насосів, клапанів, запірних пристроїв в трубопроводах. Вона обумовлена нестаціонарністю потоку рідини, оточуючої тверде тіло. Кавітація - це процес утворення і зникнення бульбашок в рідині. Зникнення бульбашок сопро- воджується гідравлічним ударом, який і є причиною кавітаційної ерозії.
Виникнення бульбашок відбувається в області низького тиску, а зникнення - в області високого тиску. Таким чином, область кавітаційного руйнування часто буває значно віддалена від зони виникнення бульбашок.
Спочатку відбувається прогресуюче розпушення матеріалу, що приводить до утворення численних мікротріщин. Потім починається викришування дрібних частинок.
Інформація для повторення
| № п/п | Вид локальної корозії (ЛК) | Метали і сплави, що піддаються (ЛК) | Середовище і місце проявлення (ЛК) | Умови проявлення (ЛК) |
| 1. | Пітингова (Площа поверхні ураження << глибини проникнення) | Fe, Ni, Co, Mn, Cr, Al, Mg, Cu, Zn | Морська вода, системи оборотного водопостачання, хім. підприємства | - метал у пассив-ному стані; -дефекти в захис-ній плівці; -наявність акти-ваторів в розчині електроліту |
| 2. | Виразкова (Площа поверхні ураження > глибини проникнення) | Вуглецеві та низьколеговані сталі | Хлоровмісні середовища, водоводи, теплоенергетичне обладнання | - метали в пасивному або активному стані |
| 3. | Щілинна | Практично всі мет. і сплави (крім спец. легован. марок) | Кор. середовища з високою конц. електроліту. Обладнання хім. пром., металургійне обладнання і т.п. | - близьке розташування двох поверхонь і застій розчину елек-троліту між ними |
| 4. | Міжкристалітна (На кордоні зерен полікристалічних матеріалів) | Сплави Fe, Al, Cu Неіржавіючі сталі | Сільнокисле середовище. Обладнання хім. пром., металур-ійне обладнання і т.п. | - порушення зв'язку між окре-мими зернами металу; - виборчі розчи-нення складових сплаву |
| 5. | Селективне витравлювання | Нержавіючі, вуглецеві сталі | Сільнокисле середовище. Обладнання хім. пром., металургійне обладнання і т.п. | - матеріал складається з двох або більше фаз, які відрізняються за властивостями; - різна швидкість розчинення фаз |
| 6. | Контактна | Нержавіючі, вуглецеві сталі, що містять Al | Підземне, теплопередавальне обладнання. | - механічні напруги; - мет. з різними електрохім. властивостями. |
| № п/п | Вид корозійно- механічного руйнування | Види впливу на матеріал | Умови і особливості протікання процесу |
| 1. | Корозійне розтріскування (20-40% всіх руйнувань) | Розтягуюча напруга і корозійне середовище. | - відсутність пластичних деформацій в мет.; - виникнення тріщин, що приводить до крихкості металу; - міжкристалітні тріщи-ни з розгалуженням. |
| 2. | Корозійна втома | Періодичне динамічне навантаження (нижче межі міцності) і кор. середовище. | утворення між-і транс-кристалітних тріщин |
| 3. | Фретинг корозія | Тертя дотичних частин конструкції | дотичні поверхні ніколи не роз'єднуються |
| 4. | Кавітаційна ерозія | Утворення і зникнення бульбашок повітря при нестаціонарному потоці рідини (гідравлічний удар) | - виникнення безлічі тріщин; - розпушення поверхні металу. |
4. КОРОЗІЯ МЕТАЛІВ В ПРИРОДНИХ І ТЕХНОЛОГІЧНИХ СЕРЕДОВИЩАХ
Машини, апарати, металоконструкції залежно від свого призначення працюють в природних або промислових середовищах.
Характер технологічного середовища надає значний вплив на закономірності корозійних процесів і вимагає ухвалення різних рішень для здійснення основного інженерного завдання - захисту металів від корозії.
Технологічні середовища хімічних виробництв відрізняються великим різноманіттям, різним поєднанням корозійно-активних компонентів, і у кожному конкретному випадку вимагають свого рішення. Тому необхідно враховувати вплив конструктивних чинників на розвиток корозійних руйнувань машин і апаратів і деякі види газової корозії, які приводять до специфічних деструктивних змін металів і сплавів.
4.1. Корозія металів в природних середовищах
Більшість металоконструкцій експлуатуються в природних середовищах. Значна кількість сталевих споруд експлуатується в атмосферних умовах. Магістральні і промислові трубопроводи, водоводи, обсадні колони свердловин нафтових і газових родовищ працюють під землею. Загальна маса сталі, що знаходиться під землею, перевищує 200 млн тонн, а поверхня сталевих споруд, що піддається грунтовій корозії, складає більше півтора мільярдів квадратних метрів.
Металеві конструкції портів, причалів, судів знаходяться в постійному контакті з водою і схильні до морської корозії.
Всі види корозійних процесів в природних умовах протікають за електрохімічним механізмом. Проте кожне природне середовище володіє своїми особливостями.
4.1.1. Атмосферна корозія металів
Атмосферна корозія- це корозія споруд і устаткування, що експлуа-туються в нормальній земній атмосфері.
Швидкість корозії і вид корозійного руйнування залежать від природи металу, вологості, забрудненості атмосфери (ГОСТ 16350-80). В середньому швидкість корозії металів в атмосфері нижча, ніж в грунті і морській воді.
Основним стимулюючим чинником атмосферної корозії є вода.
При відносній вологості повітря до 60 % сліди вологи на поверхні металу відсутні. В цьому випадку корозія протікає за хімічним механізмом. Оксидні плівки, що утворюються на поверхні, володіють захисними властивостями і гальмують розвиток корозійних руйнувань (мал. 6.1).
При відносній вологості повітря, рівній 60-70%, починається конденсація вологи і на поверхні металу з'являється адсорбційна плівка води.
Відносна вологість, при якій починається конденсація вологи на поверхні металу, називається критичною вологістю. Вона залежить від стану металу і від ступеня забруднення повітря.
При відносній вологості, близькій до 100%, або при безпосередньому зволоженні металу (дощ, туман), на поверхні відбувається утворення видимих фазових шарів води.
Вказані три типи станів значно відрізняються за механізмом протікання процесу корозії.
В області сухої корозії, як указувалося вище, реалізується хімічний механізм процесу і швидкість руйнування металів невелика.
Зростання оксидної плівки відбувається в перші секунди і хвилини. Після двох-трьох годин подальше потовщення плівки припиняється. Гранична товщина плівок на залізі - 30-40 А, на неіржавіючих сталях - 10-20 А.
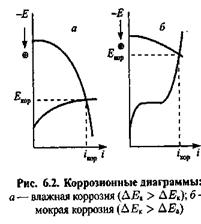
При утворенні адсорбційного шару вологи (товщиною порядка декількох молекулярних шарів) на поверхні металу з,явля
|
ється електроліт. У цих умовах реалізується електрохімічний механізм і швидкість корозії значно зростає. Плівка вологи має невелику товщину, кисень проникає через неї безперешкодно і катодний процес не утруднений. Анодний процес ускладнюється тим, що продукти корозії екранують поверхню металу. Оскільки плівка вологи дуже тонка, то істотні омічні втрати, але, в цілому, процес контролюється анодним гальмуванням (мал. 6.2, а).
При утворенні фазових плівок в області мокрої корозії утруднена доставка кисню і спостерігається катодне гальмування процесу (мал. 6.2, би}.
Залізо і сталь в звичайних умовах піддаються загальній рівномірній корозії.
Характер протікання атмосферної корозії істотно залежить від конструктивних особливостей виробу. Наявність вузьких щілин і зазорів, в яких можливі капілярна конденсація і застій вологи, посилюють атмосферну корозію і можуть привести до утворення корозійних виразок .
Забруднення атмосфери газами, пилом різко прискорює корозію. Це явище спостерігають в промислових центрах, особливо в присутності в повітрі SО2, NНз, Н2S, С12, НС1.
Виявлений різко стимулюючий корозію вплив низьких концентрацій
SО2. Так, присутність в атмосфері SО2 в концентраціях 15-35мкг/м3 збільшує швидкість корозії в десятки і сотні разів. В цей же час високі концентрації SО2 збільшують швидкість корозійних руйнувань тільки в 5-7 разів.
У роботах Ю.Н. Михайлівського запропонована физико-механическая модель атмосферної корозії, яка дозволяє пов'язати інтенсивність корозійних руйнувань з параметрами навколишнього середовища. Це служить основою для прогнозування корозійної поведінки металів і розробки способів їх захисту.
Стійкість металів до атмосферної корозії залежить від їх хімічної природи і стану поверхні.
4.1.2. Грунтова корозія металів
Різні трубопроводи, силові кабелі і кабелі зв'язку, опори, ємкості і інші металеві конструкції експлуатуються в підземних умовах.
У США, наприклад, витрати на поточний ремонт і заміну труб, що вийшли з ладу, складають декілька сотен мільйонів доларів в рік.
Грунт є складним природним середовищем, особливості якого треба враховувати при розгляді процесів корозії, що протікають в ній.
Вода в грунті присутня у вигляді зв'язаної, капілярної і гравітаційної.
Зв'язана вода, що входить до складу гідратованих хімічних сполук, не впливає на корозію.
Висота підйому капілярної вологи залежить від ефективного радіусу пір грунту. Рівень грунтових вод і пористість грунту визначають вологість, яка впливає на швидкість корозії.
Гравітаційна волога переміщається по грунту під дією сили тяжіння і також впливає на режим вологості грунту. Різні грунти по разному утримують вологу. Важкі, глинисті грунти утримують вологу тривалий час, піщані грунти - проникніші.
Із збільшенням вологості грунту її корозійна активність підвищується до тих пір, поки не досягне деякого критичного рівня. Надалі із збільшенням вологості її активність падає. Це пов'язують із зменшенням доступу кисню, необхідного для здійснення катодної реакції.
Для кожного виду грунту існує своє значення критичної вологості, при якій корозійні втрати досягають максимуму. Для глиністих грунтів це значення лежить між 12 і 25%, для піщаних - між 10 і 20 %.
При малій зволоженості грунту великі омічні втрати, що утрудняє протікання електрохімічних процесів. Значення рН для більшості грунтів знаходиться у межах рН = 6,0-7,5. Проте, зустрічаються також лужні суглинки і солончаки, що мають значення рН = 7,5-9,5, і кислі, гумусові і болотяні грунти з рН = 3,0-6,0. Такі грунти відрізняються високою агресивністю.
Мінералізація грунту може мінятися в широких межах - від 10 мг/л до 300 мг/л, що теж позначається на швидкості корозії.
Мінералогічний і гранулометричний склад грунтів, так само як і вологість, впливає на омічний опір. Так, в сухому піщано-глиністому грунті питомий опір грунту складає 240000 Ом-см, а у вологому піщано-глиністому грунті - 900 Ом-см. Цей показник також впливає на агресивність грунту. Нижче приведені дані, що характеризують взаємозв'язок між електроопором і агресивністю грунту (табл. 6.2).
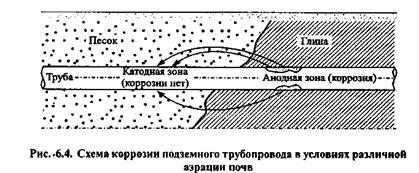
Велике значення має повітропроникність грунтів. Утруднення доступу кисню знижує швидкість корозії. З цієї причини піщані грунти часто агресивніші, ніж глиністі. Якщо трубопровід пролягає послідовно в глинистих і піщаних грунтах, тобто в умовах нерівномірної аерації, то виникають мікрогальванічні корозійні зони: на глинистій ділянці - анодна, а на піщаному - катодна (мал. 6.4).
|
Руйнування металу протікає а тих ділянках, до яких утруднений доступ кисню. Анодні і катодні ділянки можуть бути значно віддалені один від одного. Відстань між ними може складати декілька сотень метрів. У більшості грунтів процес корозії протікає з катодним гальмуванням із-за трудності транспорту кисню (мал. 6.5, а). У рихлих грунтах, що добре аеруються, спостерігається анодне гальмування (мал. 6.5, б). При виникненні корозійних пар, в яких анодні і катодні ділянки значно віддалені один від одного, процес характеризується омічним гальмуванням (мал. 6.5, в).
Крім рівномірної корозії підземні металеві споруди схильні до пітингу і корозійного розтріскування (КР). Пітинг виникає найчастіше на нижній частині трубопроводів, де є постійний контакт з грунтом. КР виявляють в катодно поляризованих трубопроводах в місцях порушення захисних покриттів.
Блукаючі струмиє причиною серйозних корозійних руйнувань підземних комунікацій і споруд в промисловій зоні. Блукаючі постійні струми з'являються внаслідок витоку в грунт постійного струму, споживаного наземним і підземним рейковим транспортом (метро, трамвай, електрифікована залізниця), агрегатами електрозварювань.
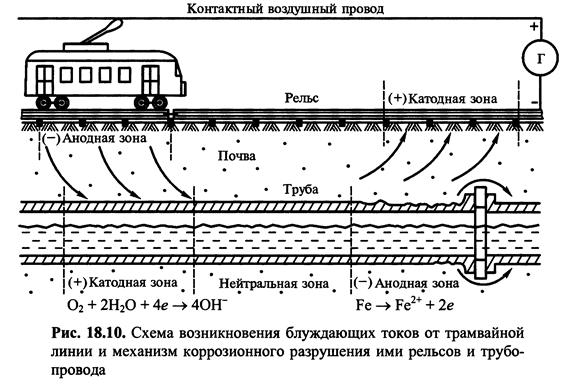
Ділянки, де блукаючі струми входять із землі в металеву конструкцію, стають катодами, а там, де струм стікає з металу в почву-анодами. Інтенсивність корозійних пошкоджень знаходиться в прямій залежності від величини блукаючих струмів і підкоряється закону Фарадея. Протікання струму величиною в 1 А протягом року відповідає розчиненню близько 9 кг заліза. У деяких несприятливих випадках були зареєстровані блукаючі струми величиною до 200-500 А. Звідси видно наскільки інтенсивними можуть бути пошкодження від блукаючих струмів. Якщо анодна область рівномірно розподілена по великій поверхні, корозійні втрати можуть і не викликати аварійних руйнувань, але в місцях порушення неметалічного захисного покриття корозійні руйнування відбуваються швидко.
Для захисту трубопроводів від дії блукаючих струмів використовують дренаж - з'єднання металевою шиною джерела блукаючих струмів, наприклад, рейок, з їх приймачем, наприклад, трубопроводом. Якщо дренаж встановити неможливо, то у напрямі рейки закопують спеціальний анод з чавуну, який сполучають з анодною областю трубопроводу мідним провідником. Тоді блукаючий струм викликає корозію тільки цього спеціального анода. Якщо додаткового анода недостатньо, то в ланцюг між анодом і трубою включають джерело постійного струму протилежного напряму. Для зменшення руйнуючої дії блукаючих струмів використовують також ізолюючі прокладки в місцях стику трубопроводу.
Підземна корозія може інтенсифікуватися мікроорганізмами. У грунті мешкають два види мікроорганізмів: аеробні, життєдіяльність яких протікає тільки за наявності кисню, і анаеробні бактерії, що розвиваються за відсутності кисню. Корозія металів, викликана або посилена дією мікроорганізмів, носить назву біологічною або біохімічною.
Аеробні бактерії можуть бути двох видів: одні окиснюють сірку, інші - осаджують залізо. Перший вид бактерій краще всього розвивається в кислому середовищі (рН = 3-6). Вони окиснюють сірку до сірчаної кислоти. При цьому на окремих ділянках концентрація сірчаної кислоти може доходити до 10%. Таке підкислення середовища викликає різке збільшення швидкості корозії.
Аеробні бактерії, що переробляють залізо, розвиваються в інтервалі рн = 4-^10. Суть їх діяльності полягає в тому, що вони поглинають залізо в іонному стані, а виділяють його у вигляді нерозчинних сполук. Нерівномірне відкладення цих сполук приводить до збільшення гетерогенності поверхні, що підсилює корозію.
Анаеробні бактерії в основному відновлюють сірку з сульфатів, що знаходяться в грунті. Цей тип бактерій розвивається при рН= 5,5-8,0. В результаті їх життєдіяльності іони SO відновлюються до 82~ з виділенням С>2. Останній починає брати активну участь в катодному процесі. Присутність в корозійному середовищі сульфідів і сірководня приводить до появи на поверхні виробу рихлого шару сульфіду заліза. Корозія має пітинговий характер.
4.1.3. Морська корозія металів
Портові споруди, причали, судна, використання морських нафтопроводів схильні до дії морської корозії.
Морська вода є розчином різноманітних солей, головним чином хлоридів, сульфатів і карбонатів натрію, магнію, калія, кальцію і так далі Вона є електролітом, її електропровідність достатньо висока і складає (2,5-3,0)-10~2Ом~1-см~1, має нейтральну або слаболужну реакцію (рН = 7,2-8,6). Присутність в морській воді іонів хлора, тобто іонів-активаторів, робить це середовище високо корозійно-активним.
Солоність морської води визначають в промілях (%о). Промилею називається кількість твердих речовин в грамах, розчинена в 1000 г морської води, за умови, що всі галогени замінені еквівалентною кількістю хлора, всі карбонати переведені в оксиди, органічні речовини спалені. В цьому випадку 1%о = 0,1мас.%. Середня солоність води в океані 3-3,5 %о. Але вона значно коливається в різних водних басейнах.
У морській воді міститься велика кількість мікроорганізмів, сприяючих приско-ренню корозії і обростанню дотичних з водою металоконструкцій.
Корозія в морській воді протікає по електрохімічному механізму виключно з катодним контролем. Присутність іонів-активаторів (С1~) перешкоджає утворенню пасивних плівок на поверхні металів. Висока електропровідність виключає прояв омічного гальмування.
Залежність швидкості корозії заліза від концентрації КС1 в аерованому водному розчині проходить через максимум при змісті КС1- 3 %. Зменшення швидкості корозії пояснюється зниженням розчинності кисню у воді із зростанням концентрації NaC1.
Збільшення швидкості потоку веде до посилення корозії внаслідок поліпшення аерації поверхні металу. Крім того, високі швидкості потоку сприяють ерозійному руйнуванню металу.
Підвищений вміст кисню в поверхневих шарах води викликає посилену корозію в області ватерлінії судів, на ділянках гідроспоруд, що знаходяться близько до поверхні або періодично омиваних водою (мал. 6.6).
На занурених у воду конструкціях закріплюються або розвиваються багато рослинних і тваринних організмів.
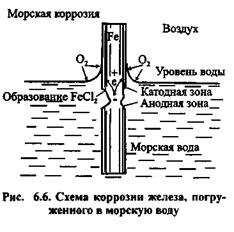
|
Це явище називаєтся обростанням. Мікроорганізми прискорюють руйнування протикорозійних покриттів. З'являються локальні вогнища оголеної металевої поверхні, які провокують інтенсивне руйнування металу. Основним видом захисту від морської корозії є протикорозійні і протиобростаючі лакофарбні і металізації покриття і електрохімічний захист.
Серед лакофарбних покриттів найбільш ефективні товстошарі покриття на епоксидній основі з обмеженим змістом розчинника або без розчинника.
У захисні композиції додають речовини, що володіють протиобрастаючою дією. Вони носять назву біоцидів. Найчастіше застосовують оксиди міді (I) і (II). Вони, вимиваючись з покриття, утворюють в морській воді важкорозчинні комплекси. Крім того у сполук міді відсутній кумулятивний ефект для морських організмів.
Для захисту судневих конструкцій найчастіше використовують алюміній з легуючими добавками, наприклад, цинком або лантаном. Алюмінієві покриття у поєднанні з лакофарбними покриттями володіють високою стійкістю в морській воді, мають підвищену стійкість до ерозії.
Для боротьби з морською корозією широко використовують електрохімічний захист (ГОСТ 26301-85 і ГОСТ 26251-84). Захист підводної частини великотонажних судів здійснюють автоматичними системами катодного захисту.
4.2. Вплив конструктивних чинників на розвиток корозійних
руйнувань машин і апаратів
При проектуванні хімічного виробництва, як правило, приділяють основну увагу аналізу характеру агресивного середовища і умовам протікання процесу. Керуючись цими даними, вибирають матеріал, що володіє достатнім хімічним опором.
Такої ж пильної уваги заслуговує раціональне конструювання окремих вузлів і апаратів.Невдале конструювання у багатьох випадках може бути причиною утворення застійних зон, зазорів, концентрації напруги і інших явищ, сприяючих виникненню і протіканню корозії.
Разом з тим вже на стадії проектування можна передбачити такі конструктивні вирішення окремих вузлів апарату, які значно понизять або усунуть можливість виникнення процесу корозії.
При конструюванні обладнання слід звертати увагу на характер обробки поверхні металу, контакт сполучених елементів з різних матеріалів, режим розподілу потоків теплоносія, наявність щілин і зазорів, можливість утворення застійних зон.
Гладка поверхня металу має менше різних дефектів у вигляді подряпин, нерівностей і так далі На шорсткій поверхні легше скупчується грязь, пил і інші речовини. Це особливо характерно для виробництва добрив, солей. Металеве обладнання і конструкції з шорсткою поверхнею в цьому випадку покриваються різними речовинами. Якщо ці речовини гігроскопічні і легко вбирають вологу, то вони прилипають до поверхні металу, створюються місцеві осередки з високою концентрацією електроліту, що сприяє посиленій корозії.
Якщо в конструйованому апараті є деталі, виконані з різних металевих матеріалів,то виникає небезпека прояву контактної корозії (див. 5.1.6.). В цьому випадку ще на стадії проектування обов'язково повинні бути прийняті заходи по запобіганню або ослабленню цього явища. Зазвичай застосовують один з двох можливих прийомів.
1) Контактуючі деталі з різнорідних металів виготовляють з різною площею поверхні. При цьому деталь з найменшою поверхнею повинна бути виконана з благороднішого металу (втулки вентилів, поршневі кільця насосів і так далі).
2) Якщо такий спосіб виявляється неможливим, то деталі з різних матеріалів повинні бути ізольовані один від одного. Цей спосіб запобігання електрохімічній контактній корозії часто застосовують при проектуванні трубопроводів, в будівельних конструкціях. Особливу увагу при цьому треба приділити властивостям матеріалу прокладки. Він повинен бути інертним по відношенню до робочого середовища, здатним витримувати температурні і механічні навантаження, мати високу зносостійкість. Особливу увагу слід приділити монтажу контактних вузлів. Якщо монтаж виконаний неакуратно, то можливе виникнення застійних зон, щілин і інших осередків посиленого розвитку корозії.
Багато хімічних і нафтохімічних процесів протікають при підвищених температурах. Корозійні процеси в цих умовах мають свої особливості. Чим вище температура, тим інтенсивніше відбувається руйнування металу. Швидкість корозії в умовах теплопереноса може змінюватися до двох порядків.
Поверхня металу, дотична з теплоносіямиі хладагентами, піддається додатковій корозійній дії. Наприклад, теплообмінники є одним з найменш стійких видів обладнання У 92% випадків причиною відмови в роботі теплообмінника є корозія теплопередаючих поверхонь.
У ізотермічних умовах при рівності температур металуі технологічного середовища в певному інтервалі температур спостерігається ефект різкого збільшення швидкості корозії металів, що пасивуються, і зниження потенціалу вільної корозії. Метал з пасивного стану переходить в активне.
Ця температура за визначенням Я.М. Колотиркина названа граничною температурою самопасивацїі. Очевидно, що в реальних умовах треба прагнути працювати при таких температурах, при яких метал ще зберігає здібність до самостійного переходу в пасивний стан.
При конструюванні апаратів слід передбачити рівномірний розподіл теплового потоку, виключити можливість локального перегріву. У багатьох промислових апаратах, в яких протікають високотемпературні процеси, такі заходи передбачені.
Для теплообмінного обладнання найбільш поширеними є локальні види корозії, такі як пітингова, щілинна і міжкристалітна.
При проектуванні конструкцій повинні бути позначені місця і способи зварки. При зварці металів в зоні шва і в колошовній зоні створюється велика розтягуюча напруга. У зонах, розташованих уздовж шва, де метал нагрівається вище за критичні температури, міняється структура металу. Це може привести до розтріскування металу.
При конструюванні зварних вузлів і деталей слід передбачати ряд засобів: уникати скупчення швів, виключити точкову зварку, при якій особливо велика концентрація напруги, застосовувати місцевий відпал і так далі
Дуже небезпечними в корозійному відношенні зонами в апаратурі є зазори і щілини. У них може відбуватися концентрація робочого розчину, порушуватися аерація, що неминуче приведе до розвитку місцевої корозії. З цієї точки зору небезпечні переривисті зварні шви, в яких унаслідок нещільного прилягання матеріалу один до одного утворюються щілини і зазори, що є причиною виникнення щілинної корозії.
Розділ III МЕТОДИ ЗАХИСТУ ВІД КОРОЗІЇ
1. КЛАСИФІКАЦІЯ МЕТОДІВ ЗАХИСТУ
В техніці захист від корозії здійснюється різними методами. Найбільш раціональний і надійний шлях - це виготовлення апаратів, машин і так далі з корозійностійких як металевих, так і неметалічних матеріалів. Проте цей шлях захисту від корозії не завжди може бути використаний через економічні, технічні або технологічні умови. В промисловості часто готують вироби, апарати, труби з дешевих і доступних матеріалів, що володіють високими технологічними і механічними властивостями, з подальшим їх захистом від корозії.
Методи захисту від корозії можна розділити на три групи:
1) дія на метал;
2) дія на агресивне середовище;
3) комбіновані методи захисту.
До першої групи методів захисту відносять:
а) легування металів - створення екрануючого поверхневого шару, введення елементів, що знижують катодну або анодну активність сплаву, введення елементів, що запобігають структурній корозії;
б) обробка поверхні металу - термічна і термохімічна обробка, вібраційне плющення поверхні, хімічне і електрохімічне напилення, механічна обробка (наклепання, ролики і т. д.), модифікування іржі на поверхні;
в) нанесення захисних покриттів - постійну, тимчасову і періодичну дії (мастило, віск);
г) підбір корозійностійких матеріалів для умов експлуатації конструкції;
д) раціональне конструювання - виведення окремих вузлів конструкції з агресивних середовищ, виключення застійних зон агресивних рідин;
е) електрохімічний захист.
Друга група методів захисту включає:
а) застосування інгібіторів (сповільнювачів) корозії;
б) герметизація конструкцій (повна або часткова);
в) створення штучних середовищ (обробка водних середовищ, застосування нейтральних середовищ, осушення повітря).
До третьої групи (комбінованим методам захисту) відносять:
а) комплексна дія методів захисту на метал;
б) комплексна дія методів захисту на агресивне середовище;
в) комплексна дія на метал і агресивне середовище.
3.1 КОНТРОЛЮЮЧИЙ ФАКТОР І МЕТОДИ ПРОТИВОКОРОЗІЙННОГО ЗАХИСТУ
Встановивши характер кінетики основних контролюючих стадій корозійного процесу в даних умовах, можна обгрунтовано вибирати найбільш раціональний і ефективнийдля даного випадку методборотьби з корозією.
Існує багато різноманітних методів захисту металів від електрохімічної корозії:
- захисні покриття: на органічній основі (лакофарбні і високополімерні покриття, мастила), на неорганічній основі (окисні, фосфатні, хроматниє і ін.), металеві (металізації, гальванічні, дифузійні, плакированіє).
Захисні покриття можуть сильно розрізнятися по товщині: від дуже тонких- адсорбційні пасивні плівки (десятки ангстрема), до товстих - плакировка, обкладання і футерування (іноді декілька міліметрів);
- обробка корозійного середовища - що знижує її корозійну активність. Наприклад, нейтралізація кислих середовищ і знекиснення води для парових казанів, застосування інгібіторів корозії для рідких і газових середовищ (так званих летючих інгібіторів, що володіють високою пружністю пари і металевих деталей, що застосовуються для тривалої консервації);
Дата добавления: 2015-11-06; просмотров: 1332;
