Закон Гесса (1840) и следствия из него
Тепловой эффект химической реакции зависит только от вида и состояния исходных веществ и конечных продуктов, но не зависит от пути перехода.
Или:
Если из данных исходных веществ можно различными путями получить заданные конечные продукты, то независимо от путей получения, т.е. от вида промежуточных реакций суммарный тепловой эффект для всех путей будет одним и тем же.
Этот закон строго соблюдается для изохорных процессов (когда тепловой эффект равен DU) или для изобарного процесса (когда тепловой эффект равен DH).
Тепловой эффект химической реакции – это тепло, которое поглощается или выделяется в результате химического процесса, если температура исходных веществравна температуре продуктов реакции.
Некоторые определения, связанные с законом Гесса и его следствиями.
Tеплота образования – это тепловой эффект реакции образования данного соединения из простых веществ, отвечающих наиболее устойчивому состоянию рассматриваемого элемента при данной температуре.
Teплотой сгорания называется тепловой эффект реакции окисления данного соединения кислородом с образованием высших окислов соответствующих елементов или соединений этих окислов.
Следствия из закона Гесса:
1) тепловой эффект реакции равен разности между теплотами образования всех веществ, указанных в правой части уравнения, и теплотами образования всех веществ, указанных в левой части уравнения реакции (взятых с коэффициентами, равными коэффициентам перед формулами этих веществ в уравнении самой реакции).
Математически :
DHoх.р. = å(nDHoобр)прoд - å(nDHoобр)реаг,
гдe DHoобр. - тепловой эффект образования вещества в стандартных условиях (t=25C или 298K, p=1 атм)
2) тепловой эффект реакции равен разности между теплотами сгорания всех веществ, указанных в левой части уравнения, и теплотами сгорания всех веществ, указанных в правой части уравнения реакции (взятых с коэффициентами соответствующими стехиометрическими коэффициентам). Математически :
DHoхр = å(nDHocгор)рeaг - å(nDHocгoр)прoд, гдe DHoсгор. - тепловой эффект сгорания вещества в стандартных условиях (t=25C или 298K, p=1 атм)
3) Тепловой эффект разложения сложного вещества на простые вещества равен по величине и противоположен по знаку тепловому эффекту образования этого вещества из простых составляющих. DHoобр. = -DHoразл.
Закон Гесса и следствия из него широко применяются для определения тепловых эффектов различных реакций. В частности, можно определить эффективность топлива применяемого для различного рода двигателей. Эффективность топлива – это количество тепла, выделяющегося при реакции сгорания 1 кг реагентов
DHf = 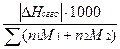
При расчетах нужно быть внимательным при использовании справочных данных:
-вещества находятся в одинаковых условиях (температура, давление );
-тепловой эффект образования простых веществ в их наиболее стабильных состояниях равен нулю;
-тепловой эффект реакции зависит от фазового состояния вещества (это - газ, жидкость или твердое вещество, и от кристаллической модификации твердого вещества), фазовое состояние отмечается индексом возле символа (химической формулы) вещества.
Дата добавления: 2015-11-04; просмотров: 1015;
