Обучающие задачи. Задача 1. Какой объем раствора серной кислоты с массовой долей 98 % (ρ = 1,81г/мл) необходимо взять для приготовления 500 мл раствора с молярной
Задача 1. Какой объем раствора серной кислоты с массовой долей 98 % (ρ = 1,81г/мл) необходимо взять для приготовления 500 мл раствора с молярной концентрацией кислоты 0,25 моль/л. (Кз=1,86 кг×К/моль)
Решение:
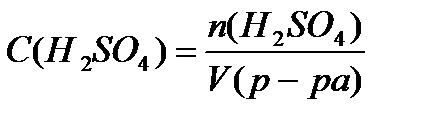
n (H2SO4) = C (H2SO4) × V (p-pa) = 0,25 моль/л×0,5л = 0,125моль
2. m (H2SO4) = n (H2SO4)×M (H2SO4)
M (H2SO4) = 2 + 32 + 64 = 98 г/моль
m (H2SO4) = 0,125моль×98 г/моль = 12,25 г
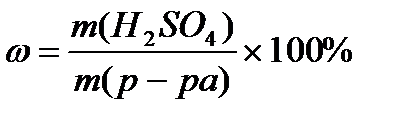
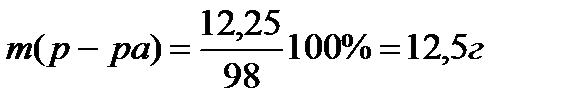

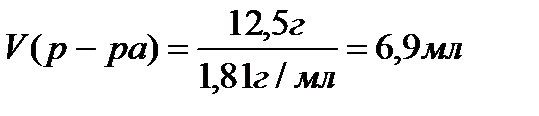
Ответ: V(р-ра) = 6,9 мл
Задача 2. Вычислите температуру замерзания раствора, содержащего 10г глюкозы в 180г воды (изотонический раствор).
Решение:
1. DTзам = K∙× b (C6H12O6)
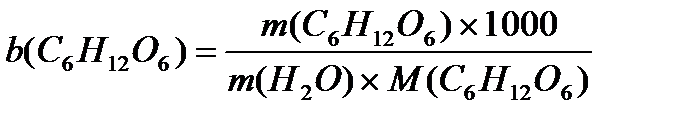
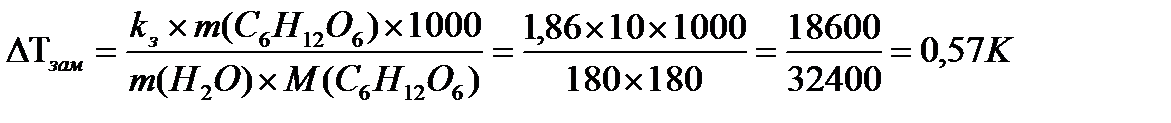
Tзам раствора = Tзам. р-ля - DTзам.
Tзам. раствора = 273 - 0,57 = 272,430К или -0,570С
Ответ: -0,570 С
Задача 3. Определите осмотическое давление при 370С в растворе с молярной концентрацией NaCl 0,16 моль/л. Будет ли этот раствор изотоничен плазме крови? Изотонический коэффициент NaCl равен 1,95.
Решение:
p = i×C (NaCl)∙×R×T R = 8,31 кПа×л/моль×К T = 273 + 37 = 310 K
p = 1,95 × 0,16моль/л × 8,31кПа×л/моль×К × 310К = 803,7 кПа
Осмотическое давление близко плазме крови, раствор изотоничен плазме крови.
Дата добавления: 2015-10-19; просмотров: 3349;
