Реакция комплексообразования с ионами железа (III)
Основана на свойствах фенольного гидроксила образовывать с ионами железа 3+ растворимые комплексные соединения, окрашенные чаще в синий (фенол) или фиолетовый цвет (резорцин, кислота салициловая) реже в красный (ПАСК – натрия) и зелёный (хинозол, адреналин – пирокатехиновый фрагмент).
Состав комплексов обусловлен количеством фенольных –ОН, влиянием других функциональных групп, реакцией среды:с избытком Br2
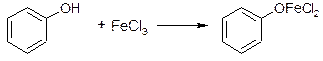
Синее окрашивание
При избытке фенола:
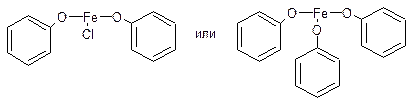
|
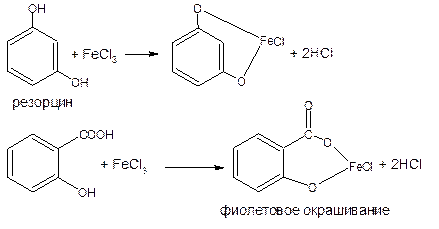
2. Реакции окисления. Фенолы легко окисляются, образуя о- или п-хиноны (циклические дикетоны), окрашенные в розовый, реже жёлтый цвет:
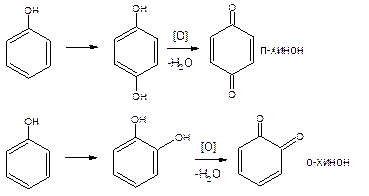 или
или 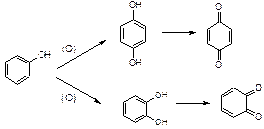
Реакции образования индофенолового или индоаминового красителя:
а) Основана на окислении фенолов до хинонов, которые при конденсации с аммиаком или аминопроизводным и избытком фенола образуют индофеноловый краситель, окрашенный в сине-фиолетовый цвет.
Окислитель – хлорная известь
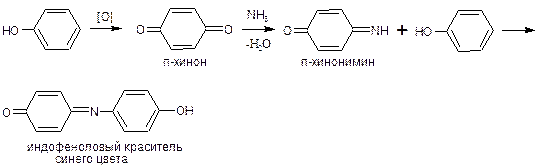
или 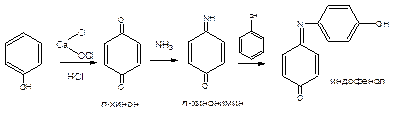
б) Реакция рекомендована для веществ, образующих в результате гидролиза
п-аминофенол (парацетамол), который обнаруживают образованием индоамина (по свойствам родственный индофенолу). Окислитель – дихромат калия в кислой среде.
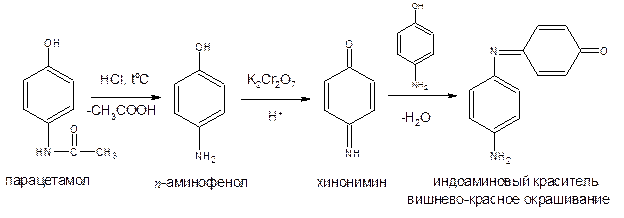
в) Разновидностью данной реакции является нитрозореакция Либермана, она характерна для фенолов, не имеющих заместителей в о- и п-положениях.
При действии окислителя – нитрита натрия в кислой среде образуется
п-нитрозофенол, изомеризующийся в п-хиноидоксим, который, реагируя с избытком фенолав кислой среде, образует индофенол:
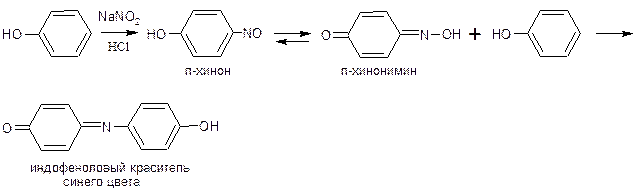
3. Реакции электрофильного замещения Sе .
3.1 Реакции галогенирования. Реакция галогенирования ароматического ядра основана на электрофильном замещении водорода на галоген.
Основные правила бромирования:
1)водород замещается в о- и п-положениях по отношению к фенольному ОН (наиболее реакционноспособно п-положение):
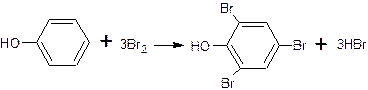
2)при наличии в о- или п-положениях заместителей, в реакцию вступает меньше атомов брома (тимол - дипроизводное):
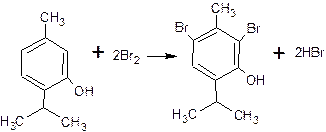
3)если в о- или п-положениях находится карбоксильная группа (салициловая кислота), то происходит с избытком брома декарбоксилирование и образование трибромпроизводного:
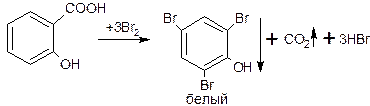
4)наличие заместителей в м-положениях не препятствует образованию трибромпроизводного (мезатон):
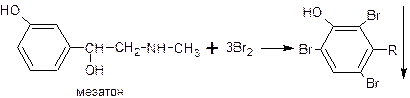
5) если в соединении два фенольных гидроксила в м-положении, то в результате их согласованной ориентации образуется трибромпроизводное
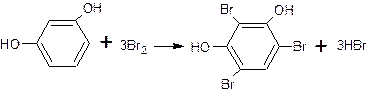
6) если же две гидроксильные группы в о- или п-положениях, то они действуют несогласованно, бромирования не происходит (адреналин, норадреналин)
3.2 Реакции азосочетания с диазореактивом в щелочной среде. Продукт реакции – азокраситель. Сочетание идет также в о- и п-положениях, в этом случае также, как и при бромировании, предпочтительным является п-положение.
Диазореактив – соль диазония (диазотированная нитритом натрия с среде разв.хлороводородной кислоты сульфаниловая кислота):резорцин
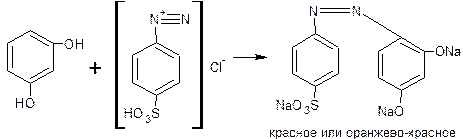
3.3 Реакции образования нитросоединений (аци-солей).При взаимодействии с разведенной азотной кислотой фенолы могут нитроваться при комнатной температуре, образуя о- и п-нитропроизводные, которые могут существовать в двух таутомерных формах:
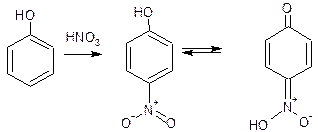
Нитропроизводное содержит в п-положении подвижный атом водорода гидроксильной группы, образуется таутомерная аци-форма с хиноидной структурой, она обычно окрашена в желтый цвет. Добавление щелочи усиливает окраску, вследствие образования хорошо диссоциируемой аци-соли:
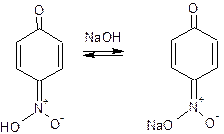
Дата добавления: 2015-09-07; просмотров: 6584;
