Випарювання 4 страница
Д/з: [1] с.148-151, [3] с. 175-179
4.5. Конденсація
План
1. Загальні відомості
2. Поверхневі конденсатори
3. Конденсатори змішування
1. Конденсацією називають процес перетворення пари (газу) в рідкий стан. Зрідження пари відбувається під час її охолодження, а газу – стисненням з наступним охолодженням. Процес конденсації широко застосовують у харчових виробництвах, використовуючи теплоту конденсації парів у рекуперативних теплообмінниках з спиртових парів і вуглекислого газу в спиртовому виробництві, для створення розрідження у вакуумних установках тощо. Конденсація може бути самостійним процесом, коли з пари чи газу отримують кінцевий або проміжний продукт виробництва, і допоміжним, наприклад для створення розрідження.
Апарати, в яких відбувається конденсація, називають конденсаторами. Як холодильний агент у них використовують воду, рідше – повітря та інші холодоносії. Далі розглянуто процес конденсації парів.
Практично конденсація пари відбувається при стиканні її з поверхнею стінки, яка їх розділяє, або безпосередньо з холодною водою. У першому випадку апарати називають поверхневими конденсаторами, у другому – конденсаторами змішування.
2. Поверхневі конденсатори
Їх застосовують тоді, коли треба отримати конденсат у чистому вигляді або створити розрідження в апаратах, конденсат вторинної пари в яких є цінним матеріалом. Теплота пари в них відводиться крізь стінку, що омивається з другого боку найчастіше водою. Як поверхневі конденсатори можуть використовуватись будь-які теплообмінні апарати рекуперативного типу. Проте процес теплообміну в них складніший, ніж у теплообмінниках з паровим обігрівом, оскільки відбувається в кілька стадій, відмінних одна від одної.
Розглянемо як наприклад вертикальний кожухотрубний конденсатор (рис.1), призначений для конденсації перегрітої пари в кількості D, кг/с, з наступним охолодженням отриманого конденсату. В такому апараті вздовж трубок заввишки Н проходять послідовно три процеси: охолодження перегрітої пари від температури tп.п., оС, до температури насичення tн (зона I), конденсація насиченої пари при tн = const (зона ІІ) і охолодження отриманого конденсату до заданої кінцевої температури tk (зона ІІІ) .
Оскільки процеси в цих умовно позначених зонах за фізичною суттю різні, то площу поверхні теплообміну Fi розраховують стосовно до теплового навантаження Qi, коефіцієнта теплопередачі ki і середньої різниці температури Δtсрі для кожної зони:
Fi = Qi / (ki Δtсрі)
Тоді загальна площа поверхні теплообміну конденсатора F, м2, дорівнюватиме сумі F1 + F2 + F3.
Позначивши витрати охолоджувальної води W, кг/с, її початкову і кінцеву температури відповідно tв.п. та tв.к. оС, запишемо рівняння теплового балансу в конденсаторі
Q = x (Q1 + Q2 + Q3) = WCB(tв.к. – tв.п.)
де св – питома теплоємність води, Дж/(кг·К);
х – коефіцієнт, що враховує теплові втрати від стінок конденсатора в навколишнє середовище (х = 0,95…0,97).
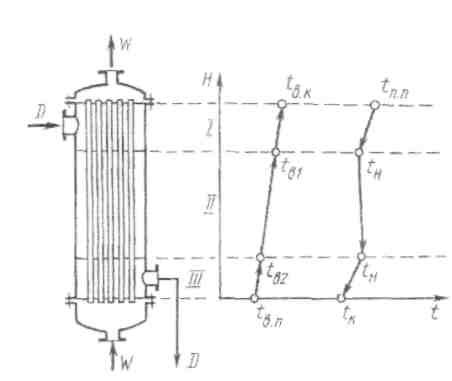
Рис. 1. Схема вертикального поверхневого конденсатора (до теплового балансу)
Щоб розрахувати W, Δtсрі, ki i Fi, складають теплові баланси для кожної зони:
Q1 = xDcn.n.(tn.n. – tн.) = Wcв (tв.к. – tв1);
Q2 = xDr = Wcв(tв1 – tв2);
Q3 = xDcк.(tн. – tк.) = Wcв(tв2 – tв.п.)
де сп.п., ск – питомі теплоємності перегрітої пари і конденсату відповідно,
Дж/(кг·К);
r – теплота конденсації насиченої пари, Дж/кг;
tв1, tв2 – проміжні температури на межі зон, °С.
З урахуванням рівнянь, рівняння теплового балансу в конденсаторі матиме вигляд:
Q = xD(i – cк.tк.) = Wcв(tв.к. – tв.п.)
де і = сп.п.(tп.п. – tп.) + r + cк.tн. – питома ентальпія перегрітої пари, Дж/кг. Звідси витрата охолоджувальної води, кг/с.
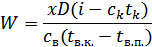
Якщо охолоджувальна вода з конденсатора буде виходити з якнайвищою температурою, то витрати її знизяться. Отриману при цьому гарячу воду можна використати на технічні потреби.
Потрібні для розрахунку Fi проміжні температури охолоджувальної води tв1 і tв2 визначають із рівнянь:
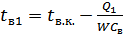 ;
;
r w:top="1134" w:right="850" w:bottom="1134" w:left="1701" w:header="720" w:footer="720" w:gutter="0"/><w:cols w:space="720"/></w:sectPr></w:body></w:wordDocument>"> 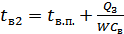 .
.
Визначивши ці величини, можна знайти для кожної зони Δtсрі, Кі і Fi, і загальну площу поверхні конденсатора F. У разі конденсації пари без помітного охолодження конденсату конденсатор розраховують тільки стосовно II зони.
Якщо поверхневі конденсатори використовують для створення розрідження у вакуумних установках, то температура охолоджувальної води має бути нижчою від кінцевої температури конденсату не менше ніж на 5 °С. Ступінь розрідження, яке створюється внаслідок зменшення об'єму пари під час її конденсації, залежить від початкової температури охолоджувальної води та її питомої витрати m = W/D, що може досягати 100...110 кг води на 1 кг пари. Чим більша різниця між температурою конденсації пари і кінцевою температурою утвореного конденсату, тим більшим буде розрідження в конденсаторі. Кількість повітря і газів, що не конденсуються і відсмоктуються з конденсатора, залежить від їхнього вмісту в парі та від щільності з'єднань. Вибираючи вакуум-насос, вважають, що при конденсації 1 кг пари в апарат орієнтовно потрапляє 0,008 м повітря.
У поверхневих конденсаторах, в яких охолоджувальним середовищем є повітря (рис. 2), пару через патрубок 6 подають у труби 5, зовнішня поверхня яких виконана ребристою для збільшення поверхні теплообміну з боку повітря. Розподіл пари по трубах і відведення конденсату через патрубок 3 здійснюється за допомогою колекторів 7, розміщених з обох боків апарата. Гази, що не конденсуються, відводяться через патрубок 4. Повітря подають у міжтрубний простір вентилятором 8, що розмішується в патрубку. Щоб збільшити коефіцієнт тепловіддачі від зовнішньої поверхні труб, повітря після вентилятора зволожують, подаючи через форсунки 2 воду.
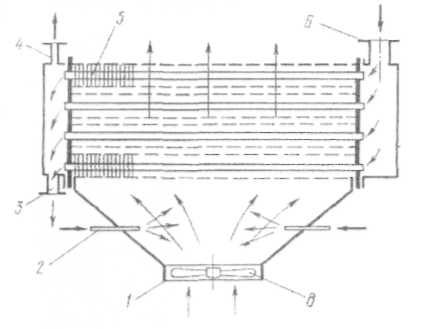
Рис. 2. Схема повітряного поверхневого конденсатора
Процес конденсації може застосовуватись для отримання із парової суміші фракцій конденсату з різним складом і тоді його називають фракційною конденсацією.
Розглянемо як приклад бінарну парову суміш, в якій компонент А має меншу температуру конденсації, ніж компонент В (tл < tiв).Для розрахунку використаємо графічну залежність температур кипіння 1 і конденсації 2 від складу пари і рідини. На горизонтальній осі координат відкладаємо вміст компонента A в рідкій (х) і паровій (y) суміші від 0 до 100% (мас) (% (мол)), а на вертикальній осі – температури кипіння рідини і конденсації пари.
Якщо парову суміш складу y0 (точка С частково конденсувати в першому конденсаторі охолодженням її від 12 до t2, то більшою мірою буде конденсуватись компонент B, а вміст компонента А в отриманій фракції конденсату буде визначатись точкою D1), і дорівнюватиме x1. При цьому пара, яка не конденсується і виходить з конденсатора, збагачується компонентом A (точка С1 вміст у1). Повторивши часткову конденсацію цієї пари в наступному конденсаторі охолодженням її від t2 до t3, отримаємо другу фракцію конденсату з вмістом x2 (x2 >x1) компонента A і так далі. Ступінь конденсації в першому конденсаторі дорівнює відношенню відрізків E1C1/D1C1, у другому – E2C2/D2C2, у третьому – Е3С3/D3C3.
3. Конденсатори змішування
Ці конденсатори застосовують для утилізації теплоти водяних парів низького потенціалу, для конденсації парів рідин, які практично не розчиняються у воді, тощо. Але найчастіше їх використовують для створення розрідження у випарних апаратах, вакуум-фільтрах та інших вакуумних установках, при роботі яких утворюється водяна пара (далі пара).
Пара надходить у камеру змішування конденсатора, де конденсується на поверхні падаючих крапель, струмин або плівок охолоджувальної води, а утворений конденсат змішується з останньою. Підігріта таким чином вода може використовуватись на виробництві.
При конденсації пари об'єм конденсату в тисячу і більше разів менше від об'єму пари, з якої він утворюється. Як наслідок у камері змішування конденсатора і під'єднаному до неї апараті створюється розрідження.
Одночасно з процесом конденсації відбувається накопичення у конденсаторі газів, які надходять разом з парою і не конденсуються, а також повітря, що виділяється з води при розрідженні і проникає крізь нещільності апаратури з навколишнього середовища. Внаслідок накопичення їх (в основному повітрі) зростає парціальний тиск газів і, відповідно, збільшується загальний тиск в апараті. Як наслідок зменшується розрідження в конденсаторі. Тому, щоб підтримати його на потрібному рівні, треба безперервно відводити з конденсатора гази, що не конденсуються, за допомогою вакуум-насоса.
Ефективність роботи конденсаторів змішування прямо залежить від площі поверхні, на якій відбувається теплообмін між водою і парою. Крім того, бажано, щоб ця поверхня не тільки була великою, а й безперервно оновлювалась. Цього досягають відповідною конструкцією камери змішування конденсаторів.
Конденсатори змішування бувають двох типів: мокрі та сухі. Відмінність між ними полягає у способі відведення з них газів, що не конденсуються: з мокрих ці гази відкачуються разом з водою і конденсатом одним і тим же насосом, а з сухих – відводяться окремо. Сухі конденсатори, у свою чергу, бувають низького і високого рівнів: з перших вода з конденсатом відкачується насосом, а з других відводиться самотечією.
Мокрі конденсатори.Їх використовують у малопродуктивних вакуумних установках. Охолоджувальна вода під напором насоса надходить через патрубок 5 в центральну трубу 3 і крізь маленькі отвори в ній розбризкується по всьому простору камери змішування 1. Пару через патрубок 2 подають у верхню частину конденсатора. Суміш конденсату і води разом з газами через патрубок 4 відсмоктують мокроповітряним насосом.
Сухі конденсатори низького рівня.Їх застосовують для вакуумних установок малої і середньої продуктивності. Пару й охолоджувальну воду подають в апарат відповідно через патрубки 3 і 4. Вода під напором насоса або завдяки розрідженню в конденсаторі через сопла 5 розбризкується в камері змішування 1. Через патрубок 6 з конденсатора відкачують воду з конденсатом, а гази відсмоктують вакуум-насосом через патрубок 2.
Сухі барометричні конденсатори високого рівня.Це одна з найпоширеніших конструкцій конденсаторів змішування. їх застосовують для вакуумних установок великої продуктивності. Основним робочим елементом конденсатора (рис. 3) є камера змішування 10 циліндричної форми з сегментними полицями 4, що більше ніж наполовину перекривають переріз конденсатора. Охолоджувальну воду попередньо подають через патрубок 5 у приймач 6, який згладжує її пульсації і в якому з води виділяється значна частина розчиненого повітря, а вже дегазована вода трубою 7 надходить на верхню полицю конденсатора. Вона каскадами стікає вниз з полиці на полицю, створюючи водяні завіси між ними. Рівень води на виставлених горизонтально полицях регулюється підпірними планками заввишки 40...80 мм, що виконують роль бортів полиць.
Через патрубок 3 під нижню полицю підводять пару, і вона рухається вверх звивистим шляхом, поступово конденсуючись на водяних завісах між полицями. У зв'язку з тим що кількість пари по висоті камери змішування поступово зменшується, відстань між полицями також бажано зменшувати від 0,6dк між нижніми полицями до 0,3dк між верхніми (dk – діаметр конденсатора).
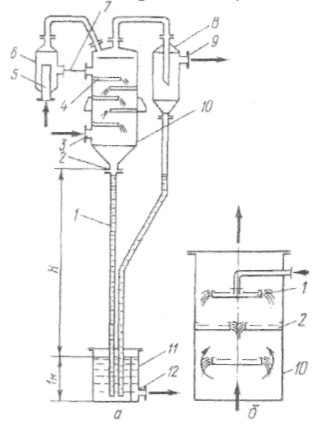
Рис.3. Схеми сухого барометричного конденсатора високого рівня (а) та камери змішування (б)
Суміш конденсату і води, яку називають у таких конденсаторах барометричною водою, через патрубок 2надходить у барометричну трубку 1, що заглиблена під рівень води в збірнику 11. Барометрична труба відіграє роль гідравлічного затвора, який унеможливлює проникання зовнішнього повітря через збірник і трубу в конденсатор і, крім того, дає можливість відводити воду з нього самотечією. Із збірника вода через патрубок 12 видаляється самотечією або відкачується насосом, залежно від мети її використання та висоти розташування збірника. Гази, що не конденсуються, збираються у верхній частині камери змішування і через уловлювач 8 захоплених бризок і патрубок 9 відсмоктуються вакуум-насосом.
У барометричних конденсаторах поряд із суцільними сегментними полицями застосовують перфоровані з отворами діаметром 8...10 мм. У цьому разі крізь отвори проходить у вигляді циліндричних струминок приблизно 40...50% від загальної витрати води. Решта води стікає з полиці через борти плоскими струминами. Це дає можливість збільшити площу поверхні контакту між парою і водою. Недоліком таких полиць є можливе забивання отворів домішками води і накипом.
Ефективним є застосування полиць різної конструкції, які чергуються по висоті камери змішування: верхня полиця 1 з двома бортами розміщується по центру камери змішування, а під нею – дві симетрично розміщені сегментні 2 і т.д. Фрагмент камери змішування 10з такими полицями наведено на рис. 3 б. Завдяки такому розміщенню полиць довжина водозливу (бортів полиць) в конденсаторі збільшується практично вдвічі. Відповідно зростає вдвічі площа поверхні контакту між парою і водою порівняно з конденсатором із сегментними полицями.
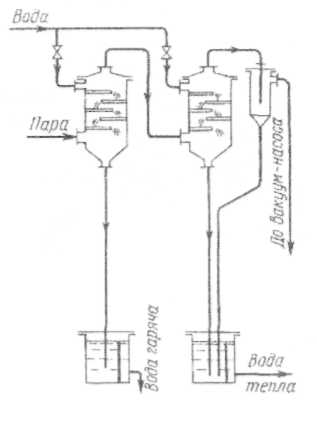
Рис. 4. Схема двоступінчастого барометричного конденсатора
Щоб отримати гарячішу барометричну воду,яку в подальшому використовують для технологічних потреб, застосовують двоступінчастий конденсатор (рис. 4). У перший конденсатор воду подають у недостатній кількості, щоб пара конденсувалася неповністю. Пара, що не сконденсувалась, надходить у другий конденсатор для її повної конденсації,а гази,що не конденсуються, уже з нього відсмоктуються вакуум-насосом. Температура барометричної води в ньому нижча. Змінюючи кількість води,яку подають у перший конденсатор,можна регулювати температуру гарячої води.
Розрахунок поличного барометричного конденсатора.Коли розраховують такий конденсатор, визначають витрати охолоджувальної води, розміри камери змішування: її діаметр, кількість полиць у ній та висоту, а також розміри барометричної труби (діаметр і висоту) та кількість повітря, що відсмоктується вакуум-насосом.
При відомих витратах пари D, кг/с, і тиску в конденсаторі p, Па, витрату охолоджувальної води W, кг/с, визначають з рівняння теплового балансу
Di" + Wсвtв.п. = (D + W)cв.tв.к.
Звідки
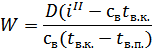
де i" – питома ентальпія пари, Дж/кг;
св – питома теплоємність води, Дж/(кг·К);
tв.п., tв.к. – початкова і кінцева температури води відповідно, °С.
Питома витрата охолоджувальної води m = W/D становить від 15 до 60 кг на 1 кг пари. Температуру барометричної tв.к. беруть на 3...4 °С нижче від температури насичення tн., яка відповідає тиску в конденсаторі р.
Діаметр конденсатора визначають із рівняння витрат при швидкості пари w в його вільному перерізі в межах 12...18 м/с:
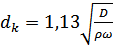
де ρ – густина пари при тиску р в конденсаторі, кг/м3.
За аналогічними формулами розраховують діаметри патрубків і діаметр барометричної труби, підставляючи відповідні витрати, густини та швидкості: 40...50 м/с – для пари; 12...15 – для повітря (газів, що не конденсуються); 1,0...1,2 – для охолоджувальної води і 0,3...0,5 м/с – для барометричної води.
Встановлено, що більша частина пари конденсується на верхніх полицях (тарілках). Тому, щоб спростити розрахунок і конструкцію конденсатора, беруть однаковими відстані між полицями h = 0,5dк та загальні кількості води і конденсату на всіх полицях W1 = W + D. За таких умов кількість полиць можна розрахувати за формулою
n = lg [(tн. – tв.п.) / (tн. – tв.к.)] / lg [(tн. – tв.п.) / (tн. – tв1)]
де tв1 – температура води при вході на другу (зверху) полицю, °С. Цю температуру
розраховують з формули
lg [(tн. – tв.п.) / (tн. – tв.к.)] = 0,029 (gde/w2п.)0,2(h/de)0,7
де de = 2bδ/(b + δ) – еквівалентний діаметр струмини, що стікає з першої полиці, м;
δ = 0,98dк – ширина струмини,що дорівнює довжині борта полиці, м;
δ = V1 / (wср.b) – товщина струмини, м;
V1 = W1 / рв. – об'ємні витрати води, м /с, при середній температурі її tср.=0,5(1в.п.+tв.к.);
Wn = V1 / (bh1) – початкова швидкість стікання води з першої полиці, м/с;
wср. = 0,5 (wп. + 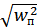 + 2gh)
+ 2gh)
h1 – висота шару води над бортом полиці (водозливом), м
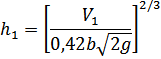
До кількості розрахованих полиць n що не перевищує 7, додають одну, резервну, і визначають висоту камери змішування.
Висота барометричної труби Н від патрубка 2 до рівня води у збірнику 11 дорівнює Н1 + 0,5 м, де Н1 = 10,33 (рр/ра) – висота водяного стовпа в трубі, що відповідає розрідженню pp = pл. – р в конденсаторі й потрібна для врівноваження атмосферного тиску рл., м; 0,5 – запас висоти для компенсації гідравлічних опорів, що виникають під час переміщення води в трубі, і на випадок коливань розрідження в конденсаторі та атмосферного тиску (і, відповідно, рівня води в трубі). З урахуванням висоти нижньої частини барометричної труби, яка заглиблена у збірник на 1,0...1,5 м під рівень води, загальна її висота при розрідженні 87...90 кПа становить не менше ніж 10,5 м.
Кількість повітря, яке відсмоктують з конденсатора за одиницю часу, визначають за емпіричною формулою, кг/с,
Mпов. = 0,0001 (0,025W + 10D)
Об'єм цього повітря, м /с, розраховують за формулою
V = 288mпов. (273 + tпов.) / рпов.
де tп. = tв.п. + 0,1(tв.к. – tв.п.) + 4 – температура повітря, °С;
pn = p – pн1 – парціальний тиск повітря, Па;
рн1 – парціальний тиск пари, що дорівнює тиску насичення при tн., Па; 288 – газова стала повітря, Дж/(кг · К).
Для відсмоктування повітря звичайно застосовують водокільцеві вакуум-насоси, їхня марка відповідає об'єму відсмоктуваного повітря в кубічних метрах за хвилину. Наприклад, вакуум-насос ВВН-12 має продуктивність 12 м3 /хв.
Д/з [1] с. 144-157, [2] с. 216-223
Розділ V. Процеси масообміну
5.1.Теоретичні основи процесів масопередачі
План
1. Загальні відомості про процес.
2. Рівновага фаз.
3. Основне рівняння масопередачі.
4. Загальні відомості про процес адсорбції.
5. Види адсорбентів.
1. Масообміни – це процеси, сутність яких складає перенос речовини з однієї фази в іншу.
Кожна речовина складається з фаз.
Фаза – це визначна кількість речовини, однорідної за всією масою.
Системи можуть бути однофазними (вода у вигляді рідини), двофазними (вода та її пара) та багатофазними (вода, крига та пара).
Фази у системі відокремлюються одна від одної поверхнями розділу.
Системи, які складаються з декількох фаз, називаються гетерогенними або неоднорідними.
Перехід речовини з однієї фази в іншу при масообміні здійснюється шляхом дифузії.
2. Основною умовою протікання масо обмінного процесу є порушення рівноваги між фазами, яке може відбутися при зміні температури (t), тиску (Р) або складу хоча б однієї з фаз. Процес при цьому буде проходити до тих пір, поки знову не встановлюється рівновага.
Для того, щоб процес протікав, фази повинні бути приведені в контакт, і чим більше поверхня контакту фаз і концентрація відрізняється від рівноважної, тим більше буде швидкість масообмінного процесу. При наближенні системи до стану рівноваги рухома сила, а слід, і швидкість процесу зменшуються.
3. Кількість речовини, що продифундувала крізь деяку поверхню, може бути розрахована за допомогою рівняння масопередачі:
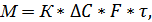
де: М – маса речовини, що переходе з однієї фази в іншу, кг;
К – кінематичний коефіцієнт, який враховує опір в процесі переносу;
∆С - середня різниця концентрації, кг/кг, кмоль/кмоль, кг/м3 тощо;
F – площина між фазової поверхні, крізь яку здійснюється перенос речовини, м2;
τ – тривалість процесу, с.
Коефіцієнт масопередачі. Розмірність його залежить від розмірності, прийнятої для концентрації. Наприклад, якщо
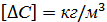 , то
, то 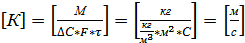
якщо кг/кг
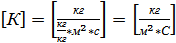
Фізична сумісність коефіцієнта К: коефіцієнт масопередачі показує, яка кількість речовини переноситься крізь 1м2 поверхні фазового розділу за 1 с при різниці концентрацій = 1.
К не залежить від площини поверхні, часу і концентрацій. Він залежить від властивостей речовин, які приймають участь у процесі, та характеру взаємодіє фаз.
4. Адсорбція – процес вибіркового поглинання компонента газу, пари або розчину поверхнею твердої речовини.
Для того, щоб процес був ефективним, поверхня поглинання повинна бути великою. Тому для адсорбції застосовують пористі речовини, які володіють величезною поверхнею.
Тверде тіло, на поверхні пор якого конденсується вбирана речовина, називається адсорбентом, вбирана речовина – адсорбтивом, вона ж у концентрованому вигляді на повехні адсорбенту – адсорбентом.
Розрізняють фізичну адсорбцію та хімічну (хемосорбцію).
Фізична адсорбція пояснюється взаємним притяганням молекул адсорбенту і адсорбтиву. При цьому не виникає хімічної взаємодії. Фізична адсорбція оборотня, при зміненні умов (t, Р) процес може розвиватися у протилежному напрямку і виникає десорбція – виділення раніше адсорбованої речовини з адсорбенту.
У випадку хемосорбції між молекулами адсорбенту та адсорбтиву відбувається хімічна реакція та виникає хімічний зв’язок.
В харчовій промисловості адсорбція застосовується на стабілізації вин, освітленні соків у консервному виробництві, рафінації рослинної олії, стабілізації пива.
5. Адсорбенти повинні володіти надзвичайно розвинутою поверхнею, що досягається за рахунок утворення великої кількості пор в твердому тілі.
1) Активоване вугілля – найбільш поширений адсорбент. Активна поверхня 1 г активованого вугілля складає від 600 до 1700 м2. Розміри частинок активного вугілля від 1 до 5 мм.
Переваги: краще поглинає пари органічних речовин, ніж пари води.
Недоліки: мала механічна міцність та горючість.
2) Костяне вугілля – його отримують із знежирених кліток крупних тварин шляхом пропікання їх в реостатах без допуску повітря. Розмір частинок приблизно 3 мм. Поверхня пор вкрита дуже тонким шаром вуглецю, який має дуже високу адсорбційну поверхню.
3) Силікагель – зневоднений гель кремнієвої кислоти. Розмір гранул від 0,2 до 7 мм. Сумарна площа поверхні 1 г – 400-770 м2. Селікагелі здатні поглинати до 50 % свої маси.
Переваги: поглинає пари органічних речовин, вологу з повітря та газів. Негорюч, має велику механічну міцність.
Також застосовують штучні адсорбенти: цеоліти, іоніти (аніоніти та катіоніти).
В якості природних адсорбентів в харчовій промисловості (для освітлення вин) застосовують дрібнодисперсні глини, бетоніт, каолін. Також застосовують риб’ячий клей (желатин).
4) Целюлозна маса має меншу питому поверхню, ніж вугілля і силікагель. Застосовується при освітленні соків і пива.
Д/з [1] c. 237-241, [2] c. 240-242.
5.2. Абсорбція
План
1. Теоретичні відомості про процес
2. Абсорбери
1. Абсорбцією називають процеси поглинання газів або пари рідиною. Для більшості випадків цей процес оборотний, тобто в певних умовах, наприклад при нагріванні, можна виділити газ з рідини. Такий процес називають десорбцією. Поєднання абсорбції і десорбції дозволяє створити безперервні промислові виробництва з багатократним використовуванням рідкого поглинача і виділенням в чистому виді речовини, поглиненої з парогазовой суміші. В харчових виробництвах процеси абсорбції займають значне місце. Наприклад, при виробництві спирту з що утворюється в результаті бродіння вуглекислого газу абсорбцією уловлюють пари спирту, а потім обчищений газ зріджують для використовування в інших виробництвах.Процес насичення мінеральної води і інших численних напоїв вуглекислим газом, в спеціальній технології званий сатурацией, насправді служить класичним прикладом процесу абсорбції.
Закон Генрі. Рівновага при абсорбції. Кількість газу, яка може
поглинути рідину, залежить від властивостей газу в рідині, температури і парціального тиску поглинального газу в газовій суміші над поверхнею абсорбції. Для прикладу розглянемо розділення бінарної газової суміші, що складається з компонентів А і В хай рідина поглинає компонент А. Определить число ступенів свободи для цієї системи, скориставшися правилом фаз
Ф + С = К + 2,
где Ф – число фаз;
С – число ступенів свободи;
К – число компонентов.
Для нашого прикладу Ф = 2, оскільки в процесі беруть участь дві фази: газ і рідина. Число компонентів До = 3, газові компоненти А і В і третій - поглинає рідину. Тоді число ступенів свободи З = 3 + 2 - 2 = 3
Три ступені свободи тут - три змінні параметри: температура, тиск і концентрація. Зміна будь-якого з них порушує сталу рівновагу. В стані рівноваги, при постійних температурах і загальному тиску, концентрації компоненту А в газовій суміші відповідає певна концентрація цього компоненту в рідині. Цей закон, відомий як закон Генрі, записується наступним рівнянням:
Дата добавления: 2015-10-13; просмотров: 2702;
