рЕНПЕРХВЕЯЙНЕ ББЕДЕМХЕ. рЕґОґКНґБНЕ УЮНґРХґВЕґЯЙНЕ ДБХґФЕґМХЕ ЛНґКЕґЙСК ЦЮґГЮ ЯОНґЯНАґЯРґБСґЕР ЯЦКЮґФХґБЮґМХЧ БЯЪґЙХУ ПЮГґКХґВХИ ЛЕґФґДС ПЮБґМШґЛХ ВЮЯґРЪґЛХ ЦЮґГЮ
рЕґОґКНґБНЕ УЮНґРХґВЕґЯЙНЕ ДБХґФЕґМХЕ ЛНґКЕґЙСК ЦЮґГЮ ЯОНґЯНАґЯРґБСґЕР ЯЦКЮґФХґБЮґМХЧ БЯЪґЙХУ ПЮГґКХґВХИ ЛЕґФґДС ПЮБґМШґЛХ ВЮЯґРЪґЛХ ЦЮґГЮ. оНґЩРНґЛС, ЕЯґКХ ЛШ ХЛЕґЕЛ ЯКНХ ЦЮґГЮ, ДБХґФСґЫХЕґЯЪ Я ПЮГґКХВґМШґЛХ ОН БЕґКХґВХґМЕ ЯЙНґПНґЯРЪґЛХ, РН МЮ СОНґПЪґДНґВЕМґМНЕ ДБХґФЕґМХЕ ЯКНґЕБ ЦЮґГЮ Я ПЮГґКХВґМШґЛХ ЯЙНґПНґЯРЪґЛХ МЮґЙКЮґДШґБЮґЕРґЯЪ УЮНґРХґВЕґЯЙНЕ ДБХґФЕґМХЕ ЛНґКЕґЙСК. лНґКЕґЙСґКШ ОЕґПЕґУНґДЪР ХГ ЯКНЪ, ДБХґФСґЫЕґЦНґЯЪ ЯН ЯЙНґПНґЯРЭЧ v1, Б ЯКНИ, ДБХґФСґЫХИґЯЪ ЯН ЯЙНґПНґЯРЭЧ v2, Х НАґПЮРґМН, ОЕґПЕґМНґЯЪ ОПХ ЩРНЛ ХЛґОСКЭЯ. рЮґЙНИ ОПНґЖЕЯЯ ОЕґПЕґМНґЯЮ ХЛґОСКЭґЯЮ, БШґПЮБґМХґБЮЧґЫХИ ЯЙНґПНґЯРХ НРґДЕКЭґМШУ ЯКНґЕБ, ЯНґОПНґБНґФґДЮґЕРґЯЪ ОПЕґБПЮґЫЕґМХґЕЛ ЙХґМЕґРХґВЕґЯЙНИ ЩМЕПґЦХХ СОНґПЪґДНґВЕМґМНґЦН ДБХґФЕґМХЪ ДЮМґМНґЦН ЯКНЪ Б ЩМЕПґЦХЧ РЕґОґКНґБНґЦН ДБХґФЕґМХЪ ЛНґКЕґЙСК Х МЮґГШґБЮґЕРґЯЪ БМСРґПЕМґМХЛ РПЕґМХґЕЛ. гЮґЙНМ мЭЧґРНґМЮ ДКЪ БМСРґПЕМґМЕґЦН РПЕґМХЪ ХЛЕЕР БХД:
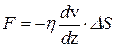 . (12.1)
. (12.1)

 гДЕЯЭ η √ ЙНЩТТХЖХЕМР БЪГЙНЯРХ, ВХЯКЕММН ПЮБМШИ ЯХКЕ БЪГЙНЦН РПЕМХЪ ЛЕФДС ДБСЛЪ ЯКНЪЛХ ЕДХМХВМНИ ОКНЫЮДХ ОПХ ЕДХМХВМНЛ ЦПЮДХЕМРЕ ЯЙНПНЯРЕИ. щРНР ГЮґЙНМ ЛНФґМН БШґБЕЯґРХ, ХЯґОНКЭґГСЪ НЯґМНБґМШЕ ОНґКНґФЕґМХЪ ЛНґКЕґЙСґКЪПґМН-ЙХґМЕґРХґВЕґЯЙНИ РЕНґПХХ. оСЯРЭ С МЮЯ ХЛЕґЧРґЯЪ ДБЮ ЯКНЪ ЦЮґГЮ, ДБХґФСґЫХЕґЯЪ ЯН ЯЙНґПНґЯРЪґЛХ v1Х v2 (ПХЯ.12.1). бШДЕКХЛ ЛШЯКЕММН Б ЯПЕДЕ ЙЮЙСЧ-РН ОКНЫЮДЙС ΔS Х МЮОПЮґБХЛ НЯЭ zНПРНЦНМЮКЭМН Й МЕИ. дБЕ ДПСЦХЕ НЯХ У Х С ОЮПЮККЕКЭМШ ОКНЫЮДґЙЕ. уЮНРХВМНЯРЭ ДБХФЕМХЪ ЛНКЕЙСК ЯЛНДЕКХПСЕЛ ЯКЕДСЧЫХЛ НАПЮГНЛ. аСДЕЛ ЯВХРЮРЭ, ВРН ПНБМН 1/3 ЛНКЕЙСК ДБХФЕРЯЪ БДНКЭ НЯХ У, 1/3 √ БДНКЭ НЯХ С Х 1/3 √ БДНКЭ НЯХ z. хГ ЛНКЕЙСК, КЕґРЪЫХУ ОЮПЮККЕКЭМН z, ПНБМН ОНКНБХґМЮ(1/6 ВЮЯРЭ ОНКМНЦН ВХЯКЮ ЛНКЕЙСК) ДБХФЕРЯЪ Б ОНКНФХРЕКЭМНЛ МЮОПЮБКЕґМХХ, Х ЯРНКЭЙН ФЕ √ Б НРПХЖЮРЕКЭМНЛ. оНДЯВХРЮЕЛ ЙНКХВЕЯРБН ЛНКЕЙСК N, ОЕґПЕЯЕЙЮЧЫХУ ОКНЫЮДЙС ΔS Б ЕДХМХЖС БПЕЛЕМХ. ъЯМН, ВРН ЛНКЕЙСґКШ, КЕРЪЫХЕ БДНКЭ НЯЕИ У Х С,ОКНЫЮДґЙС МЕ ОЕПЕЯЕЙСР. гЮ БПЕЛЪ Δt ЛНКЕЙСКШ ОПЕНДНКЕБЮЧР ПЮЯЯРНЪМХЕ
гДЕЯЭ η √ ЙНЩТТХЖХЕМР БЪГЙНЯРХ, ВХЯКЕММН ПЮБМШИ ЯХКЕ БЪГЙНЦН РПЕМХЪ ЛЕФДС ДБСЛЪ ЯКНЪЛХ ЕДХМХВМНИ ОКНЫЮДХ ОПХ ЕДХМХВМНЛ ЦПЮДХЕМРЕ ЯЙНПНЯРЕИ. щРНР ГЮґЙНМ ЛНФґМН БШґБЕЯґРХ, ХЯґОНКЭґГСЪ НЯґМНБґМШЕ ОНґКНґФЕґМХЪ ЛНґКЕґЙСґКЪПґМН-ЙХґМЕґРХґВЕґЯЙНИ РЕНґПХХ. оСЯРЭ С МЮЯ ХЛЕґЧРґЯЪ ДБЮ ЯКНЪ ЦЮґГЮ, ДБХґФСґЫХЕґЯЪ ЯН ЯЙНґПНґЯРЪґЛХ v1Х v2 (ПХЯ.12.1). бШДЕКХЛ ЛШЯКЕММН Б ЯПЕДЕ ЙЮЙСЧ-РН ОКНЫЮДЙС ΔS Х МЮОПЮґБХЛ НЯЭ zНПРНЦНМЮКЭМН Й МЕИ. дБЕ ДПСЦХЕ НЯХ У Х С ОЮПЮККЕКЭМШ ОКНЫЮДґЙЕ. уЮНРХВМНЯРЭ ДБХФЕМХЪ ЛНКЕЙСК ЯЛНДЕКХПСЕЛ ЯКЕДСЧЫХЛ НАПЮГНЛ. аСДЕЛ ЯВХРЮРЭ, ВРН ПНБМН 1/3 ЛНКЕЙСК ДБХФЕРЯЪ БДНКЭ НЯХ У, 1/3 √ БДНКЭ НЯХ С Х 1/3 √ БДНКЭ НЯХ z. хГ ЛНКЕЙСК, КЕґРЪЫХУ ОЮПЮККЕКЭМН z, ПНБМН ОНКНБХґМЮ(1/6 ВЮЯРЭ ОНКМНЦН ВХЯКЮ ЛНКЕЙСК) ДБХФЕРЯЪ Б ОНКНФХРЕКЭМНЛ МЮОПЮБКЕґМХХ, Х ЯРНКЭЙН ФЕ √ Б НРПХЖЮРЕКЭМНЛ. оНДЯВХРЮЕЛ ЙНКХВЕЯРБН ЛНКЕЙСК N, ОЕґПЕЯЕЙЮЧЫХУ ОКНЫЮДЙС ΔS Б ЕДХМХЖС БПЕЛЕМХ. ъЯМН, ВРН ЛНКЕЙСґКШ, КЕРЪЫХЕ БДНКЭ НЯЕИ У Х С,ОКНЫЮДґЙС МЕ ОЕПЕЯЕЙСР. гЮ БПЕЛЪ Δt ЛНКЕЙСКШ ОПЕНДНКЕБЮЧР ПЮЯЯРНЪМХЕ 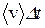 , ЦДЕ
, ЦДЕ 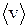 √ ЯПЕДМЪЪ ЮПХТЛЕРХВЕЯЙЮЪ ЯЙНПНЯРЭ. оНґРНЛС МЮ ОКНЫЮДЙС ОНОЮДЕР РНКЭЙН 1/6 ВЮЯРЭ ЛНКЕЙСК ХГ НАЗЕЛЮ
√ ЯПЕДМЪЪ ЮПХТЛЕРХВЕЯЙЮЪ ЯЙНПНЯРЭ. оНґРНЛС МЮ ОКНЫЮДЙС ОНОЮДЕР РНКЭЙН 1/6 ВЮЯРЭ ЛНКЕЙСК ХГ НАЗЕЛЮ 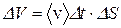 , РН ЕЯРЭ
, РН ЕЯРЭ
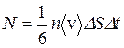 , (12.2)
, (12.2)
ЦДЕ 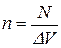 √ ЙНМЖЕМРПЮЖХЪ ЛНКЕЙСК.
√ ЙНМЖЕМРПЮЖХЪ ЛНКЕЙСК.
хЛОСКЭЯ, ОЕґПЕґМНґЯХґЛШИ ОНґРНґЙНЛ ЛНґКЕґЙСК ГЮ БПЕЛЪ Δt ВЕПЕГ ОКНЫЮДЙС ΔS Б ОНґКНґФХґРЕКЭґМНЛ МЮґОПЮБґКЕґМХХ НЯХ zХГ ЯКНЪ, ДБХґФСґЫЕґЦНґЯЪ ЯН ЯЙНґПНґЯРЭЧ v1 (ПХЯ.12.2), ПЮБЕґМ:

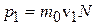 , (12.3)
, (12.3)
ЦДЕ 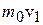 √ ХЛОСКЭЯ НДМНИ ЛНКЕЙСКШ, ЯБЪГЮММШИ Я МЮОПЮБКЕММШЛ ДБХФЕМХЕЛ ЛНКЕЙСК.
√ ХЛОСКЭЯ НДМНИ ЛНКЕЙСКШ, ЯБЪГЮММШИ Я МЮОПЮБКЕММШЛ ДБХФЕМХЕЛ ЛНКЕЙСК.
хЛОСКЭЯ, ОЕПЕМНЯХЛШИ Б ОПНРХБНОНКНФМНЛ МЮОПЮБКЕМХХ, ПЮБЕМ
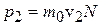 . (12.4)
. (12.4)
оНКМНЕ ХГґЛЕґМЕґМХЕ ХЛґОСКЭґЯЮ ЯКНЪ ОНКСВХЛ ХГ (12.2-12.4):
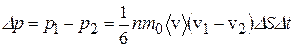 . (12.5)
. (12.5)
оНЯКЕДМХИ ПЮГ ОЕПЕД ОНОЮДЮМХЕЛ МЮ ОКНЫЮДЙС ΔS ЛНКЕЙСКШ ЯРЮКЙХБЮКХЯЭ Я ДПСЦХЛХ ЛНКЕЙСКЮЛХ МЮ ПЮЯЯРНЪМХХ ДКХМШ ЯБНАНДМНЦН ОПНАЕЦЮ λ НР ОКНЫЮДЙХ. оНЩРНЛС Й БШДЕКЕММНИ МЮЛХ ОКНЫЮДХ НМХ ОНДУНДЪР Я РЕЛХ ХЛОСКЭЯЮЛХ ВЮЯРХЖ, ЙНРНПШЕ ЯКНФХКХЯЭ Б РНВЙЮУ Я ЙННПДХМЮРЮЛХ (z√λ)Х (z+λ)ЯННРБЕРЯРБЕММН (z √ ЙННПДХМЮРЮ ОКНЫЮДЙХ) Х ЯННРБЕРЯРБСЧР ЯЙНПНЯРЪЛ МЮОПЮБКЕММНЦН ДБХФЕМХЪ v2 Х v1 (ПХЯ.12.2).
оНЯЙНКЭЙС ДКХМЮ ЯБНАНДМНЦН ОПНАЕЦЮ λ ЛЮКЮ, РН ПЮГґМНЯРЭ ЯЙНґПНґЯРЕИ 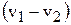 ЛНФґМН БШґПЮґГХРЭ ВЕґПЕГ ЦПЮґДХґЕМР ЯЙНґПНґЯРХ Х ДКХґМС ЯБНґАНДґМНґЦН ОПНґАЕґЦЮ ЛНґКЕґЙСК l:
ЛНФґМН БШґПЮґГХРЭ ВЕґПЕГ ЦПЮґДХґЕМР ЯЙНґПНґЯРХ Х ДКХґМС ЯБНґАНДґМНґЦН ОПНґАЕґЦЮ ЛНґКЕґЙСК l:
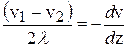 . (12.6)
. (12.6)
сВХґРШґБЮЪ, ВРН nm0=r (ОКНРґМНЯРЭ БЕґЫЕґЯРґБЮ), ХГ (12.5) Х (12.6) ОНКСВХЛ:
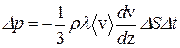 . (12.7)
. (12.7)
оН БРНПНЛС ГЮЙНМС мЭЧРНМЮ ХГґЛЕґМЕґМХЕ ХЛґОСКЭґЯЮ РЕґКЮ ПЮБМН ХЛґОСКЭґЯС ЯХґКШ: 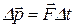 , РНЦДЮ
, РНЦДЮ
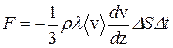 . (12.8)
. (12.8)
лШ БШБЕКХ ГЮЙНМ мЭЧРНМЮ (12.1) ДКЪ БЪГЙНЯРХ Х ОНКСВХКХ БШПЮФЕМХЕ ДКЪ ЙНЩТТХЖХЕМРЮ ДХМЮЛХВЕЯЙНИ БЪГЙНЯРХ:
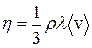 . (12.9)
. (12.9)
рЕОЕПЭ ЛНФМН СЯРЮМНБХРЭ ГЮБХЯХЛНЯРЭ БЪГЙНЯРХ ЦЮГЮ НР РЕЛОЕПЮРСПШ: ОНЯЙНКЭЙС ЯПЕДМЪЪ ЮПХТЛЕРХВЕЯЙЮЪ ЯЙНПНЯРЭ
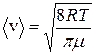 , (12.10)
, (12.10)
Ю ДКХМЮ ЯБНАНДМНЦН ОПНАЕЦЮ ЛНКЕЙСК
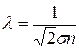 , (12.11)
, (12.11)
РН ОПХ ОНЯРНЪММНИ ЙНМЖЕМРПЮЖХХ ЛНКЕЙСК (МЮОПХЛЕП, Б ХГНУНПМНЛ ОПНЖЕЯЯЕ) БЪГЙНЯРЭ Я ОНБШЬЕМХЕЛ РЕЛОЕПЮРСПШ СБЕКХВХБЮЕРЯЪ ОПНОНПЖХНМЮКЭМН 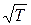 .
.
оНКСВХЛ БШПЮФЕМХЕ ДКЪ ПЮЯВ╦РЮ ЯПЕДМЕИ ДКХМШ ЯБНАНДМНЦН ОПНАЕЦЮ ЛНКЕЙСК ХГ (12.9) Я СВ╦РНЛ (12.10):
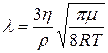 . (12.12)
. (12.12)
оКНРМНЯРЭ ЦЮГЮ БШПЮГХЛ ХГ СПЮБМЕМХЪ лЕМДЕКЕЕБЮ-йКЮОЕИПНМЮ 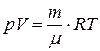 :
: 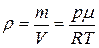 , РНЦДЮ ХГ (12.12):
, РНЦДЮ ХГ (12.12): 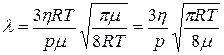 , ХКХ
, ХКХ
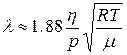 , (12.13)
, (12.13)
ЦДЕ p=105 оЮ √ ЮРЛНЯТЕПМНЕ ДЮБКЕМХЕ; μ=0.029 ЙЦ/ЛНКЭ √ ЛНКЪПМЮЪ ЛЮЯЯЮ БНГДСУЮ; R √ СМХБЕПЯЮКЭМЮЪ ЦЮГНБЮЪ ОНЯРНЪММЮЪ.
дЮРЮ ДНАЮБКЕМХЪ: 2015-09-07; ОПНЯЛНРПНБ: 655;
