Получение солей
Способы получения солей основаны на различных реакциях с участием простых веществ, оксидов, кислот, оснований и солей. Многие соли образуются при взаимодействии:
· Металлов с неметаллами:
2Na + Cl2 = 2NaCl; Zn + S = ZnS;
· Основных оксидов с кислотами:
СaO + 2HCl = CaCl2 + H2O;
· Кислотных оксидов со щелочами:
CO2 + Ba(OH)2 = BaCO3¯ + H2O;
· Амфотерных оксидов с кислотами:
SnO + 2HCl = SnCl2 + H2O;
· Амфотерных оксидов со щелочами:
SnO + 2KOH(распл) 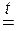 K2SnO2 + H2O; Al2O3 + 2NaOH (распл)
K2SnO2 + H2O; Al2O3 + 2NaOH (распл) 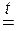 2NaAlO2 + H2O;
2NaAlO2 + H2O;
· Основных оксидов с кислотными:
BaO + CO2 = BaCO3;
· Амфотерных оксидов с кислотными оксидами:
ZnO + SO3 = ZnSO4;
· Амфотерных оксидов с основными оксидами:
ZnO + Na2O = Na2ZnO2;
· Кислот с основаниями:
HCl + NaOH = NaCl + H2O; 3H2SO4 + 2Bi(OH)3 = Bi2(SO4)3 + 6H2O;
· Амфотерных оснований со щелочами:
Cr(OH)3 + 3KOH(распл) = K3CrO3 + 3H2O;
· Металлов с кислотами:
Zn + H2SO4 = ZnSO4 + H2;
· Металлов с солями:
Zn + CuSO4 = ZnSO4 + Cu¯;
· Щелочей с солями:
2NaOH + FeCl2 = Fe(OH)2¯ + 2NaCl;
· Кислот с солями:
2HCl + K2SiO3 = H2SiO3¯ + 2KCl;
· Солей с солями:
AgNO3 + KBr = AgBr¯ + KNO3;
· Аммиака с кислотами:
NH3 + HNO3 = NH4NO3.
Дата добавления: 2015-09-18; просмотров: 641;
