Альфа-спираль-между NH группой 1 аминокислоты и СО другой
 1) Альфа-спираль- имеет определенные характеристики: ширину, расстояние между двумя витками спирали. Для белков характерна правозакрученная спираль. В этой спирали на 10 витков приходится 36 аминокислотных остатков. У всех пептидов, уложенных в такую спираль, эта спираль абсолютно одинакова. Фиксируется альфа-спираль с помощью водородных связей между NH-группами одного витка спирали и С=О группами соседнего витка. Эти водородные связи расположены параллельно оси спирали и многократно повторяются, поэтому прочно удерживают спиралеобразную структуру.
1) Альфа-спираль- имеет определенные характеристики: ширину, расстояние между двумя витками спирали. Для белков характерна правозакрученная спираль. В этой спирали на 10 витков приходится 36 аминокислотных остатков. У всех пептидов, уложенных в такую спираль, эта спираль абсолютно одинакова. Фиксируется альфа-спираль с помощью водородных связей между NH-группами одного витка спирали и С=О группами соседнего витка. Эти водородные связи расположены параллельно оси спирали и многократно повторяются, поэтому прочно удерживают спиралеобразную структуру.
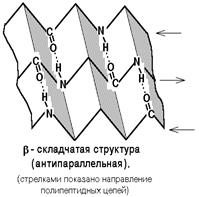
Бета-складчатая структура - или структура складчатого листа. Фиксируется также водородными связями между С=О и NH-группами. Фиксирует два участка полипептидной цепи. Эти цепи могут быть параллельны или антипараллельны. Если такие связи образуются в пределах одного пептида, то они всегда антипараллельны, а если между разными полипептидами, то параллельны.
3) Нерегулярная структура (синонимы: беспорядочный клубок, аморфные области) – тип вторичной структуры, в котором расположение различных участков полипептидной цепи относительно друг друга не имеет регулярного (постоянного) характера, поэтому нерегулярные структуры могут иметь различную конформацию.
Содержание a -спиралей и b -структур в разных белках различно: у фибриллярных белков - только a -спираль или только b -складчатый лист; а у глобулярных белков - отдельные фрагменты полипептидной цепи: либо a -спираль, либо b -складчатый лист, либо беспорядочный клубок. В одном и том же белке могут присутствовать все три способа укладки полипептидной цепи.
Третичная структура белка -это пространственная конформация полипептида, имеющего вторичную структуру, и обусловленная взаимодействиями между радикалами. Третичная структура полностью задается первичной.
Выделяют два общих типа третичной структуры:
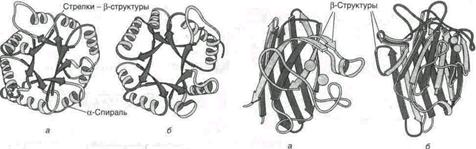
1) В фибриллярных белках (например, коллаген, эластин) молекулы которых имеют вытянутую форму и обычно формируют волокнистые структуры тканей, третичная структура представлена либотройной альфа-спиралью (например, в коллагене), либо бета-складчатыми структурами.
2) В глобулярных белках, молекулы которых имеют форму шара или эллипса (латинское название: GLOBULA - шар), встречается сочетание всех трех типов структур: всегда есть нерегулярные участки, есть бета-складчатые структуры и альфа-спирали. Третичная структура глобулярных белковпредставляет ориентацию в пространстве полипептидной цепи, содержащей a -спирали, b -структуры и участки без периодической структуры (беспорядочный клубок). Дополнительное складывание скрученной полипептидной цепи образует компактную структуру. Это происходит, прежде всего, в результате взаимодействия между боковыми цепями аминокислотных остатков.
Связи, стабилизирующие третичную структуру (рис.1):
1. электростатические силы притяжения между R-группами, несущими противоположно заряженные ионогенные группы (ионные связи);
2. водородные связи между полярными (гидрофильными)R-группами;
3. гидрофобные взаимодействия между неполярными (гидрофобными) R-группами.Гидрофобное ядро существует у большинства белков.
4. дисульфидные связи между радикалами двух молекул цистеина. Эти связи ковалентные. Они повышают стабильность третичной структуры, но не всегда являются обязательными для правильного скручивания молекулы. В ряде белков они могут вообще отсутствовать.
Примеры фибриллярных белков (рис.2).
Структурным белком, построенным преимущественно в виде α-спирали, является α-кератин. Волосы (шерсть), перья, иглы, когти и копыта животных состоят главным образом из кератина. Кератин (цитокератин) является важнейшей составной частью цитоскелета. В кератинах большая часть пептидной цепи свернута в правую α-спираль. Две пептидные цепи образуют единую левую суперспираль (или димер). Димеры кератина объединяются в тетрамеры, которые агрегируют с образованием протофибриллдиаметром 3 нм. Наконец, восемь протофибрилл образуют микрофибриллыдиаметром 10 нм.
Волосы построены из таких же фибрилл. Так, в отдельном волокне шерсти диаметром 20 мкм переплетены миллионы фибрилл. Отдельные цепи кератина скреплены поперечно многочисленными дисульфидными связями, что придает им дополнительную прочность.
Дата добавления: 2015-09-14; просмотров: 6655;
