Превращения алкадиенов и алкинов
Алкадиены и алкины термически более устойчивы, чем алкены. При относительно невысокой температуре (ниже 400°С) и давлении, близком к атмосферному, алкадиены превращаются быстрее других классов соединений. Основное направление реакции — диеновый синтез, протекающий по молекулярному механизму:
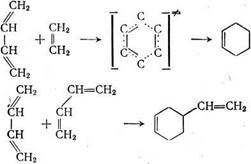
При температуре выше 700°С диеновый синтез протекает в незначительной степени, основное значение приобретает радикально-цепное разложение.
Цепной распад ацетилена можно представить схемой:
• •
2CHºCH ® CHºC + CH=CH2
• •
CHºC + CHºCH ® CHºCCH=CH
•
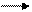
 CHºC–CºCH + H
CHºC–CºCH + H
• CHºCH
•
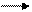
 CHºCCH=CH CHºCCH=CH2 + CHºC
CHºCCH=CH CHºCCH=CH2 + CHºC
CHºCH
•
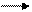 CHºCCH=CHCH=CH ®
CHºCCH=CHCH=CH ® 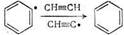
В результате радикально-цепного превращения ацетилена образуются сильноненасыщенные соединения большей молекулярной массы и арены.
Превращения аренов
Термическая устойчивость аренов сильно изменяется в зависимости от строения. Незамещенные и метилзамещенные бензол и нафталины значительно более устойчивы, чем алканы. Алкилзамещенные арены, имеющие связь С—С, сопряженную с кольцом, разлагаются быстрее алканов. Это объясняется распределением энергии между связями в молекуле (цифры — энергия связи в кДж/моль):

Термодинамически наиболее вероятным направлением термического превращения незамещенных аренов является распад на элементы. Однако эта реакция имеет место лишь при очень высокой температуре. В условиях термических процессов незамещенные арены подвергаются дегидроконденсации и уплотнению по цепному механизму. Бензол конденсируется по схеме
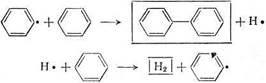
В результате образуются бифенил и водород.
Толуол при малой глубине крекинга подвергается разложению:
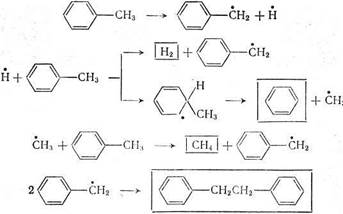
Бензильный радикал -(С6Н5СН2) малоактивен, он вступает главным образом в реакции рекомбинации, и цепи не развиваются. Скорость термического распада толуола в этом случае равна скорости разрыва связи С6Н5СН2—Н. Суммарные реакции превращения толуола можно представить как дегидроконденсацию с образованием дибензила и деметилирование до метана и бензола.
С повышением температуры концентрация бензильных радикалов при крекинге толуола возрастает за счет распада алифатической С—С-связи в дибензиле. Скорость продолжения цепи становится больше скорости распада толуола, и процесс развивается по цепному механизму:
•
• 
 С6Н5СН2 –
С6Н5СН2 – 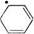 – СН3 ® (C6H5CH2C6H4CH3) + H
– СН3 ® (C6H5CH2C6H4CH3) + H
 С6Н5СН2 + С6Н5СН3 •
С6Н5СН2 + С6Н5СН3 •
 С6Н5СН2 –
С6Н5СН2 – 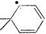 ® (С6Н5СН2C6H5) + СН3
® (С6Н5СН2C6H5) + СН3
Н3С
Алкилпроизводные аренов с длинными боковыми цепями в условиях термических процессов подвергаются распаду алкильных цепей. Инициирование реакции происходит путем разрыва слабейшей связи β-С—С, сопряженной с ароматическим кольцом:
α β • •
C6H5 – CH2 – CH2–R ® C6H5CH2 + CH2R
Основными продуктами процесса являются толуол, стирол и алкан.
Дата добавления: 2015-11-20; просмотров: 918;
