ГЛАВА 12
| Таблица 12.1. Применение аминокислот | |
| Аминокислота | Применение/Свойства |
| Аланин | Усилитель вкуса и аромата |
| Аргинин | Лечение заболеваний печей и |
| Аспарагин | Диуретик |
| Аспарагиновая кислота | Усилитель вкуса и аромата; синтез подсластителей |
| Валин | Растворы для внутривенных инъекций |
| Гистидин | Лечение язв; антиоксидант |
| Глицин | Синтез подсластителей |
| Глутамин | Лечение язв |
| Глутаминовая кислота | Усилитель вкуса и аромата |
| Изолейцин | Растворы для внутривенных инъекций |
| Лейцин | Растворы для внутривенных инъекций |
| Лизин | Кормовая добавка; пищевая добавка |
| Метионин | Кормовая добавка |
| Пролин | Растворы для внутривенных инъекций |
| Серин | Косметическая промышленность |
| Тирозин | Растворы для внутривенных инъекций: предшественник L-DOPA |
| Треонин | Кормовая добавка |
| Триптофан | Растворы для внутривенных инъекций; антиоксидант |
| Фенилаланин | Инфузии; синтез подсластителей |
| Цистеин | Производство хлеба; лечение бронхита; антиоксидант |
держать гены устойчивости к тетрациклину, хлорамфениколу или канамицину. Поскольку и E. coli, и Corynebacterium spp. чувствительны к данным антибиотикам, эти гены могли бы служить селективными маркерами для обоих микроорганизмов.
Эффективный метод трансформации С. glutamicum, одного из видов Corynebacterium, часто используемых в такого рода экспериментах, до сих пор не разработан. Многие гены С. glutamicum неэффективно экспрессируются в Е. coli. Поэтому для систем отбора, основанных на экспрессии гена (например, при комплементации), клетки С, glutamicum должны быть трансформированы полным банком клонов. К сожалению, частота трансформации при введении ДНК в С glutamicum обычным способом или электропорацией очень низка. Ее можно существенно повысить, если для введения чужеродной ДНК использовать конъюгацию или удалить клеточные стенки трансформируемых клеток лизоцимом (использовать протопласты). Проникновение экзогенной плазмидной ДНК в протопласты облегчается в присутствии полиэтиленгликоля.
Получены первые положительные результаты в увеличении выхода незаменимой аминокислоты триптофана, синтезируемой С glutamicum, Для этого в клетки С. glutamicum дикого типа была введена вторая копия гена, кодирующего антранилатсинтазу, фермент, лимитирующий синтез триптофана (рис. 12.8). Ниже описан один из способов выделения этого гена.
1. Библиотеку хромосомной ДНК Brevibacterium flavum клонировали в челночном векторе С. glutamicum—E. coli и ввели в мутантный штамм С. glutamicum, не синтезирующий активной антранилатсинтазы.
2. Трансформантов отобрали по их способности расти в отсутствие антраниловой кислоты. Этим они отличались от мутантных нетрансформированных клеток.
3. Вектор, содержащий ген антранилатсинтазы, перенесли в штамм С. glutamicum дикого типа.
В табл. 12.2 представлены результаты определения количества триптофана, синтезированного мутантным штаммом С. glutamicum и штаммом дикого типа, которые содержали или не содержали вектор с клонированным геном антранилатсинтазы. Как видно из таблицы, клони-
| Таблица 12.2. Синтез триптофана некоторыми штаммами С. glutamicum при стандартных условиях роста1) | |
| Штамм | Концентрация триптофана, мг/мл |

| |
| 1) По данным Ozaki etal. U.S. parent 4,874,698T 1989. |
Использование рекомбинантных микроорганизмов для получения коммерческих продуктов 257
| Рис. 12.8. Упрощенная схема биосинтеза триптофана в клетках С glutamicum. Сплошные линии — биосинтетические реакции, штриховые — ингибирование по типу обратной связи. В качестве побочного продукта образуется индол, который превращается в триптофан под действием триптофансинтазы ß. DS — 3-дезокси-D-арабиногептулозонат-7-фосфатсинтаза. ANS — антранилатсинтаза, PRT -антранилатфосфорибозилтрансфераза. | 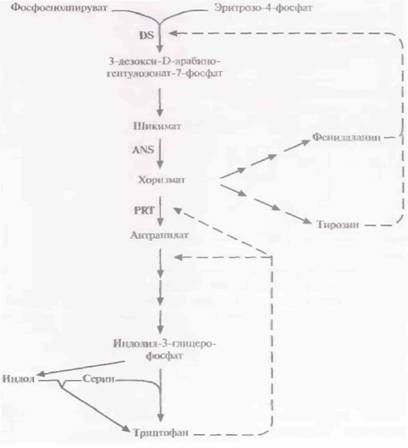
|
рованный ген практически полностью восстанавливал способность мутантного штамма синтезировать триптофан. Однако эффект введения этого гена в штамм дикого типа был еще сильнее: уровень синтеза триптофана в этом случае увеличивался примерно до 130%, что связано с более эффективным использованием доступных предшественников. Еще более высокий уровень синтеза триптофана достигался при введении в клетки С. glutamicum модифицированных генов трех ключевых ферментов: 3-дезокси-D-арабиногептулозонат-7-фосфатсинтазы, антранилатсинтазы и антранилатфосфорибозилтрансферазы. Гены, кодирующие эти ферменты, благодаря внесенным в них мутациям стали нечувствительны к ингибированию конечным продуктом (ингибирование по типу обратной связи).
В качестве альтернативы для синтеза аминокислот можно использовать E. coli. Этот микроорганизм хорошо изучен, а генноинженерные методы работы с ним более или менее детально разработаны.
Антибиотики
Со времени открытия пенициллина в конце 1920-х годов из различных микроорганизмов были выделены более 6000 антибиотиков, обладающих разной специфичностью и разным механизмом действия. Их широкое применение для лечения инфекционных заболеваний помогло сохранить миллионы жизней. Подавляющее большинство основных антибиотиков было выделено из гpaмположительной почвенной бактерии Strepfotnyces, хотя их продуцируют также грибы и другие грамположительные и грамотрицательные бактерии. Ежегодно во всем мире производится 100 000 т антибиотиков на сумму
258 ГЛАВА 12
примерно 5 млрд. долларов, в том числе более 100 млн. долларов приходится на долю антибиотиков, добавляемых в корм скоту в качестве добавок или ускорителей роста.
По оценкам, каждый год ученые обнаруживают от 100 до 200 новых антибиотиков, прежде всего в рамках обширных исследовательских программ по поиску среди тысяч различных микроорганизмов таких, которые синтезировали бы уникальные антибиотики. Получение и клинические испытания новых препаратов обходятся очень дорого, и в продажу поступают только те из них, которые имеют большую терапевтическую ценность и представляют экономический интерес. На их долю приходится 1—2% всех обнаруживаемых антибиотиков. Большой эффект здесь может дать технология рекомбинантных ДНК. Bo-первых, с ее помощью можно создавать новые антибиотики с уникальной структурой, оказывающие более мощное воздействие на определенные микроорганизмы и обладающие минимальными побочными эффектами. Во-вторых, генноинженерные подходы могут использоваться для увеличения выхода антибиотиков и соответственно для снижения стоимости их производства.
При создании рекомбинантных штаммов Streptomyces — основного микроорганизма, используемого для получения антибиотиков, – важно помнить, что трансформация и отбор трансформированных клеток не должны быть слишком сложными. Однако в отличие от Е. coli Streptomyces существуют не в виде изолированных клеток, а в виде протяженных мицелл, поэтому перед трансформацией необходимо разрушить клеточную стенку и высвободить отдельные протопласты (рис. 12.9). Без этого будет невозможно отличить трансформированные клетки от нетрансформированных, поскольку видимые колонии на твердой среде будут образовываться из группы клеток, а не из индивидуальной клетки; соответственно колонии, растущие в присутствии селективного антибиотика, будут представлять собой смесь трансформированных и нетрансформированных клеток. Проникновение плазмидной ДНК в протопласты Streptomyces облегчается в присутствии полиэтиленгликоля. После трансформации протопласты сначала высевают на твердую среду, чтобы образовалась
клеточная стенка, а затем для отбора трансформированных клеток переносят на селективную среду, обычно содержащую либо неомицин, либо тиострептон.
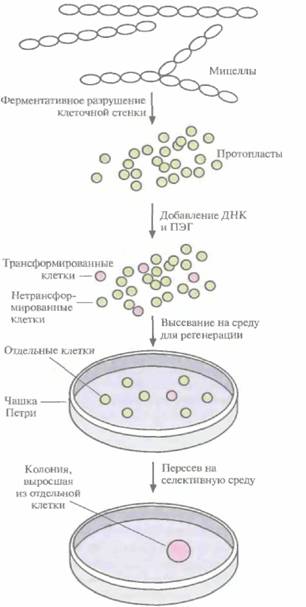
| Рис. 12.9. Схема трансформации и отбора рекомбинантных штаммов Sireptvmycea. Tрансформированные клетки обозначены розовыми кружками, нетрансформированные — зелеными. ПЭГ — полиэтиленгликоль. |
Использование рекомбинантных микроорганизмов для получения коммерческих продуктов 259
Клонирование генов биосинтеза антибиотиков
Процесс биосинтеза одного антибиотика может состоять из 10—30 ферментативных реакций, так что клонирование всех генов его биосинтеза -задача не из легких. Один из подходов к выделению полного набора таких генов основан на трансформации одного или нескольких мутантных штаммов, не способных синтезировать данный антибиотик, банком клонов, созданным из хромосомной ДНК. штамма дикого типа. После введения банка клонов в мутантные клетки проводят отбор трансформантов, способных синтезировать антибиотик. Затем выделяют плазмидную ДНК клона, содержащего функциональный экспрессируюшийся ген антибиотика [т. е. ген, восстанавливающий (комплементирующий) утраченную мутантным штаммом функцию], и используют ее в качестве зонда для скрининга другого банка клонов хромосомной ДНК штамма дикого типа, из которого отбирают клоны, содержащие нуклеотидные последовательности, которые перекрываются с последовательностью зонда. Таким образом идентифицируют, а затем клонируют элементы ДНК, примыкающие к комплементирующей последовательности, и воссоздают полный кластер генов биосинтеза антибиотика. Описанная процедура относится к случаю, когда эти гены сгруппированы в одном сайте хромосомной ДНК. Если же гены биосинтеза разбросаны в виде небольших кластеров по разным сайтам, то нужно иметь по крайней мере по одному мутанту на кластер, чтобы получить клоны ДНК, с помощью которых можно идентифицировать остальные гены кластеров.
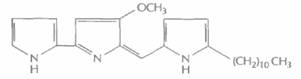
Этот подход с успехом использовался для идентификации некоторых генов биосинтеза ундецилпродигиозина из Streptomyces coelicolor A3 (рис. 12.10), В этом случае комплементационный анализ основывается на сравнении цвета колоний: колонии микроорганизмов дикого типа имеют красный цвет, а колонии мутантных микроорганизмов — кремовый. Таким образом, в результате комплементации образуется красная колония.
Помимо комплементации, для идентификации генов биосинтеза антибиотиков могут использоваться и более прямые подходы. Так, с
|
| Рис. 12.10. Структурная формула ундецилпродигиозина. |
помощью генетических или биохимических экспериментов можно идентифицировать, а затем выделить один или несколько ключевых ферментов биосинтеза, определить их N-концевые аминокислотные последовательности и, исходя из этих данных, синтезировать олигонуклеотидные зонды. Этот подход использовался для выделения из Pénicillium chrysogenutn гена синтетазы изопенициллина N. Этот фермент катализирует окислительную конденсацию δ-(L-α-аминоадипил)-L-цистеинил-D-валина в изопенициллин N, ключевое промежуточное звено в биосинтезе пенициллинов, цефалоспоринов и цефамицинов (рис. 12.11 ).
Синтез новых антибиотиков
Новые антибиотики с уникальными свойствами и специфичностью можно получить, проводя генноинженерные манипуляции с генами, участвующими в биосинтезе уже известных антибиотиков. Один из первых экспериментов, в ходе которого был получен новый антибиотик, состоял в объединении в одном микроорганизме двух немного различающихся путей биосинтеза антибиотика.
Одна из плазмид Streptomyces, рIJ2303, несущая фрагмент хромосомной ДНК S. coelicolor длиной 32,5 т.п.н., содержит все гены ферментов, ответственных за биосинтез из ацетата антибиотика актинородина, представителя семейства изохроманхиноновых антибиотиков (рис. 12.12). Целую плазмиду и различные субклоны, несущие части 32,5 т.п.н.-фрагмента (например, рIJ2315), вводили либо в штамм АМ-7161 Streptomyces sp., синтезиурующий родственный антибиотик медермицин, либо в штамм В1140 или Tü22 S. violaceoruber, синтезирующие родственные антибиотики гранатицин и дигидрогранатицин.
Все указанные антибиотики являются кислотно-щелочными индикаторами, которые при-
260 ГЛАВА 12
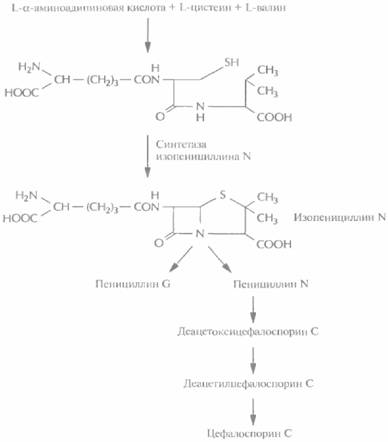
| Рис. 12.11. Биосинтез ленициллинов и цефалоспоринов в P. chrysogenum. Синтетаза изопенициллина N катализирует синтез из δ-(L-α-аминоалилил)-L-цистеинил-D-валина изопенициллина N — предшественника пенициллина G, пенициллина N и цефалоспорина С. |
дают растущей культуре характерный цвет, зависящий от pH среды (табл. 12.3). В свою очередь pH (и цвет) среды зависят от того, какое соединение синтезируется. Мутанты родительского штамма 5. coelicolor, не способные синтезировать актинородин, бесцветные. Появление окраски после трансформации штамма АМ-7161 Streptomyces sp. либо штаммов В1140 или Tü22 S. violaсеоruber плазмидой, несущей все или несколько генов, кодирующих ферменты биосинтеза актинородина, свидетельствует о синтезе нового антибиотика (рис. 12.12, табл. 12.3), Трансформанты штамма АМ-7161 Streptomyces sp. и штамма В1140 S. violaceoruber, содержащие плазмиду p[J2303, синтезируют антибиотики, кодируемые и плазмидой, и хромосомной ДНК. Однако при трансформации штамма Tü22 5. violaceoruber плазмидой pIJ2303 наряду с актинородином синтезируется новый антибиотик — Дигидрогранатиродин, а при трансформации штамма АМ-7161 Sireptomuces sp. плазмидой pIJ2315 синтезируется еще один новый антибиотик — медерродин А.
В структурном отношении эти новые антибиотики мало отличаются от актинородина, медермицина, гранатицина и гидрогранатицина и, вероятно, образуются в том случае, когда промежуточный продукт одного пути биосинтеза служит субстратом для фермента другого пути. Когда будут детально изучены биохимические свойства различных путей биосинтеза антибиотиков, появится возможность создавать новые уникальные высокоспецифичные антибиотики, манипулируя генами, которые кодируют соответствующие ферменты.
Разработка новых методов получения поликетидных антибиотиков
Термин «поликетидные» относится к классу антибиотиков, которые образуются в результате
Использование рекомбинантных микроорганизмов для получения коммерческихпродуктов 261
| Таблица 12.3. Антибиотики, синтезируемые различными штаммами Streptomyces, в том числе штаммами, трансформированными плазмидами pIJ2303 и pIJ23l51) | ||||
| Штамм/плазмида | Цвет культуры | Антибиотик(и) | ||
| кислая среда | щелочная среда | |||

| ||||
последовательной ферментативной конденсации карбоновых кислот типа ацетата, пропионата и бутирата. Некоторые поликетидные антибиотики синтезируются растениями и грибами, но большая их часть образуется актиномицетами в виде вторичных метаболитов. Прежде чем. проводить манипуляции с генами, кодирующими ферменты биосинтеза поликетидных антибиотиков, необходимо выяснить механизм действия этих ферментов.
Поликетидные антибиотики синтезируются по тому же пути, что и длинноцепочечные жирные кислоты. В результате каждого цикла конденсации к растущей углеродной цепи добавляется ß-кетогруппа. Процесс состоит из ряда повторяющихся стадий, включающих восстановление кетогруппы, дегидратацию и восстановление ß-еноильных групп в растущей поликетидной цепи. Существуют два класса поликетидсинтаз — ферментных комплексов, ответственных за синтез поликетидных антибиотиков (рис. 12.13). Первый класс составляют синтазы, катализируюшие реакции биосинтеза ароматических поликетидов; каждая синтаза представляет собой один полипептид с одним активным центром, который последовательно катализирует биосинтетические реакции (рис. 12.13, А). Второй класс включает синтазы, образованные несколькими полипептидами (А~Е на рис. 12.13, Б); каждый из них имеет свой активный центр и обладает специфической ферментативной активностью, катализирующей определенную реакцию биосинтеза.
Если каждый домен субъединицы многофункциональной поликетидсинтазы, обладающий ферментативной активностью, катализирует определенную реакцию, то утрата любой из активностей затронет только одну реакцию биосинтеза, а изменение домена с известной функцией приведет к предсказуемым изменениям структуры синтезируемого антибиотика. Так, детально изучив генетические и биохимические составляющие биосинтеза эритромицина в клетках Saccharopolyspora erythraea, удалось внести специфические изменения в гены, ассоциированные с биосинтезом этого антибиотика, и синтезировать производные эритромицина с другими свойствами. Вначале была определена первичная структура фрагмента ДНК 5, erythraea длиной 56т. п. н., содержащего кластер генов ery, затем двумя разными способами модифицирована эритромицинполикетидсинтаза. Для этого 1) удаляли участок ДНК, кодирующий ß-кеторедуктазу, либо 2) вносили изменение в участок ДНК, кодирующий еноилредуктазу. Делеция ß-кеторедуктазного гена приводила к накоплению промежуточного продукта, у которого к С-5-атому кольца была присоединена карбонильная группа, а не гидроксильная (рис. 12,14), а мутация в гене еноилредуктазы — к образованию двойной связи между атомами С-6 и С-7 (рис. 12.14). Из этих экспериментов следует, что если идентифицировать и охарактеризовать кластер генов, кодирующих ферменты биосинтеза определенного поликетидного антибиотика, то, внося в
262 ГЛАВА 12
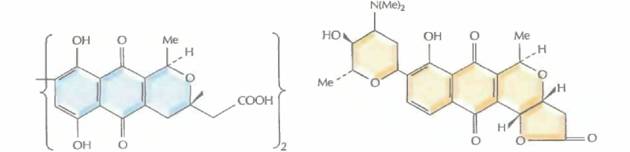
| |
| Актинородин | Медермицин |
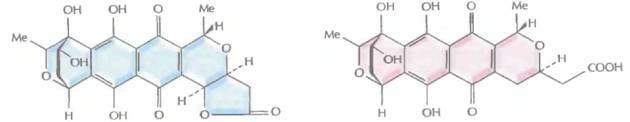
| |
| Гранатицин | Дигидрогранатицин |
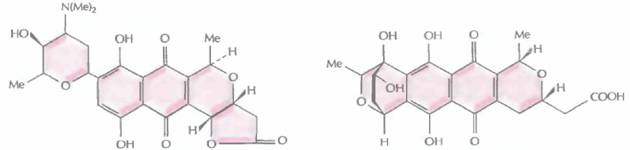
| |
| Медерродин А | Дигидрогранатиродин |
| Рис. 12.12. Структурные формулы различных изохроманхиноновых антибиотиков, синтезируемых штаммами Streptomyces. S. coelicolor дикого типа и плазмида рIJ2303 кодируют актинородин; Streptomyces sp. синтезирует медермицин, a S. violaceoruber — гранатицин и дигидрогранатицин. Синтезируемые гибридные антибиотики — это медерродин А и дигидрогранатиродин. |
них специфические изменения, можно будет направленно изменять структуру антибиотика. Кроме того, вырезая и соединяя те или иные участки ДНК, можно перемещать домены поликетидсинтазы и получать новые поликетидные антибиотики.
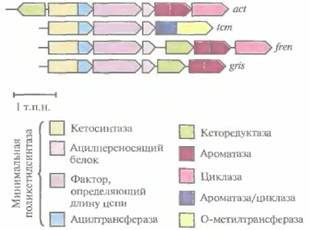
Все кластеры генов ароматических поликетидов содержат три гена, кодирующих так называемую минимальную поликетидсинтазу. Этот ферментный комплекс включает кетосинтазу (с ацилтрансферазным доменом), фактор, определяющий длину цепи, и ацилпереносящий белок. Минимальная поликетидсинтаза отвечает за синтез ароматического поликетидного остова, а его модификации осуществляются другими ферментами, действующими согласо-
Использование рекомбинантных микроорганизмов для получения коммерческих продуктов 263
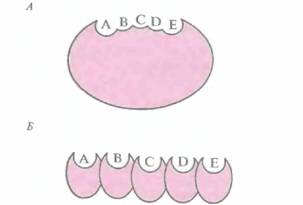
| Рис. 12.13. Схематическое изображение структуры поликетидсинтазы ароматических поликетидов, у которой активный центр находится в одном полипептиде (А), и поликетидсинтазы, представляющей собой комплекс нескольких полипептидов с разными активными центрами (Б). Ферменты обоих типов содержат несколько доменов (А— Е), каждый из которых обладает собственной ферментативной активностью. |
ванно с ней. Гены, кодирующие все эти ферменты, обычно организованы в один кластер (рис. 12.15). Каждый кластер генов кодирует синтез определенного антибиотика. С помощью обмена генами между кластерами были синтезированы два новых ароматических поликетидных антибиотика (рис. 12.16), что еще раз иллюстрирует возможности генной инженерии.
Усовершенствование производства антибиотиков
С помощью генной инженерии можно не только создавать новые антибиотики, но и увеличивать эффективность синтеза уже известных. Лимитирующим фактором в промышленном производстве антибиотиков с помощью Streptomyces spp. часто является количество доступного клеткам кислорода. Вследствие плохой растворимости кислорода в воде и высокой плотности культуры Sireptomyces его часто оказывается недостаточно, рост клеток замедляется и выход антибиотика снижается. Чтобы решить эту проблему, можно, во-первых, изменить конструкцию биореакторов, в которых выращивается культура Streptomyces, a во-вторых, используя методы генной инженерии, создать штаммы Streptomyces, более эффективно использующие имеющийся кислород. Эти два подхода не исключают друг друга.
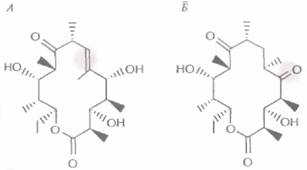
| Рис. 12.14. Производные эритромицина, полученные генноинженерными методами. А, В результате мутации в гене еноилредуктазы образуется продукт с двойной связью между атомами С-6 и С-7 (цветной кружок). Б. Делеция гена ß-кеторедуктазы сопровождается образованием производного с С-5-карбонильной, ане гидроксильной группой (цветной кружок). (По данным работы Kutz, Donadio, Annu. Rev. Microbiol. 47: 875-912, 1993.) |
|
| Рис. 12.15. Кластер генов биосинтеза ароматических поликетидных антибиотиков актинородина (act), тетраценомицина (tcm), френолицина (fren) и гризеузина (gris). Каждый кластер содержит гены, кодирующие минимальную поликетидсинтазу, которая отвечает за синтез поликетидного остова. Ферменты, кодируемые другими генами, катализируют реакции его модификации. Сужающийся «конец» гена указывает направление его транскрипции. |
264 ГЛАВА 12
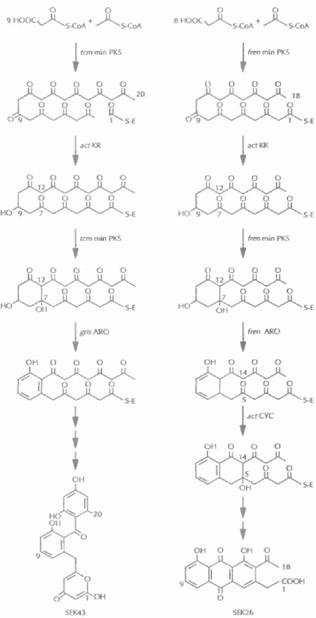
| Рис. 12.16. Искусственно созданные пути биосинтеза поликетидных антибиотиков SEK43 и SEK26- Обозначения: act — актинородин, tст — тетраценомицин, fren — френолицин, gris -гризеузин, min PKS — минимальная поликетидсинтаза, KR — ß-кеторедуктаза. ARO -ароматаза, CYC — цикл а за. |
Одна из стратегий, используемых некоторыми аэробными микроорганизмами для выживания в условиях недостатка кислорода, состоит в синтезе гемоглобинподобного продукта, способного аккумулировать кислород и доставлять его в клетки. Например, аэробная бактерия Vitreoscilla sp. синтезирует гомодимерный гемсодержащий белок, функционально подобный эукариотическому гемоглобину. Ген «гемоглобина» Vitreoscilla
был выделен, встроен в плазмидный вектор Streptomyces и введен в клетки этого микроорганизма. После его экспрессии на долю гемоглобина Vitreoscilla приходилось примерно 0,1% всех клеточных белков S. coelicolor даже в том случае, когда экспрессия осуществлялась под контролем собственного промотора гена гемоглобина Vitreoscilla, а не промотора Streptomyces. Трансформированные клетки S. coelicolor, растущие
Использование рекомбинантных микроорганизмов для получения коммерческих продуктов 265

| ||
| Получение 2-кето-L-гулоната промежуточного продукта синтеза L- аскорбиновой кислоты — с помощью рекомбинантной бактерии Erwinia herbicola | ||
| S. Anderson, С. В, Marks, R. Lazarus. J. Miller, K. Stafford, J. Serymour, D. Light, W. Rastetter, D, Este» Science 230: 144-149, 1985 | ||
| Для направленного изменения прокариот, синтезирующих определенные метаболиты, в принципе есть два пути. Во-первых, можно изменить активность или содержание одного или нескольких ферментов того или иного биосинтетического пути с тем, чтобы увеличить продукцию нужного метаболита. Во-вторых, в прокариотический геном можно ввести чужеродные гены, кодирующие ферменты, которые, используя эндогенный метаболит в качестве субстрата, обеспечат синтез метаболита, изначально не продуцируемого хозяйской клеткой. Такого рода манипуляции представляются достаточно простыми, однако далеко не всегда | удается выделить нужный ген и подобрать подходящие условия для его экспрессии. Чтобы создать бактерию, синтезирующую 2-кето-L-гулоновую кислоту, непосредственного предшественника витамина С в промышленном производстве этого витамина, Андерсон и др. выделили из Corynebacterium ген фермента, катализирующего превращение 2,5-дикето-D-глюконовой кислоты в 2-кето-L-гулоновую кислоту, и ввели этот ген в клетки Erwinia sp. — бактерии, синтезирующей 2,5-дикето-Dглюконовую кислоту из D-глюкозы. Выделение этого гена осложнялось тем, что сам фермент практически не был изучен. Та- | ким образом, прежде чем идентифицировать ген, нужно было очистить соответствующий белок и частично секвенировать его, а затем на основании данных об аминокислотной последовательности сконструировать зонды для гибридизации. Это была одна из первых работ, относящихся к той области исследований, которую иногда называют инженерией метаболизма. В такого рода работах из одного микроорганизма в другой переносят гены, ответственные за какую-то часть метаболического пути, так что второй микроорганизм приобретает способность синтезировать новые метаболиты. |
при низком содержании растворенного кислорода (примерно 5% от насыщающей концентрации), синтезировали в 10 раз больше актинородина на 1 г сухой клеточной массы и имели большую скорость роста, чем нетрансформированные. Этот подход можно использовать и для обеспечения кислородом других микроорганизмов, растущих в условиях недостатка кислорода. Исходным материалом при химическом синтезе некоторых цефалоспоринов — антибиотиков, обладающих незначительным побочным эффектом и активных в отношении множества бактерий, — является 7-аминоцефалоспорано-вая кислота (7АСА), которая в свою очередь синтезируется из антибиотика цефалоспорина С (рис. 12,11 ). К сожалению, природных микроорганизмов, способных синтезировать 7АСА, до сих пор не выявлено. Новый путь биосинтеза 7АСА был сконструирован включением специфических генов в плазмиду гриба Acremonium chrysogenum, который обычно синтеризует только цефалоспорин С. Один из этих генов был представлен кДНК гриба Fusarium solani, кодирующей оксидазу D-аминокислот, а другой происходил из геномной ДНК Pseudomonas diminuta и кодировал цефалоспоринацилазу. В плазмиде гены находились под контролем промотора A. chrysogenum. На первом этапе нового биосинтетического пути цефалоспорин С превращается в 7-β-(5-карбокси-5-оксопентанамид)цефалоспорановую кислоту (кето-АD-7АСА) при помощи оксидазы D-аминокислот (рис. 12.17). Часть этого продукта, вступая в реакцию с пероксидом водорода, одним из побочных продуктов, превращается в 7-р-(4-карбоксибутанамид)цефалоспорановую кислоту (GL-7ACA). И цефалоспорин С, и кето-АD-7АСА, и GL-7ACA могут подвергаться гидролизу цефалоспоринацилазой с образованием 7АСА, однако только 5% цефалоспорина С напрямую гидролизуется до 7АСА. Следовательно, для образования 7АСА с высоким выходом необходимы оба фермента.
266 ГЛАВА 12
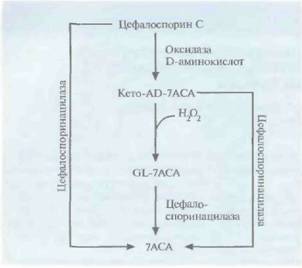
| Рнс. 12.17. Генетически сконструированный путь биосинтеза 7-аминоцефалоспорановой кислоты (7АСА) из цефалоспорина С. Ген оксидазы D-аминокислот выделен из гриба F. solani, a ген цефалоспоринацилазы - из бактерии P. diminuta. |
Биополимеры
Биополимеры — это высокомолекулярные соединения, синтезируемые живыми организмами. Некоторые из них обладают ценными физическими и химическими свойствами и могут использоваться в пищевой, перерабатывающей и фармацевтической промышленности. С возникновением технологии рекомбинантных ДНК появилась возможность создавать новые биополимеры, заменять синтетические продукты их биологическими аналогами, модифицировать уже существующие биополимеры с целью улучшения их физических и структурных характеристик, повышать эффективность соответствующих промышленных процессов, уменьшать их стоимость.
Создание рекомбинантной бактерии Xanthomonas campestris с целью получения ксантановой слизи
Xanthomonas campestris — грамотрицательная облигатно аэробная почвенная бактерия, синтезирующая ценный коммерческий биополимер ксантановую слизь, высокомолекулярный экзополисахарид Его структурный каркас составляет линейная полимерная цепь из молекул глюкозы. К каждому второму глюкозному остатку присоединена трисахаридная боковая цепь, состоящая из однго остатка глюкуроновой кислоты и двух остатков маннозы (рис. 12,18). Ксантановая слизь имеет высокую вязкость, не разрушается в агрессивных физических и химических средах и по физическим и химическим свойствам напоминает пластик. В частности, ее можно использовать как стабилизирующий, эмульгирующий, загущающий или суспендирующий агент. Для успешного коммерческого производства ксантановой слизи необходимо выращивать X. campestris на недорогом и доступном источнике углерода. X. campestris дикого типа эффективно утилизирует глюкозу, сахарозу и крахмал, но не лактозу. При производстве сыра в большом количестве образуется такой побочный продукт, как сыворотка. Она состоит из воды (94—95%), лактозы (3,5—4%) и небольших количеств белка, минеральных веществ и низкомолекулярных органических соединений. Огромные количества сыворотки дает молочная промышленность, и ее утилизация — это большая проблема. Часто сыворотку сливают в реки и озера, что приводит к уменьшению в них количества доступного кислорода и гибели многих водных организмов. Транспортировка сыворотки к местам захоронения мусора обходится очень дорого, к тому же серьезную проблему создает риск загрязнения ею грунтовых вод. Наконец, большие средства уходят на удаление твердых компонентов сыворотки. Все это заставило попытаться найти способы выгодной переработки сыворотки.
Сыворотку можно использовать как источник углерода при выращивании ценных промышлен-
Использование рекомбинантныхмикроорганизмов для получения коммерческих продуктов 267
| Рис. 12.18. Структурная формула полисахарида, образующего ксантановую слизь. Каркас составляет линейная полимерная цепь из молекул глюкозы. К каждому второму остатку присоединена трисахаридная боковая цепь. | 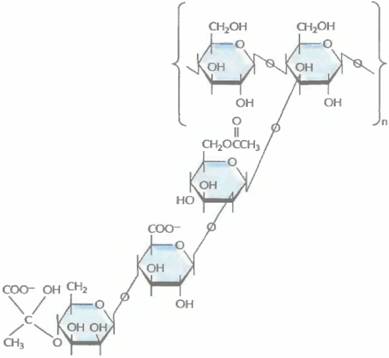
|
ных микроорганизмов. Чтобы X. campestris приобрела способность расти на сыворотке, было проделано следующее. Гены lacZY E. coli, кодирующие ферменты ß-галактозидазу и лактозо-пермеазу, встроили в плазмиду с широким кругом хозяев так, чтобы они находились под транскрипционным контролем промотора одного из бактериофагов X. campestris. Эту конструкцию ввели в Е. coli, а затем перенесли из E. coli в X. campestris тройным скрещиванием. Трансформанты, содержащие плазмиду, синтезировали ß-галактозидазу и лактозопермеазу, используя лактозу как единственный источник углерода, а также продуцировали в больших количествах ксантановую слизь, используя в качестве источников углерода глюкозу, лактозу и сыворотку (табл. 12.4). Подчеркнем еще раз, что X. campesfrïs дикого типа синтезирует много ксантановой слизи, только когда растет на глюкозе.
Выделение генов биосинтеза меланина
Меланины образуют многочисленное семейство различных поглощающих свет биополимеров; их синтеризуют животные, растения, бактерии и грибы. Эти пигменты можно было бы использовать при изготовлении солнцезащитных экранов и покрытий, в качестве добавки к косметическим средствам. В настоящее время меланины получают в небольших количествах либо экстракцией из природных источников, либо путем химического синтеза. С помощью технологии рекомбинантных ДНК, возможно, удастся создать недорогое крупномасштабное производство меланинов с различными физическими свойствами.
| Таблица 12,4, Синтез ксантановой слизи в трансформированных клетках Х. campestris и клетках дикого типа, растущих в среде с разными источниками углерода 1) | |||
| X. campestris | Количество ксантановой слизи, мкг/мл1) | ||
| 0,4% глюкоза | 0,4% лактоза | 10% сыворотка | |
| Дикий тип | |||
| Трансформант | |||
| 1) По данным работы Fu, Tseng, Appl. Environ. Micibbioi. Sfc 919—923, 1990. | |||
| 2) Количество образующегося продукта выражено б числе микрограммов на 1 мл культуры, растущей на минимальной среде в присутствии 0,4% глюкозы или 0,4% лактозы либо на разбавленной (10%) сыворотке, содержащей примерно 0, 4% лактозы. Трансформант содержит плазмиду, несущую гены lacZY E. coli. |
Дата добавления: 2015-07-14; просмотров: 1636;
