Глава 3. СТРУКТУРА ИММУННОЙ СИСТЕМЫ
Постоянный контроль генетического постоянства состава внутренней среды а, в случае обнаружения посторонних антигенов, создание и использование индивидуальных (специфичных) защитных программ, требуют тесного взаимодействия различных органов, тканей и клеток иммунной системы.
3.1. Органы и ткани иммунной системы
Иммунная система млекопитающего представлена лимфомиелоидными органами и лимфоидной тканью. Её центральные отделы преимущественно обеспечивают образование клеток, участвующих в иммунном ответе, а в периферических органах и тканях в основном происходит нейтрализация антигенов.
К центральным структурам иммунной системы относятся: костный мозг, вилочковая железа и сумка Фабрициуса.
Красный костный мозг служит источником полипотентной стволовой кроветворной клетки, из которой в постнатальном периоде образуются все клетки крови (рис. 2).
Образующаяся из полипотентной стволовой кроветворной клетки миелоидная стволовая клетка дает четыре ростка: мегакариоцитарный, эритроидный, гранулоцитарный и моноцитарно-макрофагальный. После ряда превращений из мегакариоцитарного ростка развиваются тромбоциты, из эритроидного - эритроциты, гранулоцитарного - нейтрофилы, эозинофилы и базофилы, а из моноцитарно-макрофагального - моноциты. Лимфоидная стволовая клетка в красном костном мозге обеспечивает лишь ранние этапы созревания лимфоцитов. После завершения пролиферации и дифференцировки в красном костном мозге, клетки поступают в кровь. Причем, лейкоциты (нейтрофилы, базофилы, эозинофилы, моноциты и лимфоциты) через некоторое время покидают кровеносное русло и расселяются вне его. Часть В-лимфоцитов после контакта с антигеном в периферических лимфоидных органах возвращается в красный костный мозг (или периферические лимфоидные органы) и здесь созревает до плазматических клеток (плазмоцитов). При новом или длительном контакте с тем же антигеном В-клетки обеспечивают эффективную гуморальную защиту животного.
| Стволовая кроветворная клетка | ||||||||||||||||||||||||||||||||||||||||||||
| Миелоидная стволовая клетка | Лимфоидная стволовая клетка | |||||||||||||||||||||||||||||||||||||||||||
| Мегакариоцитарный росток | Эритроидный росток | Гранулоцитарный росток | Моноцитарно-макрофагальный росток | |||||||||||||||||||||||||||||||||||||||||
| Тромбоцит | Эритроцит | Нейтрофил | Эозинофил | Базофил | Промоноцит | Пре-Т-лимфоцит | Пре-0-лимфоцит | В-лимфоцит | ||||||||||||||||||||||||||||||||||||
| Рис. 2. Схема кроветворения в красном костном мозге | ||||||||||||||||||||||||||||||||||||||||||||
Таким образом, наряду с функцией кроветворения, красный костный мозг участвует в развитии реакций В-лимфоцитов на антигены.
Тимус (вилочковая железа) является основным источником новых клонов зрелых Т-лимфоцитов. Основу паренхимы вилочковой железы составляют продуцирующие «тимические» гормоны эпителиальные клетки и эпителиальные образования (тимические тельца).
Эпителиальные клетки вилочковой железы продуцируют тимические гормоны влияющие паракринным и эндокринным путями на гемопоэз, а также на дифференцировку и активность Т-клеток. Здесь на предшественников Т-лимфоцитов действует тимопоэтин (ускоряет преимущественно пролиферацию клеток), а затем тимозины, которые делают дифференцирующиеся клетки чувствительными к тимулину, способствующему созреванию Т-клеток в тимусе и вне его. Кроме этого, выделенные в кровь гормоны тимуса осуществляют контроль за нейромышечной передачей и состоянием углеводного обмена в целостном организме. Секреция тимических гормонов регулируется глюкокортикоидами и СТГ.
В коре тимуса пре-T-лимфоциты дифференцируются, а затем образующиеся из них субпопуляции проверяются по способности реагировать на собственные молекулы ГКГС (в них заложена информация о своих нормальных антигенах). Активирующиеся при этом клетки уничтожаются (отрицательная селекция), а остальные на поверхности крупных эпителиальных клеток окончательно созревают и скапливаются в мозговом веществе железы вместе с пришедшими туда из крови малыми В-лимфоцитами (необходимы для формирования иммунной памяти).
В эмбриогенезе тимус формируется раньше других лимфоидных образований и к рождению является самым большим лимфоидным органом у млекопитающего. Вес вилочковой железы увеличивается до начала полового созревания. После этого эпителиальные клетки железы постепенно замещаются периваскулярными пространствами, фибриллярными структурами и жировой тканью. Однако небольшие дольки функционируют в тимусе и до глубокой старости.
Возрастная атрофия железы связана с уменьшением потребности макроорганизма в формировании новых клонов Т-клеток. Дело в том, что большинство уже образованных клонов является долгоживущими, а вероятность встречи особи с новыми антигенами с возрастом уменьшается.
Сумка Фабрициуса (бурса) обеспечивает формирование и созревание B-лимфоцитов у птиц. У млекопитающих бурса не обнаружена, а ее функции, вероятно, выполняют: красный костный мозг, лимфоидные ткани в стенках желудочно-кишечного тракта и миндалины.
К периферическим структурам иммунной системы относятся: селезенка, лимфатические узлы, миндалины носоглотки, пейеровы бляшки кишечника, лимфоидные узелки, диффузная лимфоидная ткань, лимфоидные клетки кожи и межэпителиальные лимфоциты.
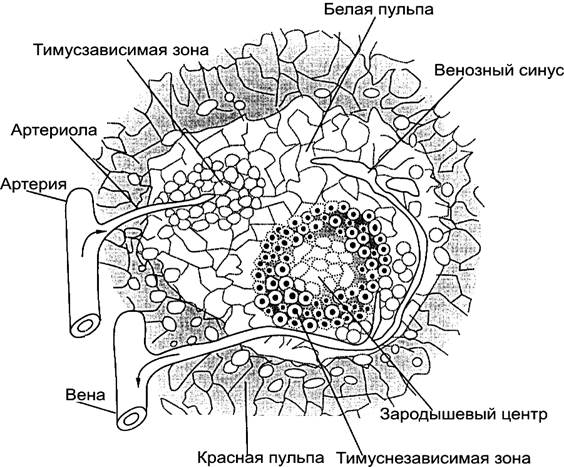
Селезенка в пренатальный период функционирует как орган кроветворения. Затем у большинства млекопитающих (у грызунов он сохраняется всю жизнь) гемопоэз в ней прекращается. Функциональной единицей селезенки (рис. 3) являются связанные с одной артериолой красная и белая пульпы. Однако, основным местом протекания иммунных реакций в селезенке является только белая пульпа.
|
| Рис. 3. Функциональная единица селезенки |
Она представляет собой лимфоидные фолликулы, состоящие в основном из богатых Т-лимфоцитами периартериальных муфт (тимусзависимая зона) и расположенных ближе к венозному синусу богатых В-лимфоцитами тимуснезависимых зон. В этой зоне В-клетки при контакте с антигенами дифференцируются до плазматических клеток и образуют зародышевые центры (или «центры размножения»), а в тимусзависимой зоне Т-клетки становятся Т-лимфобластами.
Описанная структура позволяет белой пульпе селезенки очищать кровь от чужеродных частиц, участвовать в выработке антител и обеспечивать развитие иммунного ответа.
Лимфатические узлы расположены в месте слияния афферентных лимфатических сосудов и обильно снабжаются кровью. Из нее лимфоциты переходят в паренхиму узлов. При этом в тимуснезависимой зоне коркового вещества оседают преимущественно В-клетки, а в тимусзависимой зоне паракортикального вещества (расположено между корой и мозговым веществом) - Т-клетки (преимущественно T-киллеры).
В местах скопления В-клеток формируются первичные фолликулы, которые через 4-5 сут после первого контакта находящихся в них наивных лимфоцитов с антигеном превращаются в зародышевый центр, содержащий В-лимфоциты, макрофаги и дендритные клетки. Повторное или длительное поступление того же антигена в узел вызывают разрастание данного центра и быстрое образованием в нем плазматических клеток.
В мозговом веществе узла в небольшом количестве представлены различные лимфоциты, плазмоциты и свободные макрофаги.
Притекающая к узлам по афферентным сосудам лимфа представляет собой смесь ультрафильтрата плазмы крови с накопившимися в межклеточных пространствах различных органов и тканей крупными частицами. В силу больших размеров, они не могут перейти через стенку кровеносного сосуда в кровь и вместе с накапливающейся в межклеточных пространствах водой переходят в лимфатические капилляры, которые затем объединяются в афферентные лимфатические сосуды. Через них в лимфатические узлы поступают: собственные поврежденные, или инфицированные клетки, бактерии, вирусы, токсины и другие высокомолекулярные продукты жизнедеятельности. Перечисленные частицы фильтруются через корковое и мозговое вещество узлов. Здесь лимфа становится практически стерильной и нетоксичной, насыщается лимфоцитами (из тимусзависимой и тимуснезависмой зон узла) и другими факторами иммунитета, а затем по эфферентным лимфатическим сосудам поступает в кровь.
Таким образом, лимфа удаляет из тканей и органов избыток межклеточной жидкости вместе с растворенными в ней крупными частицами (дренажная функция), а также доставляет лимфоциты в кровь.
В области главных «входных ворот» для антигенов, поступающих с кормом, вдыхаемым воздухом и через мочеполовой тракт расположены лимфоидные фолликулы, миндалины носоглотки, пейеровы бляшки, лимфоидные узелки и диффузная лимфоидная ткань. Они заселены В-лимфоцитами (при контакте с антигеном обеспечивают преимущественную секрецию IgA), которые вместе с T-клетками и фагоцитами препятствуют проникновению через ближайшей слизистой оболочке патогенов.
Таким образом, в центральных органах иммунной системы происходит антигеннезависимое созревание, а в периферических - специализация лимфоцитов и протекание их реакций на антиген. Перечисленные структуры связаны между собой. Перемещаясь по кровеносными и лимфатическим сосудам, лимфоциты получают информацию об антигене и передают ее в другие образования иммунной системы.
3.2. Клетки иммунной системы
В отличие от строго локализованных (неподвижных) органов и тканей иммунной системы, ее клетки присутствуют практически во всех жидких средах организма. Они сами способны приближаться даже к неподвижным чужеродным частицам и приводить к их нейтрализации, а также обеспечивают взаимосвязь всех структур иммунной системы.
3.2.1. Лимфоциты
Главными эффекторными клетками иммунной системы являются лимфоциты. Они после дифференцировки в центральных органах иммунной системы мигрируют в периферические лимфоидные структуры, а через некоторое время возвращаются в кровь. Такая циркуляция лимфоцитов обеспечивает обнаружение ими антигенов в любых внеклеточных средах организма и способствует своевременному развитию иммунных реакций.
Зрелые лимфоциты делят на Т-зависимые, В-зависимые и нулевые.
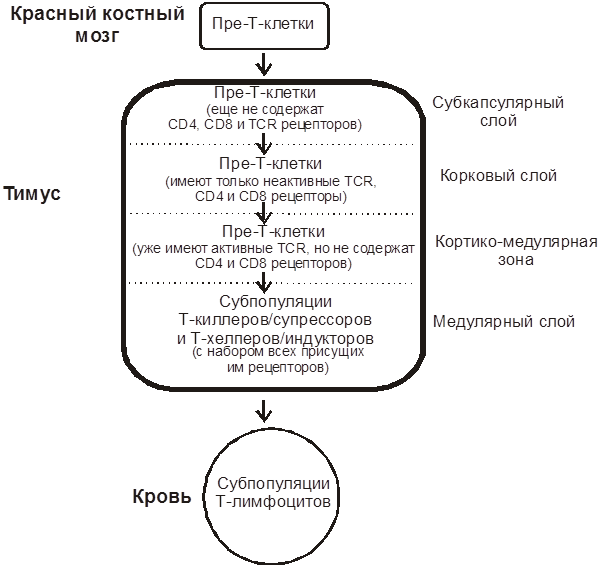
Т-лимфоциты образуются в паренхиме тимуса из пре-T-клеток (рис. 4). По мере созревания на Т-клетках появляются характерные для каждой субпопуляции маркеры (обозначаются буквами CD и порядковым номером обнаружения). Например, на поверхности всех T-киллеров и T-супрессоров имеются маркеры CD8, а на Т-хелперах - CD4.
Только что вышедшие из тимуса зрелые лимфоциты называют наивными, так как они еще не «знакомы» с чужими антигенами, но уже не реагируют на собственные. Затем Т-клетки мигрируют в периферические лимфоидные ткани и ждут там встречи с ранее не попадавшим в данный организм «чужим» антигеном. Его появление вызывает образование специфичных клонов T-клеток, а оставшиеся наивными T-лимфоциты мигрируют в другие периферические структуры иммунной системы.
Сформировавшиеся субпопуляции Т-клеток по их свойствам делятся на киллеры, супрессоры, хелперы и клетки памяти.
Т-киллеры (цитотоксические T-лимфоциты или ЦТЛ) созревают при специфическом распознавании (в присутствии T-хелперов первого типа и макрофагов) их предшественниками инфицированных клеток. Затем в области контакта с мишенью проявляется антителонезависимая клеточно опосредованная цитотоксичность зрелых Т-киллеров. Для этого они выделяют цитотоксины (основными являются перфорины и гранзимы) и (или) оказывают прямое действие на Fas-рецепторы мишеней. Оба перечисленных механизма запускают апоптоз в клетках (характеристика апоптоза дана в разделе, посвященном естественным киллерам).
|
| Рис. 4. Локализация процессов созревания Т-лимфоцитов в тимусе. |
Один Т-киллер может уничтожить несколько клеток, затрачивая на обработку каждой из них около пяти минут («серийный убийца»).
Наряду с антителонезависимой клеточно опосредованной цитотоксичностью, Т-киллеры формируют иммунологическую память, а также синтезируют γ-интерферон и факторы некроза опухоли (стимулируют макрофаг и развитие иммунного воспаления).
T-киллеры и T-супрессоры нередко рассматривают как самостоятельные субпопуляции. Но, возможно, одна CD8+ субпопуляция Т-лимфоцитов (в зависимости от конкретных условий) может быть как ЦТЛ, так и супрессором. Даже зрелые Т-киллеры могут рассматриваться как супрессоры, если они вызывают апоптоз иммунокомпетентных клеток (этот механизм может своевременно прекратить ставшие избыточными иммунные реакции).
Предшественники T-хелперов (Т0-хелперы) при встрече с тимусзависимым антигеном на антигенпредставляющей клетке (в зависимости от содержания цитокинов в окружающей среде) превращаются в Т-хелперы клеточного (Т-хелперы первого типа) или гуморального (Т-хелперы второго типа) иммунитета.
Контакт Т0-хелпера со специфичной антигенной детерминантой на инфицированном бактериями макрофаге вызывает преимущественное образование T-хелперов первого типа. Этому способствует усиленная секреция цитокинов (ИЛ-12 и γ-интерферона) макрофагами, а также естественными киллерами и цитотоксическими лимфоцитами.
Приобнаружении тимусзависимых антигенов на B-лимфоцитах, специфичные Т0-хелперы дифференцируются до Т-хелперов второго типа. Этому способствует секреция цитоканов (ИЛ-4 и 13) базофилами, тучными клетками, эозинофилами и γδТ-лимфоцитами.
Обе зрелые субпопуляции Т-хелперов секретируют цитокины влияющие на гемопоэз (например, ИЛ-3 и ГМ-КСМ). Дополнительно к перечисленному, Т-хелперы первого типавыделяют в окружающую их среду цитокины (например, γ-интерферон, факторы некроза опухоли, ИЛ-2 и 12) ускоряющие пролиферацию цитотоксических T-лимфоцитов и стимулирующие макрофаги, а Т-хелперы второго типа секретируют цитокины (например, ИЛ-4, -5, -6, -9, -10 -13) стимулирующие пролиферацию и дифференцировку B-лимфоцитов до плазмоцитов, а также синтез более эффективных антител. Дополнительно к перечисленному, цитокины Т-хелперов гуморального иммунитета вызывают хемотаксис гранулоцитов в очаг воспаления и активируют тучные клетки.
У новорожденных преобладают Т-хелперы второго типа, а развитию Т-хелперов второго типа способствует заселение пищеварительного тракта нормальной микрофлорой.
В то же время, Т-хелперы гуморального или клеточного иммунитетаоказывают супрессорное влияние друг на друга, а одновременная активация T-хелперов двух типов - тормозит все варианты иммунного ответа.
В связи с этим среди иммуноцитов специальных популяций супрессоров может и не быть, но в определенных условиях проявляются супрессорные эффекты цитотоксических лимфоцитов и двух типов Т-хелперов.
Менее 1% от общего пула Т-лимфоцитов составляет особая γδТ-популяция. Она происходят из мигрировавших в покровы тела (на ранних этапах эмбриогенеза) стволовых клеток и созревает вне тимуса. Практически все γδТ-лимфоциты локализуются в эпидермисе и слизистой пищеварительного тракта. Они активируются поврежденными клетками эпителия покровов тела и наиболее распространенными микробными антигенами. Перечисленные свойства позволяют γδТ-лимфоцитам быстро включаться в борьбу с патогенами на ранних этапах противоинфекционной защиты. Для этого γδТ-лимфоциты секретируют цитокины, активирующие местный иммунитет и развитие воспаления, а также контролирующие численность собственной популяции.
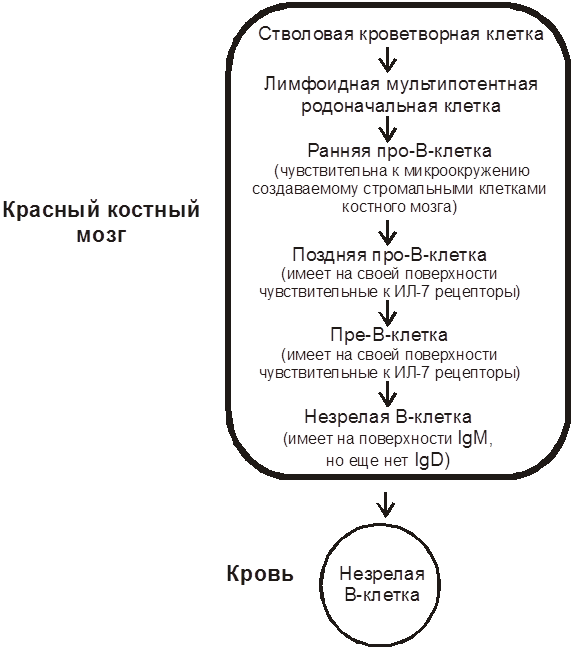
У взрослых млекопитающих основные этапы дифференцировки B-лимфоцитов происходят в красном костном мозге (рис. 5). Непосредственное их развитие начинается образованием ранней про-B-клетки.
Затем, в присутствии цитокинов (в первую очередь ИЛ-7) последовательно образуются поздняя про-B-клетка, пре-B-клетка и незрелый B-лимфоцит, на поверхности которого появляется рецептор, содержащий первый иммуноглобулин класса M.
|
| Рис. 5. Последовательность образования В-лимфоцитов в красном костном мозге. |
После этого лимфоциты подвергаются селекции, в ходе которой разрушаются клетки, реагирующие на собственными нормальные антигены.
Остальные еще наивные (то есть еще не знакомые с чужим антигеном) В-лимфоциты поступают в кровь, а затем заселяют тимуснезависимые зоны периферических лимфоидных органов. Здесь клетки ожидают встречи с новым антигеном. Если этого не происходит, они через определенное время рециркулируют и оседают в других лимфоидных образованиях.
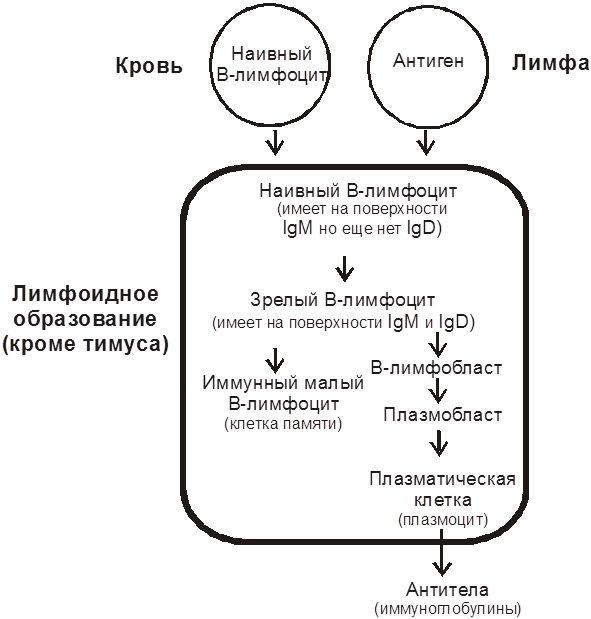
Встретившийся с антигеном B-лимфоцит (под влиянием вырабатываемых моноцитами, макрофагами и T-хелперами гуморального иммунитета цитокинов) активируется и созревает (на нем появляется IgD и могут присутствовать другие специфичные к тому же антигену классы иммуноглобулинов). Затем он дифференцируется (рис. 6) до плазмоцитов (служат основным источником антител) и долгоживущих B-лимфоцитов, которые до повторного контакта с тем же антигеном выполняют функцию клеток памяти, а при очередной специфической стимуляции (уже знакомым антигеном) обеспечивают более быстрый и эффективный иммунный ответ.
Зрелый В-лимфоцит способен реагировать на антигены, иммуноглобулины, компоненты комплемента, цитокины, T-лимфоциты и макрофаги.
Некоторые антигены (например, эндотоксины, полисахарид стрептококков, белки жгутиков бактерий) являются тимуснезависимыми. Их высокие концентрации вызывают пролиферацию и дифференцировку даже неспецифичных B-клеток, а в малых концентрациях стимулируют лишь специфичные клоны. Такие реакции быстро развиваются, не требуют присутствия Т-хелперов второго типа, не обеспечивают формирования иммунной памяти и ограничены продукцией лишь низкоафинных IgM.
Подобные реакции в отсутствии Т-клеток вызывают и тимусзависимые антигены. Однако в лимфоидной ткани при образовании комплекса В-лимфоцитов с тимусзависимым антигеном и Т-хелперами гуморального иммунитета, часть клона В-лимфоцитов перемещается в зародышевый центр (под действием выделяемого Т-клетками ИЛ-4). Здесь под действием ИЛ-5 и ИЛ-6 (также выделяются Т-хелперами второго типа) В-клетки пролиферируют и дифференцируются до плазмоцитов, которые затем переключаются на синтез более эффективных классов антител.
|
| Рис. 6. Этапы дифференцировки В-лимфоцитов после первой встречи с тимусзависимым антигеном. |
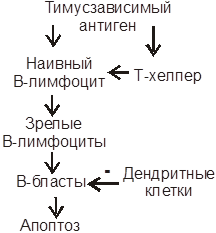
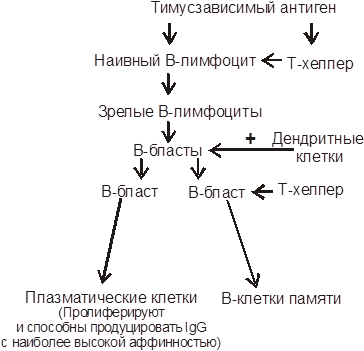
Иммунный ответ на впервые обнаруженный тимусзависимый антиген формирует клоны, вырабатывающие разные по афинности антитела. Поэтому, образующиеся в зародышевых центрах В-бласты, при участии дендритных клеток подвергаются селекции по афинности (рис. 7). В ходе ее уничтожаются продуценты низкоафинных иммуноглобулинов, а клоны, секретирующие высокоафинные IgG, сохраняются, пролиферируют и дифференцируются. Часть таких клеток (при участии Т-хелперов) становится клетками памяти, которые быстро возобновляют секрецию тех же антител при новом контакте с антигеном.
| 
|
| А | Б |
| Рис.7. Схема селекции клеток по афинности вырабатываемых ими антител: А- с низкой афинностью и Б - с высокой афинностью. Условные обозначения: + - положительная селекция, - - отрицательная селекция. | |
При первом контакте с тимусзависимым антигеном наблюдается первичный иммунный ответ.
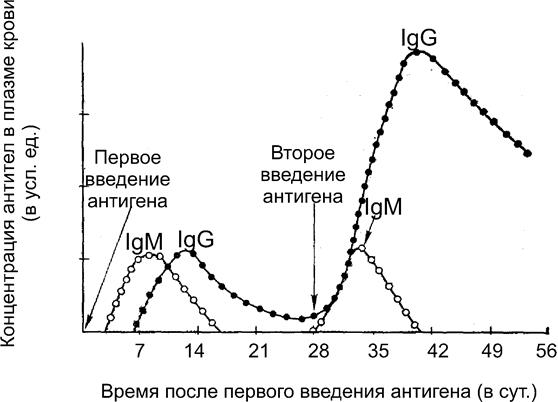
Его можно разделить на 4 стадии (рис. 8). На первой стадии (занимает 3-4 сут после первого контакта с антигеном), антитела к соответствующему антигену отсутствуют. На второй стадии первичного иммунного ответа появляются IgM, а спустя 7-14 суток (продолжительность образования необходимых для этого плазмоцитов) после контакта с антигеном - IgG. На третьей стадии уровень антител остается относительно постоянным, а на четвертой стадии (может растягиваться на месяцы) наблюдается постепенное снижение уровня антител.
|
| Рис. 8. Кинетика изменения концентрации IgM и IgG в плазме крови при первичном и вторичном иммунных ответах на один и тот же тимусзависимый антиген |
При следующей встрече или продолжительном контакте с тем же антигеном (вторичный иммунный ответ) выработка IgM близка к ответу при первичном иммунном ответе. В то же время, концентрация IgG нарастает быстрее, достигает бόльших величин и медленнее снижается.Это связано с наличием иммунологической памяти, которую обеспечивают юные плазмоциты, не закончившие ранее полный цикл трансформации.
Формирование иммунологической памяти обеспечивает устойчивость к повторному заражению инфекционными болезнями. После первичной иммунизации через 10-20 дней количество клеток памяти достигает максимума и держится на постоянном уровне от нескольких месяцев до нескольких лет. У клеток иммунологической памяти специфичный антиген вызывает пролиферацию и дифференцировку, которая заканчивается образованием плазмоцитов за 2-3 дня.
Таким образом, важным результатом иммунного ответа является формирование клеток памяти. Под ними подразумевают те долгоживущие предшественники наиболее мощных эффекторных Т- и В-лимфоцитов, которые сформировались в ходе развития предыдущей иммунной реакции на тот же тимусзависимый антиген. При вторичном иммунном ответе, часть ранее возникших клеток служит источником новых эффекторных клеток, а часть сохраняется для обеспечения последующих ответов.
Нулевые лимфоцитынесколько крупнее B- и T-лимфоцитов, имеют бобовидное ядро, в их цитоплазме много азурофильных гранул. Поэтому их часто называют большими гранулярными лимфоцитами. По своим функциям нулевые клетки отличаются от B- и T-лимфоцитов тем, что не распознают антиген и не образуют клетки памяти. Однако после миграции в периферические лимфоидные структуры нулевые лимфоциты могут созревать до Т- и В-клеток.
Сами 0-лимфоциты благодаря наличию на их поверхности рецепторов к наиболее общим фрагментам иммуноглобулина, могут оказывать цитотоксическое действие на клетки, поверхность которых покрыта антителами.
Следовательно, нулевые лимфоциты (их наиболее изученным представителем являются NK-клетки) преимущественно участвуют в неспецифических, а Т- и В-клетки – антигенспецифических механизмах защиты.
3.2.2. Антигенпредставляющие клетки
Если В-клетки чувствительны только к растворенным (нативным) специфическим антигенам, то Т-лимфоциты реагируют лишь на комплексы определенных антигенных детерминант с молекулами ГКГС на поверхности антигенпредставляющих (антигенпрезентирующих) клеток.
Главной их особенностью является способность поглощать антиген, а затем выделять из него наиболее иммуногенные пептиды и размещать их на своей поверхности в комплексе с молекулами ГКГС. Это специфически влияет на субпопуляции T-лимфоцитов и обеспечивает поддержание памяти об антигене.
Функции презентации антигена выполняют макрофаги, целая группа дендритных клеток, B-лимфоциты, а также некоторые эндотелиальные, глиальные и другие клетки.
Макрофаги,даже при незавершенном фагоцитозе, размещаются на своей поверхности в комплексе с молекулами ГКГС II класса наиболее иммуногенные фрагменты фагоцитированных структур. Это позволяет лимфоцитам обнаруживать и «атаковать» инфицированные фагоциты.
Дендритные клетки в строме лимфоидных органов поглощают белки и вирусные частицы, поступившие по афферентным сосудам с лимфой, а затем экспрессируют на своей поверхности их иммуногенные фрагменты. Это способствует дифференцировке окружающих дендритные клетки наивных T-лимфоцитов до зрелых Т-хелперов первого или второго типа и поддерживает иммунологическую память.
Дендритные клетки тимуса активируют селекцию клонов T-лимфоцитов.
Клетки Лангерганса связывают проникающий через кожу антиген и с ним мигрируют в лимфатические узлы. Здесь клетки Лангерганса становятся зрелыми дендритными клетками, завершают обработку антигена и также размещают его на своей поверхности.
Дендритные клетки слизистых оболочек взаимодействуют с антигенами в лимфоидных фолликулах, а образовавшийся на них комплекс антигена с молекулой ГКГС активирует T-хелперы (преимущественно второго типа) и ускоряет образование плазмоцитов.
B-лимфоциты выполняют функцию антигенпредставляющих клеток при контакте с нативными бактериальными эндотоксинами и другими чужеродными белками в наружных слоях коры лимфоидных органов. Здесь B-клетки поглощают антиген, а затем размещают его фрагмент в комплексе с молекулой ГКГС на своей поверхности.
Дата добавления: 2015-07-14; просмотров: 1766;
