Методы выделения и очистки белков. Методы выделения и очистки касаются не только белков, но это ещё и универсальные методы, которые используются в биохимии
Методы выделения и очистки касаются не только белков, но это ещё и универсальные методы, которые используются в биохимии. Клетки содержат большое количество разных белков.Прежде, чем исследовать индивидуальный белок, необходимо получить (вытащить) его из общей массы.
Методы:
1. Необходимо измельчить биоматериал.
2. Из этой гомогенной массы извлечь все белки.
3. Затем разделить эти белки на определённые фракции или отдельные белки.
Обычные методы органической химии не подойдут. Используя обычные методы можно прийти к тому, что белок теряет природные (нативыные свойства).
Методы гомогенезации: используют различные гомогенезеторы(ножевые, пестиковые, шаровые мельницы). Успешно используют метод попеременного замораживания и размораживания тканей, при этом происходит разрыв оболочек кристалликами льда. Иногда используют метод замораживания с применением пресса. Для извлечения белков из микробной ткани используют метод азотной бомбы, т.е. микробные клетки насыщают азотом под давлением, затем резко сбрасывают давление и выделившийся газ взрывает клетки.
После гомогенизации начинают экстракцию белков.
Проводят диализ – отделение ВМС от НМС. Проводят в мешочках из полупроницаемой плёнки (с микропорами), через которую могут проходить НМС. Помещают гомогенезированный материал в диализный мешок и помещают в дестиилированную воду. Это до тех пор, пока качественная реакция не будет давать продукты.
После гомогенизации начинают экстракцию белков от других больших молекул. Для этого надо перевести белки в растворенное состояние, экстрагировать белки разными растворами (водные растворы, солевые растворы, растворы глюкозы). Растворение белков в воде связано с гидратацией каждой молекулы, что приводит к образованию вокруг каждой молекулы белка водных гидратных оболочек. По своим физическим и химическим свойствам вода гидратных оболочек отличается от воды-растворителя.
Нитевидные белки – плохо растворимы в воде, глобулярные – растворяются в воде.
Если в такой коллоидный раствор прилить водоотнимающее средство, то разрушается гидратная оболочка, белки начинают слипаться, происходит осаждение белков в осадок. Этот метод используется для выделения того или иного белка, называется высаливание, для него используют любые водоотнимающие средства (спирт, соли щелочных металлов). После удаления высаливающего раствора белок может перейти в растворимое состояние, не теряя своих нативных свойств. Этот метод используется в медицине – метод Кона: при перегонке крови, при низких температурах –3 -5 градусов белки плазмы кровы разделяют по фракциям, применяя различные концентрации этанола.
Самый распространенный и универсальный метод разделения – метод хроматографии, принцип разработан русским химиком Цветом.
Существует 4 основных типа:
1. адсобрбционная;
2. распределительная;
3. ионообменная;
4. хроматография по сродству (аффинная хроматография).
При адсорбционной хроматографии разделение компонентов смеси основано на их различной полярности, в качестве адсорбента используют активированный уголь, Al2O3, Si2O3. Адсорбент в виде суспензии помещают в колонку. Образец в небольшом количестве растворителя тоже помещается в колонку. Белки адсорбируются в определенном слое адсорбента. Для разделения белков производят элюирование, элюент – полярный растворитель, буферные растворы, которые будут по-разному действовать на разные белки.
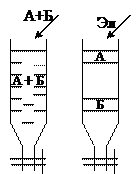 Частным случаем такой адсорбционной хроматографии является тонкослойная хроматография.
Частным случаем такой адсорбционной хроматографии является тонкослойная хроматография.
Распределительная хроматография наиболее часто используется в биохимии. Твердая фаза адсорбент служит только основой для стационарной жидкой фазы (крахмал – твердая фаза, вода – жидкая). Образец растворяют в органическом растворителе и пропускают через колонку. Различные белки, имея различное сродство к воде и органическим растворителям, растворяются в колонке и передвигаются ко дну колонки с разной скоростью.
Ионообменная хроматография.
Здесь используют ионообменные смолы – катиониты (катионный обмен) и аниониты (анионный обмен). Полистиролсульфокислоты или их соли. 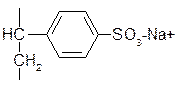
Белки, которые имеют положительный заряд, они будут способны к катионному обмену, а другие белки, которые не имеют заряда, они будут свободно проходить через эту колонку. Анионный обмен – наоборот. Солевыми насыщенными растворами проводят снятие белков с адсорбента.
Аффинная хроматография основана на принципе избирательного взаимодействия белка со специфическими веществами, называемыми лигандами, которые закреплены на носителе. Например, смесь белков содержит амиллазу, при прохождении через крахмальную прослойку, амилаза будет адсорбироваться на крахмале, а другие белки будут проходить мимо.
В последнее время широкое применение получила гель-фильтрация или метод молекулярных сит. С помощью этого метода можно рассортировать белки по их размерам, по величине. Для этого смесь белков пропускают через колонку, заполненную очень мелкими пористыми гранулами высокогидратированного полимера (дексатраны – полисахариды бактерии, состоят из молекул глюкозы, полимерная цепочка которых имеет очень разветвлённое строение). (связи 1-4, 1-6). Маленькие молекулы будут проходить через поры, а большие нет, т.о. происходит разделение белков по молекулярной массе. Этот метод в настоящее время очень широко используется в фармакологии, биохимических производствах.
Дата добавления: 2015-08-20; просмотров: 1942;
